МІНІСТЕРСТВО ОХОРОНИ ЗДОРОВ’Я УКРАЇНИНАКАЗ03 серпня 2021 року № 1614Про організацію профілактики інфекцій та інфекційного контролю в закладах охорони здоров’я та установах / закладах надання соціальних послуг / соціального захисту населення
Зареєстровано в Міністерстві юстиції України
11 жовтня 2021 р. за № 1318/36940
Останні зміни внесено: наказ Міністерства охорони здоров'я України від 21.02.2023 № 354
Відповідно до абзаців другого, тринадцятого, шістнадцятого, вісімнадцятого статті 6 Закону України «Про захист населення від інфекційних хвороб», підпункту 1 пункту 1 додатку 3 до Порядку укладення, зміни та припинення договору про медичне обслуговування населення за програмою медичних гарантій, затвердженого постановою Кабінету Міністрів України від 25 квітня 2018 року № 410 (в редакції постанови Кабінету Міністрів України від 27 листопада 2019 року № 1073), підпунктів 5, 11 пункту 3 Національного плану дій щодо боротьби із стійкістю до протимікробних препаратів, затвердженого розпорядженням Кабінету Міністрів України від 06 березня 2019 року № 116-р, пункту 8 Положення про Міністерство охорони здоров’я України, затвердженого постановою Кабінету Міністрів України від 25 березня 2015 року № 267 (в редакції постанови Кабінету Міністрів України від 24 січня 2020 року № 90), з метою забезпечення належної організації профілактики інфекцій та інфекційного контролю в закладах охорони здоров’я та установах / закладах надання соціальних послуг / соціального захисту населення
НАКАЗУЮ:
1. Затвердити такі, що додаються:
1) Порядок здійснення епідеміологічного нагляду та ведення обліку інфекційних хвороб, пов’язаних з наданням медичної допомоги;
2) Порядок профілактики інфекційних хвороб, пов’язаних з наданням медичної допомоги, в закладах охорони здоров’я, які надають медичну допомогу в стаціонарних умовах;
3) Порядок впровадження профілактики інфекцій та інфекційного контролю в закладах охорони здоров’я, які надають медичну допомогу в стаціонарних умовах;
4) Інструкцію з впровадження покращення гігієни рук в закладах охорони здоров’я та установах / закладах надання соціальних послуг / соціального захисту населення;
5) Інструкцію з впровадження адміністрування антимікробних препаратів в закладах охорони здоров’я, які надають медичну допомогу в стаціонарних умовах;
6) Положення про відділ з інфекційного контролю закладу охорони здоров’я та установи / закладу надання соціальних послуг / соціального захисту населення;
7) Зміни до деяких нормативно-правових актів Міністерства охорони здоров’я України.
2. Визнати такими, що втратили чинність:
1) наказ Міністерства охорони здоров’я України від 10 травня 2007 року № 234 «Про організацію профілактики внутрішньолікарняних інфекцій в акушерських стаціонарах», зареєстрований в Міністерстві юстиції України 21 червня 2007 року за № 694/13961;
2) наказ Міністерства охорони здоров’я України від 04 квітня 2012 року № 236 «Про організацію контролю та профілактики післяопераційних гнійно-запальних інфекцій, спричинених мікроорганізмами, резистентними до дії антимікробних препаратів», зареєстрований в Міністерстві юстиції України 06 червня 2012 року за № 912/21224.
3. Уважати такими, що не застосовуються на території України:
1) наказ Міністерства охорони здоров’я СРСР від 31 липня 1978 року № 720 «Об улучшении медицинской помощи больным с гнойными хирургическими заболеваниями и усилении мероприятий по борьбе с внутрибольничной инфекцией»;
2) наказ Міністерства охорони здоров’я СРСР від 04 серпня 1983 року № 916 «Об утверждении Инструкци по санитарно-противоэпидемическому режиму и охране труда персонала инфекционных больниц (отделений)»;
3) наказ Міністерства охорони здоров’я СРСР від 08 грудня 1989 року № 691 «О профилактике внутрибольничных инфекций в акушерских стационарах»;
4) наказ Міністерства охорони здоров’я СРСР від 03 грудня 1989 року № 654 «О совершенствовании системы учета отдельных инфекционных и паразитарных заболеваний».
4. Державній установі «Центр громадського здоров’я Міністерства охорони здоров’я України» (Родина Р. А.) забезпечити:
1) координацію та інформаційно-консультативний супровід закладів і установ охорони здоров’я та закладів громадського здоров’я з організації та впровадження профілактики інфекцій та інфекційного контролю, покращення гігієни рук, епідеміологічного нагляду за інфекційними хворобами, пов’язаними з наданням медичної допомоги і адміністрування антимікробних препаратів;
2) координацію та інформаційно-консультативний супровід закладів громадського здоров’я з організації та проведення дозорного епідеміологічного нагляду за інфекційними хворобами, пов’язаними з наданням медичної допомоги, і моніторингу споживання антимікробних препаратів;
3) збір, узагальнення, аналіз даних та подання інформації до Міністерства охорони здоров’я України щодо інфекційних хвороб, пов’язаних з наданням медичної допомоги і споживання антимікробних препаратів;
4) розробку рекомендацій щодо планування та організації заходів профілактики і ліквідації спалахів інфекційних хвороб, пов’язаних із наданням медичної допомоги.
5. Національній службі здоров’я України забезпечити розширення функціональних можливостей Реєстру медичних записів, записів про направлення та рецептів в електронній системі охорони здоров’я для внесення до нього записів згідно із нормативно-правовими актами, затвердженими цим наказом.
6. Директорату громадського здоров’я та профілактики захворюваності (Руденко I. С.) забезпечити подання цього наказу в установленому законодавством порядку на державну реєстрацію до Міністерства юстиції України.
7. Контроль за виконанням цього наказу залишаю за собою.
8. Цей наказ набирає чинності з дня його офіційного опублікування, крім підпунктів 1, 5 пункту 1, які набирають чинності з 01 січня 2022 року.
Міністр
В. Ляшко
ПОГОДЖЕНО:
Міністр соціальної політики України
М. Лазебна
Голова Державної регуляторної служби України
О. Кучер
В. о. Президента НАМН України
Д. Заболотний
Уповноважений Верховної Ради України з прав людини
Л. Денісова
Керівник Секретаріату Спільного представницького органу
сторони роботодавців на національному рівні
Р. Іллічов
ЗАТВЕРДЖЕНО
Наказ Міністерства охорони здоров’я України
03 серпня 2021 року № 1614
Порядок здійснення епідеміологічного нагляду та ведення обліку інфекційних хвороб, пов’язаних з наданням медичної допомоги
I. Загальні положення
1. Цей Порядок визначає організаційні заходи та процедури для проведення епідеміологічного нагляду за інфекційними хворобами, пов’язаними з наданням медичної допомоги (далі — ІПНМД) в закладах охорони здоров’я (далі — ЗОЗ), які надають медичну допомогу у стаціонарних умовах.
2. У цьому Порядку терміни та умовні скорочення вживаються у такому значенні:
HelicsWin.Net — програмне забезпечення, розроблене Європейським центром контролю і профілактики захворювань, для введення і аналізу даних моніторингу ІПНМД;
девайс-асоційовані ІПНМД — ІПНМД, пов’язані з встановленням та використанням медичних виробів (наприклад, внутрішньосудинні катетери, інтубаційні трубки, сечові катетери, внутрішньовенні порти, ендопротези, металоконструкції для екстра- та інтрамедулярного остеосинтезу, кардіовертер-дефібрилятор, електроди, інсулінові помпи, вентрикулярні шунти, дренажі, стоми);
дозорний епідеміологічний нагляд за ІПНМД — епідеміологічний нагляд, заснований на зборі якісних даних щодо ІПНМД та антимікробної резистентності, що надаються у вигляді звітів/форм;
епідеміологічний нагляд за ІПНМД — це система збору, аналізу та інтерпретації даних щодо ІПНМД (захворюваність, летальність, колонізація, носійство), факторів та умов, що впливають на їх виникнення і розповсюдження;
індикаторна подія — подія, що вказує на неспроможність ЗОЗ попередити ІПНМД і потребує індивідуального розслідування;
інцидентність — кількість нових випадків захворювання, які виникають в певній популяції за встановлений період часу;
превалентність — загальна кількість всіх активних (нових та вже існуючих) випадків захворювання в певній популяції або за встановлений період часу (превалентність періодична), або в певний момент часу (точкова чи одномоментна превалентність);
рутинний епідеміологічний нагляд за ІПНМД — регулярний, систематичний збір визначених даних щодо ІПНМД;
щільність інцидентності — значення можливості виникнення захворювання відносно розмірів вільної від захворювання популяції (наприклад, кількість ІПНМД на 1000 ліжко-днів);
АМР — антимікробна резистентність;
АМП — антимікробні препарати;
ВАРІТ — відділення анестезіології, реанімації та інтенсивної терапії, включно з палатами інтенсивної терапії;
ІОХВ — інфекція області хірургічного втручання;
ВІК — відділ з інфекційного контролю;
МАМР — множинна резистентність мікроорганізмів до АМП;
ОРІПНМД — одномоментна розповсюдженість ІПНМД;
ПІІК — профілактика інфекцій та інфекційний контроль;
СОП — стандартна операційна процедура.
Інші терміни у цьому Порядку вживаються у значеннях, наведених в Законах України «Основи законодавства України про охорону здоров’я», «Про захист населення від інфекційних хвороб» та інших нормативно-правових актах у сфері охорони здоров’я.
3. На національному рівні до функцій епідеміологічного нагляду за ІПНМД відносяться моніторинг та аналіз захворюваності на ІПНМД, підготовка інформації для прийняття управлінських рішень, підготовка даних звітності для інтеграції у європейську і міжнародну системи даних щодо ІПНМД та АМР.
4. На регіональному рівні (обласний, на рівні територіальних громад та окремих ЗОЗ) завданням епідеміологічного нагляду за ІПНМД є здійснення моніторингу за динамікою епідемічного процесу, факторами та умовами, що впливають на їх виникнення та розповсюдження, узагальнення та аналіз одержаної інформації для розробки профілактичних та протиепідемічних заходів.
5. У ЗОЗ проводиться епідеміологічний нагляд за ІПНМД як постійно діюча комплексна система спостереження за причинами епідемічного процесу з метою профілактики ІПНМД та АМР та складова системи ПІІК ЗОЗ.
6. Епідеміологічний нагляд за ІПНМД здійснюється шляхом впровадження рутинного та дозорного епідеміологічного нагляду за ІПНМД відповідно до цього Порядку.
7. Епідеміологічний нагляд за ІПНМД не є державним наглядом (контролем) у сфері господарської діяльності у розумінні Закону України «Про основні засади державного нагляду (контролю) у сфері господарської діяльності».
8. Для здійснення епідеміологічного нагляду за ІПНМД враховуються такі епідеміологічні особливості ІПНМД:
1) множинність механізмів та шляхів передавання інфекційних агентів: природні (контактно-побутовий, повітряно-краплинний, фекально-оральний) та артифіційні (штучні) — внаслідок інвазивних діагностичних і лікувальних процедур;
2) джерелом ІПНМД можуть бути, але не обмежуються ними:
хворі, які перебувають на амбулаторному чи стаціонарному лікуванні у ЗОЗ;
медичні працівники;
особи, які здійснюють догляд за хворими, відвідувачі, інфіковані або контаміновані мікроорганізмами;
матері в акушерських та дитячих ЗОЗ;
конструктивні елементи приміщень, медичні і немедичні вироби та обладнання;
3) етіологічними збудниками ІПНМД є група патогенних та умовно-патогенних мікроорганізмів;
4) для кожного ЗОЗ характерний свій спектр пріоритетних збудників ІПНМД, який може змінюватися.
9. Випадки ІПНМД та АМР визначаються за Критеріями, за якими визначаються випадки інфекційних та паразитарних захворювань, які підлягають реєстрації, затвердженими наказом Міністерства охорони здоров’я України від 28 грудня 2015 року № 905, зареєстрованими в Міністерстві юстиції України 12 березня 2016 року за № 379/28509 (далі — Критерії).
II. Організація та проведення рутинного епідеміологічного нагляду за інфекційними хворобами, пов’язаними із наданням медичної допомоги
1. Система рутинного епідеміологічного нагляду за ІПНМД (далі — рутинний епіднагляд) за ІПНМД базується на виявленні індикаторних подій, спостереженні за популяцією пацієнтів в цілому або поєднанні обох цих підходів.
2. Рутинний епіднагляд, що базується на виявленні індикаторних подій, виявляє лише найбільш серйозні порушення в ПІІК і не може бути єдиним способом проведення епіднагляду в ЗОЗ через отримання показників, які не мають жодного відтворюваного зв’язку із реальними показниками.
3. Рутинний епіднагляд, що базується на популяційному підході — нагляд за всіма пацієнтами, які мають ризик розвитку ІПНМД, що потребує збору даних про кількість випадків ІПНМД, кількість пацієнтів в групі ризику, кількість днів експозиції до фактору ризику тощо.
4. Цілі рутинного епіднагляду:
1) економічна оцінка заходів з ПІІК;
2) контроль якості медичної допомоги;
3) раціональне планування заходів з ПІІК із врахуванням місцевих особливостей, в тому числі наявних ресурсів;
4) управління ризиками;
5) отримання нових наукових даних.
5. Дані, які оцінюються при епідеміологічному нагляді за ІПНМД, поділяються на три типи:
1) демографічні — можуть різнитися для різних ІПНМД;
2) дані щодо випадку ІПНМД — отримуються шляхом аналізу форм збору даних рутинного епіднагляду (далі — форм);
3) результати лабораторних досліджень.
6. Рутинний епіднагляд проводиться епідеміологом ВІК мінімум щодо наступних ІПНМД:
1) катетер-асоційованих інфекцій кровотоку (форми збору даних наведено в додатках 1, 2 до цього Порядку);
2) катетер-асоційованих інфекцій сечовивідних шляхів (форму збору даних наведено в додатку 3 до цього Порядку);
3) вентилятор-асоційованих пневмоній (форму збору даних наведено в додатку 4 до цього Порядку);
4) інфекцій області хірургічного втручання (форми збору даних наведено в додатках 5, 6 до цього Порядку).
7. Форми, наведені у додатках 1, 2, 3, 4, 5 до цього Порядку, заповнюються лікарем-епідеміологом / помічником лікаря-епідеміолога. Форма, наведена в додатку 6 заповнюються лікуючим лікарем (хірургом).
8. Щодо ІПНМД розраховуються лише відносні показники, які виражають частоту їх виникнення серед пацієнтів з груп ризику.
9. Показники ІПНМД розраховуються за певний період часу за формулами:
1) розповсюдженість катетер-асоційованих інфекцій кровотоку по відділенням (рекомендовано розраховувати окремо для центральних і периферичних катетерів):
РК = КК / ККД × 1000, де
РК — розповсюдженість катетер-асоційованих інфекцій кровотоку у відділенні на 1000 катетер-днів;
КК — кількість зареєстрованих катетер-асоційованих інфекцій кровотоку у відділенні за період часу;
ККД — загальна кількість катетер-днів у відділенні за період часу — сума днів наявності встановленого катетера у пацієнтів, в яких не розвинулася катетер-асоційована інфекція кровотоку та днів наявності встановленого катетера у пацієнтів до початку клінічних проявів катетер-асоційованої інфекції кровотоку;
1000 — 1000 катетер-днів;
2) розповсюдженість катетер-асоційованих інфекцій сечовивідних шляхів:
РКС = КК / ККД × 1000, де
РКС — розповсюдженість катетер-асоційованих інфекцій сечовивідних шляхів у відділенні на 1000 катетер-днів;
КК — кількість зареєстрованих катетер-асоційованих інфекцій сечовивідних шляхів у відділенні за період часу;
ККД — загальна кількість катетер-днів у відділенні за період часу — сума днів наявності встановленого катетера у пацієнтів, в яких не розвинулася катетер-асоційована інфекція сечовивідних шляхів та днів наявності встановленого катетера у пацієнтів до початку клінічних проявів катетер-асоційованої інфекції сечовивідних шляхів;
1000 — 1000 катетер-днів;
3) розповсюдженість вентилятор-асоційованих пневмоній:
РВ = КВ / ІД × 1000, де
РВ — розповсюдженість вентилятор-асоційованих пневмоній на 1000 днів інтубації;
КВ — кількість зареєстрованих вентилятор-асоційованих пневмоній за період часу;
ІД — загальна кількість днів інтубації за період часу — сума днів наявності встановленої інтубаційної/трахеостомічної трубки у пацієнтів, в яких не розвинулася вентилятор-асоційована пневмонія та днів наявності встановленої інтубаційної/ трахеостомічної трубки у пацієнтів до початку клінічних проявів вентилятор-асоційованої пневмонії;
1000 — 1000 днів інтубації.
10. Вибір додаткового набору даних для рутинного епіднагляду визначається планом дій з ПІІК (наприклад, якщо необхідні показники стратифіковані по факторам ризику, вибираються дані, які дозволять виділити відповідні групи ризику, або якщо фактори ризику невідомі, збираються дані про ті фактори, що підходять за літературними джерелами), який затверджується керівником ЗОЗ відповідно до Порядку впровадження профілактики інфекцій та інфекційного контролю в закладах охорони здоров’я, які надають медичну допомогу в стаціонарних умовах, затвердженого наказом Міністерства охорони здоров’я України від 03 серпня 2021 року № 1614.
11. Проведення рутинного епіднагляду включає використання показників трьох видів: інцидентність, превалентність і щільність інцидентності.
12. Дані про ІПНМД та АМР зберігаються ВІК протягом п’яти років.
13. Для порівняння показників щодо ІПНМД між різними групами пацієнтів в межах одного стаціонару чи між ЗОЗ або в різні часові періоди епідеміолог розраховує показники з урахуванням варіацій основних факторів ризику.
14. До факторів ризику належать внутрішні та зовнішні фактори ризику. Внутрішні — притаманні самому пацієнту (наприклад, характер і тяжкість основного захворювання або похилий вік) і дозволяють розрахувати окремі ризик-специфічні показники для порівняння між групами пацієнтів з подібними ризиками в різних ЗОЗ або в різні періоди часу. Зовнішні фактори — фактори, які пов’язані із конкретним персоналом (наприклад, дії певних медичних працівників) або з практикою догляду і лікування, що запроваджена на рівні ЗОЗ в цілому.
15. Дані рутинного епіднагляду є основою для прийняття в ЗОЗ всіх рішень щодо ПІІК. Висока якість даних забезпечується шляхом постійного і ретельного контролю отриманих даних.
16. Результати рутинного епіднагляду не підлягають звітуванню та використовуються ВІК для визначення ефективності впроваджених профілактичних заходів та їх корегування.
17. При забезпеченні зворотного зв’язку із керівниками ЗОЗ та клінічних структурних підрозділів, заборонено використовувати дані, які ідентифікують пацієнтів і медичних працівників.
III. Організація та проведення дозорного епідеміологічного нагляду за інфекційними хворобами, пов’язаними із наданням медичної допомоги
1. Дозорний епідеміологічний нагляд за ІПНМД здійснюється шляхом проведення дослідження з визначення ОРІПНМД та використання АМП, з метою:
1) оцінки на національному рівні загальної розповсюдженості ІПНМД та використання АМП у ЗОЗ, що надають цілодобову стаціонарну медичну допомогу;
2) визначення на національному рівні груп пацієнтів, інвазивних процедур, інфекцій (локалізацію, збудник, що викликав захворювання та наявність у нього маркерів резистентності до АМП) і призначених АМП (в тому числі комбінацію препаратів або комбінованих препаратів та показань до їх призначення);
3) корегування заходів профілактики направлених на попередження випадків ІПНМД та АМР;
4) розповсюдження результатів для підвищення обізнаності щодо проблеми, визначення загальних проблем та їх вирішення.
2. Дозорний епідеміологічний нагляд за ІПНМД здійснюється закладом громадського здоров’я, на який покладено виконання функції дозорного епідеміологічного нагляду за ІПНМД у відповідній адміністративно-територіальній одиниці (далі — ЗГЗ) та ВІК ЗОЗ, в якому проводиться визначення ОРІПНМД.
3. Визначення ОРІПНМД та використання АМП здійснюється шляхом збору та аналізу таких даних:
1) ЗОЗ в цілому:
загальне число ліжок в ЗОЗ;
число ліжок, що виділені для надання цілодобової медичної допомоги;
число ліжок у ВАРІТ;
власність ЗОЗ (приватна, державна, комунальна);
число поступлень пацієнтів на рік;
число проведених ліжкоднів пацієнтами на рік;
кількість використаного спиртовмісного антисептика на рік в літрах;
число проведених оцінок дотримання правил гігієни рук в ЗОЗ згідно з Інструкцією з впровадження покращення гігієни рук в закладах охорони здоров’я та установах / закладах надання соціальних послуг / соціального захисту населення, затвердженої наказом Міністерства охорони здоров’я України від 03 серпня 2021 року № 1614 (далі — Інструкція);
число проведених посівів крові на рік;
число проведених досліджень калу на виявлення токсинів Clostridium difficile на рік;
кількість сестер медичних, які входять до складу ВІК;
кількість лікарів, які входять до складу ВІК;
кількість клінічних провізорів, які входять до складу ВІК;
кількість сестер медичних в ЗОЗ;
кількість молодших медичних сестер в ЗОЗ;
кількість сестер медичних у ВАРІТ;
кількість молодших медичних сестер у ВАРІТ;
число палат для ізоляції пацієнтів з інфекційними хворобами з аерогенним шляхом інфікування;
затверджені керівником ЗОЗ СОП, у тому числі щодо антимікробної терапії;
число ліжок (точок догляду) з диспенсерами із спиртовмісним антисептиком для рук;
число ліжок (точок догляду), які повинні мати диспенсери із спиртовмісним антисептиком для рук відповідно до оцінки інфраструктури і ресурсів для гігієни рук в ЗОЗ, проведеної згідно з Інструкцією;
число палат/кімнат пацієнтів в ЗОЗ;
число одномісних палат/кімнат пацієнтів в ЗОЗ;
число палат/кімнат пацієнтів в ЗОЗ, що оснащені ванною кімнатою;
2) клінічного структурного підрозділу ЗОЗ:
спеціалізація клінічного структурного підрозділу ЗОЗ;
спеціалізація лікарів клінічного структурного підрозділу ЗОЗ;
наявність процедури перевірки доцільності застосування АМП протягом 72 годин після першого призначення;
число проведених ліжкоднів пацієнтами на рік;
кількість використаного спиртовмісного антисептика на рік в літрах;
загальна кількість ліжок в клінічному структурному підрозділі ЗОЗ;
число ліжок (точок догляду) з диспенсерами із спиртовмісним антисептиком для рук;
число ліжок (точок догляду), які повинні мати диспенсери із спиртовмісним антисептиком для рук відповідно до оцінки інфраструктури і ресурсів для гігієни рук в ЗОЗ, проведеної згідно з Інструкцією;
кількість медичних працівників у клінічному структурному підрозділі ЗОЗ;
число палат/кімнат пацієнтів в клінічному структурному підрозділі ЗОЗ;
число одномісних палат/кімнат пацієнтів в клінічному структурному підрозділі ЗОЗ;
число одномісних палат/кімнат пацієнтів в клінічному структурному підрозділі ЗОЗ, що оснащені ванною кімнатою;
3) щодо пацієнта ЗОЗ:
спеціалізація лікуючого лікаря;
проведення оперативних втручань;
вага при народженні (для дітей у віці до одного місяця);
встановлення інвазивних медичних пристроїв (центральний та периферичний судинні катетери, сечовий катетер, інтубаційні трубки, дренажі тощо);
дані щодо антимікробної терапії і профілактики;
дані щодо ІПНМД;
4) на національному рівні:
число ЗОЗ загалом та ЗОЗ, які прийняли участь у дослідженні;
число ліжок в ЗОЗ загалом та в ЗОЗ, які прийняли участь у дослідженні;
число відділень в ЗОЗ загалом та в ЗОЗ, які прийняли участь у дослідженні;
число проведених ліжкоднів в ЗОЗ загалом та в ЗОЗ, які прийняли участь у дослідженні;
методика відбору ЗОЗ для дослідження.
4. ЗОЗ, що включаються в дослідження, визначаються Державною установою «Центр громадського здоров’я Міністерства охорони здоров’я України» (далі — Центр) методом стратифікованої вибірки і затверджуються наказом Міністерства охорони здоров’я України.
5. Критерії включення ЗОЗ у дослідження:
1) надає цілодобову стаціонарну медичну допомогу;
2) мінімальні критерії відсутні (не враховується кількість ліжок, забезпеченість кадрами, профіль ЗОЗ тощо);
3) група ЗОЗ, що знаходиться в одному підпорядкуванні, але розмежовані географічно, вважаються одним ЗОЗ;
4) ЗОЗ не може бути включений в дослідження частіше ніж раз на п’ять років.
6. Центр затверджує та передає у відповідні ЗГЗ не пізніше 01 березня дослідного року список ЗОЗ для дозорного епіднагляду за ІПНМД і терміни проведення дослідження.
7. Терміни проведення дослідження в ЗОЗ визначаються з урахуванням наступного:
1) дані збираються в одній палаті або відділенні за один день;
2) загальний термін проведення дослідження не повинен перевищувати чотирьох тижнів;
3) у випадку, якщо в ЗОЗ існує практика планування госпіталізацій, заборонено проводити дослідження в день планової госпіталізації або в день після планової виписки.
8. Збір даних для дослідження проводиться ЗГЗ відповідно до графіку затвердженого Центром. З метою валідації даних у дослідженні можуть приймати участь представники Центру.
9. Представники ЗГЗ (працівник, який проводить дослідження визначення ОРІПНМД і працівник, який вносить дані) та представник(и) ВІК ЗОЗ, в якому проводиться визначення ОРІПНМД, мають пройти навчання і підготовку щодо збору даних та перевірки правильності цих даних. Навчання і підготовку проводить Центр.
10. Після перевірки даних представник ЗГЗ (наприклад, статистик або менеджер даних) у термін не пізніше 30 вересня дослідного року вносить дані щодо визначення ОРІПНМД до HelicsWin.Net, а паперові форми надсилає до Центру.
11. При аналізі даних, формуванні та представленні звіту щодо проведеного дослідження Центру заборонено використовувати ідентифікаційні дані ЗОЗ та пацієнтів.
12. Після перевірки та аналізу даних Центр формує звіт щодо проведеного визначення ОРІПНМД і у термін не пізніше 30 грудня дослідного року надсилає його до Міністерства охорони здоров’я України.
Генеральний директор Директорату громадського здоров’я
та профілактики захворюваності
І. Руденко
Додаток 1
до Порядку здійснення епідеміологічного нагляду
та ведення обліку інфекційних хвороб,
пов’язаних з наданням медичної допомоги
(підпункт 1 пункту 6 розділу II, пункт 7 розділу II)
Форма збору даних щодо катетер-асоційованих інфекцій кровотоку (катетеризація периферичної вени)
I |
Прізвище, ім’я та по батькові (за наявності) пацієнта, якому встановлено периферичний венозний катетер: |
Вік: __ |
№ медичної карти2: _____ Відділення: ________ |
Дата опрацювання4: ___ / ___ / __ Прізвище, ім’я та по батькові (за наявності) епідеміолога: ___________ |
Діагноз1: |
Стать: |__| Ч |__| Ж |
Дослідний номер3: _____ |
||
I |
Дата постановки: ___ / ___ / __ р. Дата зняття: ___ / ___ / ____ р. Прізвище, ім’я та по батькові (за наявності) м/с5: .................................. |
|||
II |
Клас ASA15: Вага16: ........... кг |
|||
Нагляд17, дні |
||||||||
III |
1 |
2 |
3 |
4 |
5 |
6 |
7 |
Наступний після зняття |
Ступінь запалення: |
Ступінь запалення: |
Ступінь запалення: |
Ступінь запалення: |
Ступінь запалення: |
Ступінь запалення: |
Ступінь запалення: |
Ступінь запалення: |
|
Догляд18, день |
|||||||
IV |
1 |
2 |
3 |
4 |
5 |
6 |
7 |
|__| оцінка необхідності подальшого використання |
|__| оцінка необхідності подальшого використання |
|__| оцінка необхідності подальшого використання |
|__| оцінка необхідності подальшого використання |
|__| оцінка необхідності подальшого використання |
|__| оцінка необхідності подальшого використання |
|__| оцінка необхідності подальшого використання |
|
Примітки. ________ 2 номер медичної карти стаціонарного хворого (форма первинної облікової документації № 003/о «Медична карта стаціонарного хворого № __», затверджена наказом Міністерства охорони здоров’я України від 14 лютого 2012 року № 110 (у редакції наказу Міністерства охорони здоров’я України від 21 січня 2016 року № 29), зареєстрована в Міністерстві юстиції України 12 лютого 2016 року за № 230/28360, форма первинної облікової документації № 097/о «Медична карта новонародженого № ____», затверджена наказом Міністерства охорони здоров’я України від 21 січня 2016 року № 29, зареєстрована в Міністерстві юстиції України 12 лютого 2016 року за № 233/28363, форма первинної облікової документації № 096/о «Історія вагітності та пологів № ___», затверджена наказом Міністерства охорони здоров’я України від 21 січня 2016 року № 29, зареєстрована в Міністерстві юстиції України 12 лютого 2016 року за № 232/28362), або у Реєстрі медичних записів, записів про направлення та рецептів в електронній системі охорони здоров’я) (далі — медична карта хворого). Номер медичної карти не переноситься до електронного інструменту (програмного забезпечення), який використовується ЗОЗ з метою збереження і аналізу даних рутинного епіднагляду (далі — електронний інструмент). 3 заповнюється при внесенні даних цієї форми до електронного інструменту та має відповідати номеру за порядком в ній. Рекомендовано зазначати номер з двох частин (наприклад, 24/21, де 24 — порядковий номер, 21 — поточний рік). 4 день, місяць та рік внесення даних з форми до електронного інструменту. 5 прізвище, ім’я та по батькові (за наявності) медичного працівника (медичної сестри або лікаря), який встановив периферичний катетер. 6 якщо катетер встановлюється вдруге і наступні рази. 7 зазначається виключно при повторному встановленні катетера. Підкреслюється «планово», якщо периферичний катетер замінюється в плановому порядку і про це є відповідний запис в медичній карті хворого або в листку лікарських призначень (форма первинної облікової документації № 003-4/о «Листок лікарських призначень», затверджена наказом Міністерства охорони здоров’я України від 29 травня 2013 року № 435, зареєстрована в Міністерстві юстиції України 17 червня 2013 року за № 990/23522) (далі — листок лікарських призначень). Підкреслюється «позапланово» у всіх випадках, які не відносяться до планової заміни периферичного катетера. 8 розмір катетера G, відповідно до специфікації у таблиці: |
Розмір, G |
Розмір, мм |
Об’єм рідини, що проходить за одиницю часу, мл/хв |
16 |
1,7 × 51 |
і 150 |
18 |
1,3 × 44 |
75–149 |
20 |
1,1 × 32 |
55–74 |
22 |
0,8 × 25 |
25–54 |
24 |
0,7 × 20 |
15–24 |
9 загальний об’єм інфузійних розчинів призначених на першу добу після встановлення периферичного катетера, які зазначені в листку лікарських призначень. 10 підкреслюється «не встановлено» або «встановлено», якщо під час використання периферичного катетера та протягом 48 годин після його видалення, лікарем-епідеміологом або лікуючим лікарем не встановлено або встановлено катетер-асоційовану інфекцію кровотоку, яка безпосередньо пов’язана з даним катетером. В разі підкреслення «встановлено» слід зазначається день, місяць і рік встановлення катетер-асоційованої інфекції кровотоку. 11 день, місяць і рік взяття крові для посіву на поживні середовища, на основі якого було встановлено катетер-асоційовану інфекцію кровотоку. 12 день, місяць і рік взяття спинномозкової рідини для посіву на поживні середовища, на основі якого було встановлено катетер-асоційовану інфекцію кровотоку. 13 день, місяць і рік взяття для посіву частини катетера, який безпосередньо знаходився у периферичній вені, якщо таке взяття проводилося. 14 кількість днів лікування катетер-асоційованої інфекції кровотоку від дати встановлення катетер-асоційованої інфекції кровотоку до дня закінчення лікування безпосередньо катетер-асоційованої інфекції кровотоку або смерті пацієнта. 15 клас ASA визначається на основі даних, які отримані на момент поточного поступлення пацієнта в ЗОЗ та зазначені в медичній карті хворого. 16 вага та зріст пацієнта необхідні для розрахунку його індексу маси тіла. 17 відзначається за результатами огляду пацієнта у відповідний день (відмітити можна лише один з наведених ступенів запалення). 18 відмітки проставляються в залежності від комплексу проведених заходів по догляду за периферичним венозним катетером, тобто відзначається декілька заходів в одній графі у відповідний день за інформацією, наявною в медичній карті хворого або в іншому документі, що визначає процедури догляду за периферичними венозними катетерами, затвердженому керівником закладу. 19 відмічається, якщо на пов’язці, якою покрито / зафіксовано периферичний венозний катетер, зазначена поточна дата на момент занесення відомостей в форму збору даних. Якщо процедуру заміни пов’язки проведено поза датою збору даних (наприклад, у неробочий день), помітка щодо проведення заміни пов’язки робиться в день отримання даних (ретроспективно). 20 відмічається, якщо в медичній карті хворого або в іншому документі, що визначає процедури догляду за периферичними венозними катетерами, затвердженому керівником закладу, при постановці катетера було зазначено дату планової заміни периферичного венозного катетера і таку заміну виконано в поточний день. Якщо процедуру планового видалення проведено поза датою збору даних (наприклад, у неробочий день), помітка щодо планового видалення катетера робиться в день отримання даних (ретроспективно). 21 відмічається, якщо в медичній карті хворого або в іншому документі, що визначає процедури догляду за периферичними венозними катетерами, затвердженому керівником закладу, при постановці катетера не було зазначено дату планової заміни периферичного венозного катетера і таку заміну виконано в поточний день. Якщо процедуру позапланового видалення проведено поза датою збору даних (наприклад, у неробочий день), помітка щодо позапланового видалення катетера робиться в день отримання даних (ретроспективно). 22 будь-які інші заходи з догляду за периферичним венозним катетером, які зазначені в медичній карті хворого, листку лікарських призначень або в іншому документі, що визначає процедури догляду за периферичними венозними катетерами, затвердженому керівником закладу, та відмітка щодо виконання яких на поточний день наявна. |
Додаток 2
до Порядку здійснення епідеміологічного нагляду
та ведення обліку інфекційних хвороб,
пов’язаних з наданням медичної допомоги
(підпункт 1 пункту 6 розділу II, пункт 7 розділу II)
Форма збору даних щодо катетер-асоційованих інфекцій кровотоку (катетеризація центральної судини)
I |
Прізвище, ім’я та по батькові (за наявності) пацієнта, якому встановлено центральний судинний катетер: |
Вік: __ років |
№ медичної карти2: ________ |
Дата опрацювання4: ___ / ___ / __ Прізвище, ім’я та по батькові (за наявності) епідеміолога: ___________________ |
Діагноз1: |
Стать: |__| Ч |__| Ж |
Дослідний номер3: ______ |
||
1 |
Дата постановки / зняття: ___ / ___ / ____ р. / ___ / ___ / ____ р. |
|||
2 |
Клас ASA21: Вага22: ............. кг |
|||
Нагляд23, дні |
||||||||||||||||||||||
3 |
1 |
2 |
3 |
4 |
5 |
6 |
7 |
8 |
9 |
10 |
11 |
12 |
13 |
14 |
15 |
16 |
17 |
18 |
19 |
20 |
21 |
Наступний після зняття |
СЗ: |
СЗ: |
СЗ: |
СЗ: |
СЗ: |
СЗ: |
СЗ: |
СЗ: |
СЗ: |
СЗ: |
СЗ: |
СЗ: |
СЗ: |
СЗ: |
СЗ: |
СЗ: |
СЗ: |
СЗ: |
СЗ: |
СЗ: |
СЗ: |
СЗ: |
|
Ступінь запалення (СЗ): 0 — біль і симптоматика відсутні I — біль / почервоніння в місці введення катетера II — біль, набряк, почервоніння, гнійні виділення в місці встановлення катетера III — біль, набряк, почервоніння, гнійні виділення в місці встановлення катетера, некроз тканин навколо катетера IV — біль, набряк, почервоніння, некроз тканин навколо катетера, гнійні виділення з катетера |
Догляд24, день |
|||||||
4 |
1 |
2 |
3 |
4 |
5 |
6 |
7 |
|__| оцінка необхідності подальшого використання |
|__| оцінка необхідності подальшого використання |
|__| оцінка необхідності подальшого використання |
|__| оцінка необхідності подальшого використання |
|__| оцінка необхідності подальшого використання |
|__| оцінка необхідності подальшого використання |
|__| оцінка необхідності подальшого використання |
|
8 |
9 |
10 |
11 |
12 |
13 |
14 |
|
|__| оцінка необхідності подальшого використання |
|__| оцінка необхідності подальшого використання |
|__| оцінка необхідності подальшого використання |
|__| оцінка необхідності подальшого використання |
|__| оцінка необхідності подальшого використання |
|__| оцінка необхідності подальшого використання |
|__| оцінка необхідності подальшого використання |
|
15 |
16 |
17 |
18 |
19 |
20 |
21 |
|
|__| оцінка необхідності подальшого використання |
|__| оцінка необхідності подальшого використання |
|__| оцінка необхідності подальшого використання |
|__| оцінка необхідності подальшого використання |
|__| оцінка необхідності подальшого використання |
|__| оцінка необхідності подальшого використання |
|__| оцінка необхідності подальшого використання |
|
Примітки. ________ 2 номер медичної карти стаціонарного хворого (форма первинної облікової документації № 003/о «Медична карта стаціонарного хворого № __», затверджена наказом Міністерства охорони здоров’я України від 14 лютого 2012 року № 110 (у редакції наказу Міністерства охорони здоров’я України від 21 січня 2016 року № 29), зареєстрована в Міністерстві юстиції України 12 лютого 2016 року за № 230/28360, форма первинної облікової документації № 097/о «Медична карта новонародженого № ____», затверджена наказом Міністерства охорони здоров’я України від 21 січня 2016 року № 29, зареєстрована в Міністерстві юстиції України 12 лютого 2016 року за № 233/28363, форма первинної облікової документації № 096/о «Історія вагітності та пологів № ___», затверджена наказом Міністерства охорони здоров’я України від 21 січня 2016 року № 29, зареєстрована в Міністерстві юстиції України 12 лютого 2016 року за № 232/28362), або у Реєстрі медичних записів, записів про направлення та рецептів в електронній системі охорони здоров’я) (далі — медична карта хворого). Номер медичної карти не переноситься до електронного інструменту (програмного забезпечення), який використовується ЗОЗ з метою збереження і аналізу даних рутинного епіднагляду (далі — електронний інструмент). 3 заповнюється при внесенні даних цієї форми до електронного інструменту та має відповідати номеру за порядком в ній. Рекомендовано зазначати номер з двох частин (наприклад, 5/22, де 5 — порядковий номер, 22 — поточний рік). 4 день, місяць та рік внесення даних з форми до електронного інструменту. 5 прізвище, ім’я та по батькові (за наявності) лікаря, який встановив центральний судинний катетер. 6 прізвище, ім’я та по батькові (за наявності) сестри медичної, яка асистувала при постановці центрального судинного катетера. 7 якщо катетер встановлюється вдруге і наступні рази. 8 зазначається виключно при повторному встановленні катетера. Підкреслюється «планово», якщо центральний судинний катетер замінюється в плановому порядку і про це є відповідний запис в медичній карті хворого або в листку лікарських призначень (форма первинної облікової документації № 003-4/о «Листок лікарських призначень», затверджена наказом Міністерства охорони здоров’я України від 29 травня 2013 року № 435, зареєстрована в Міністерстві юстиції України 17 червня 2013 року за № 990/23522) (далі — листок лікарських призначень). «Позапланово» підкреслюється у всіх випадках, які не відносяться до планової заміни центрального катетера. 9 може бути підкреслено декілька позицій: «діалізний» — встановлено центральний судинний катетер для проведення хронічного (планового) гемодіалізу; «тунельований» — встановлено центральний судинний катетер для проведення хронічного (планового) гемодіалізу з формуванням підшкірного тунелю; «нетунельований» — встановлено центральний судинний катетер для проведення хронічного (планового) гемодіалізу без формування підшкірного тунелю; «імплантований» — встановлено порт для тривалих внутрішньовенних інфузій; «неімплантований» — порт для тривалих внутрішньовенних інфузій не встановлено; «встановлений периферично центральний катетер» — катетер, призначений для катетеризації центральної судини, встановлено в периферичну судину; «інше» і зазначити тип катетера — встановлений катетер не відповідає вищезазначеним типам або має будь-які особливості конструкції. 10 кількість ліній центрального судинного катетера. 11 номер партії катетера, який зазначено безпосередньо на катетері. 12 відзначається яка судина катетеризована відповідно до запису в медичній карті хворого. 13 підкреслюється «права» або «ліва», якщо катетеризована судина анатомічно знаходиться в правій або лівій частині тіла; 14 підкреслюється відповідна причина постановки: «новий доступ» — у пацієнта на момент катетеризації центральної судини не було встановлено будь-яких інших центральних судинних катетерів. При наявності у пацієнта периферичного венозного катетера і відсутності центрального судинного катетера, центральна катетеризація судини визначається як «новий доступ»; «несправність» — у пацієнта було проведено заміну несправного катетера, відповідно до запису в медичній карті хворого, при цьому форма збору даних щодо заміненого центрального судинного катетера не заповнюється в динаміці (заповнюються лише архівні дані — наприклад, отриманий після зняття результат посіву); «планова заміна» — було проведено планову заміну катетера, відповідно до запису в медичній картці хворого. Плановою заміною не може вважатися: заміна катетера, який встановлено менше ніж за 14 діб до зняття; відомості щодо планової заміни якого зазначені в медичній карті хворого або в документі, що визначає процедури догляду за центральними судинними катетерами, затвердженому керівником закладу; якщо повторна катетеризація проведена без використання провідника; «аварійна заміна» — причина заміни не відповідає всім вищезазначеним причинам. 15 день, місяць та рік запланованої заміни центрального судинного катетера, відповідно до запису в медичній карті хворого або в документі, що визначає процедури догляду за центральними судинними катетерами, затвердженому керівником закладу. 16 підкреслюється «не встановлено» або «встановлено», якщо під час використання центрального судинного катетера та протягом 48 годин після його видалення, лікарем-епідеміологом або лікуючим лікарем не встановлено/встановлено катетер-асоційовану інфекцію кровотоку, яка безпосередньо пов’язана з даним катетером. В разі підкреслення «встановлено» зазначається день, місяць і рік встановлення катетер-асоційованої інфекції кровотоку. 17 день, місяць і рік взяття крові для посіву на поживні середовища, на основі якого було встановлено катетер-асоційовану інфекцію кровотоку. 18 день, місяць і рік взяття спинномозкової рідини для посіву на поживні середовища, на основі якого було встановлено катетер-асоційовану інфекцію кровотоку. 19 день, місяць і рік взяття для посіву частини катетера, який безпосередньо знаходився у периферичній вені, якщо таке взяття проводилося. 20 кількість днів лікування катетер-асоційованої інфекції кровотоку, від дати встановлення катетер-асоційованої інфекції кровотоку до дня закінчення лікування катетер-асоційованої інфекції кровотоку або смерті пацієнта. 21 клас ASA визначається на основі даних, які отримані на момент поточного поступлення пацієнта в ЗОЗ та зазначені в медичній карті хворого. 22 вага та зріст пацієнта необхідні для розрахунку індексу маси тіла пацієнта. 23 відзначається за результатами огляду пацієнта у відповідний день (відмітити можна лише один з наведених ступенів запалення). 24 відмітки проставляються в залежності від комплексу проведених заходів по догляду за центральним судинним катетером у відповідний день, тобто відзначається декілька заходів в одній графі за інформацією, наявною в медичній карті хворого або в іншому документі, що визначає процедури догляду за центральними судинними катетерами, затвердженому керівником закладу. 25 відмічається, якщо на пов’язці, якою покрито/зафіксовано центральний судинний катетер, зазначена поточна дата на момент занесення відомостей в форму збору даних. Якщо процедуру заміни пов’язки проведено поза датою збору даних (наприклад, у неробочий день), помітка щодо заміни пов’язки робиться в день отримання даних (ретроспективно). 26 відмічається, якщо в медичній карті хворого, листку лікарських призначень або в іншому документі, що визначає процедури догляду за центральними судинними катетерами, затвердженому керівником закладу, зазначено проведення процедури «антимікробний/антибіотиковий замок». Якщо процедуру «антимікробний/антибіотиковий замок» проведено поза датою збору даних (наприклад, у неробочий день), помітка щодо її проведення робиться в день отримання даних (ретроспективно). 27 відмічається, якщо в медичній карті хворого, листку лікарських призначень або в іншому документі, що визначає процедури догляду за центральними судинними катетерами, затвердженому керівником закладу, зазначено накладання пов’язки з хлоргексидином і на пов’язці, якою покрито/зафіксовано центральний судинний катетер, зазначена поточна дата на момент занесення відомостей в форму збору даних. Якщо процедуру накладання пов’язки з хлоргексидином проведено поза датою збору даних (наприклад, у неробочий день), помітка щодо її проведення робиться в день отримання даних (ретроспективно). 28 відмічається, якщо в медичній карті хворого, листку лікарських призначень або в іншому документі, що визначає процедури догляду за центральними судинними катетерами, затвердженому керівником закладу, зазначено накладання антимікробної мазі на місце встановлення центрального судинного катетера і на пов’язці, якою покрито/зафіксовано центральний судинний катетер, зазначена поточна дата на момент занесення відомостей в форму збору даних. Якщо антимікробну мазь було накладено поза датою збору даних (наприклад, у неробочий день), помітка щодо її накладання робиться в день отримання даних (ретроспективно). 29 відмічається, якщо в медичній карті хворого або в іншому документі, що визначає процедури догляду за центральними судинними катетерами, затвердженому керівником закладу, при постановці катетера було зазначено дату планової заміни центрального судинного катетера і таку заміну виконано в поточний день. Якщо процедуру планового видалення проведено поза датою збору даних (наприклад, у неробочий день), помітка щодо планового видалення катетера робиться в день отримання даних (ретроспективно). 30 відмічається, якщо в медичній карті хворого або в іншому документі, що визначає процедури догляду за центральними судинними катетерами, затвердженому керівником закладу, при постановці катетера не було зазначено дату планової заміни периферичного венозного катетеру і таку заміну виконано в поточний день. Якщо процедуру позапланового видалення проведено поза датою збору даних (наприклад, у неробочий день), помітка щодо позапланового видалення катетера робиться в день отримання даних (ретроспективно). 31 будь-які інші заходи з догляду за центральним судинним катетером, які зазначені в медичній карті хворого, листку лікарських призначень або в іншому документі, що визначає процедури догляду за центральними судинними катетерами, затвердженому керівником закладу, та відмітка щодо виконання яких на поточний день наявна. |
Додаток 3
до Порядку здійснення епідеміологічного нагляду
та ведення обліку інфекційних хвороб,
пов’язаних з наданням медичної допомоги
(підпункт 2 пункту 6 розділу II, пункт 7 розділу II)
Форма збору даних щодо катетер-асоційованих інфекцій сечовивідних шляхів
I |
Прізвище, власне ім'я та по батькові (за наявності) пацієнта, якому встановлено сечовий катетер |
Вік: __ |
№ медичної карти2: _______ |
Дата опрацювання4: ___ / ___ / __ Прізвище, ім’я та по батькові (за наявності) епідеміолога5: _____________________ |
Діагноз1: |
Стать: |__| Ч |__| Ж |
Дослідний номер3: _____ |
||
1 |
Дата постановки: ___ / ___ / ____ р. Дата зняття: ___ / ___ / ____ р. |
|||
2 |
Клас ASA18: Вага19: .............. кг |
|||
Нагляд, дні20 |
||||||||||||||||||||||
3 |
1 |
2 |
3 |
4 |
5 |
6 |
7 |
8 |
9 |
10 |
11 |
12 |
13 |
14 |
15 |
16 |
17 |
18 |
19 |
20 |
21 |
Наступний після зняття |
СЗ: |
СЗ: |
СЗ: |
СЗ: |
СЗ: |
СЗ: |
СЗ: |
СЗ: |
СЗ: |
СЗ: |
СЗ: |
СЗ: |
СЗ: |
СЗ: |
СЗ: |
СЗ: |
СЗ: |
СЗ: |
СЗ: |
СЗ: |
СЗ: |
СЗ: |
|
Ступінь запалення (СЗ): |__| 0 — біль і симптоматика відсутні |__| I — біль/ дискомфорт в місці введення катетера |__| II — біль/ набряк/ почервоніння в місці введення катетера, зміна кольору сечі |__| III — біль/ набряк/ почервоніння/ некроз в місці введення катетера, гнійні/ кров’янисті домішки в сечі |
Догляд, день21 |
|||||||
4 |
1 |
2 |
3 |
4 |
5 |
6 |
7 |
|__| оцінка необхідності подальшого використання |
|__| оцінка необхідності подальшого використання |
|__| оцінка необхідності подальшого використання |
|__| оцінка необхідності подальшого використання |
|__| оцінка необхідності подальшого використання |
|__| оцінка необхідності подальшого використання |
|__| оцінка необхідності подальшого використання |
|
Догляд, день21 |
|||||||
4 |
8 |
9 |
10 |
11 |
12 |
13 |
14 |
|__| оцінка необхідності подальшого використання |
|__| оцінка необхідності подальшого використання |
|__| оцінка необхідності подальшого використання |
|__| оцінка необхідності подальшого використання |
|__| оцінка необхідності подальшого використання |
|__| оцінка необхідності подальшого використання |
|__| оцінка необхідності подальшого використання |
|
15 |
16 |
17 |
18 |
19 |
20 |
21 |
|
|__| оцінка необхідності подальшого використання |
|__| оцінка необхідності подальшого використання |
|__| оцінка необхідності подальшого використання |
|__| оцінка необхідності подальшого використання |
|__| оцінка необхідності подальшого використання |
|__| оцінка необхідності подальшого використання |
|__| оцінка необхідності подальшого використання |
|
Примітки. 1 основний клінічний діагноз пацієнта на момент катетеризації сечового міхура 2 номер медичної карти стаціонарного хворого (форма первинної облікової документації № 003/о «Медична карта стаціонарного хворого № __», затверджена наказом Міністерства охорони здоров’я України від 14 лютого 2012 року № 110 (у редакції наказу Міністерства охорони здоров’я України від 21 січня 2016 року № 29), зареєстрована в Міністерстві юстиції України 12 лютого 2016 року за № 230/28360, форма первинної облікової документації № 097/о «Медична карта новонародженого № ____», затверджена наказом Міністерства охорони здоров’я України від 21 січня 2016 року № 29, зареєстрована в Міністерстві юстиції України 12 лютого 2016 року за № 233/28363, форма первинної облікової документації № 096/о «Історія вагітності та пологів № ___», затверджена наказом Міністерства охорони здоров’я України від 21 січня 2016 року № 29, зареєстрована в Міністерстві юстиції України 12 лютого 2016 року за № 232/28362), або у Реєстрі медичних записів, записів про направлення та рецептів в електронній системі охорони здоров’я) (далі — медична карта хворого). Номер медичної карти не переноситься до електронного інструменту (програмного забезпечення), який використовується ЗОЗ з метою збереження і аналізу даних рутинного епіднагляду (далі — електронний інструмент). 3 заповнюється при внесенні даних спостереження до електронного інструменту та має відповідати номеру за порядком в ній. Рекомендовано зазначати номер з двох частин (наприклад, 100/22, де 100 — порядковий номер, 22 — поточний рік). 4 день, місяць та рік внесення даних з форми до електронного інструменту. 5 прізвище, ім’я та по батькові (за наявності) лікаря-епідеміолога ВІК, який відповідальний за збір, верифікацію та обробку даних щодо катетер-асоційованих інфекцій кровотоку в ЗОЗ. 6 прізвище, ім’я та по батькові (за наявності) медичного працівника (медичної сестри або лікаря), який встановив катетер. 7 якщо сечовий катетер встановлюється вперше протягом поточного перебування в ЗОЗ. 8 катетер встановлюється вдруге і наступні рази. 9 зазначається виключно при повторному встановленні катетера. Підкреслюється «планово», якщо сечовий катетер замінюється в плановому порядку і про це є відповідний запис в медичній карті хворого або в листку лікарських призначень (форма первинної облікової документації № 003-4/о «Листок лікарських призначень», затверджена наказом Міністерства охорони здоров’я України від 29 травня 2013 року № 435, зареєстрована в Міністерстві юстиції України 17 червня 2013 року за № 990/23522) (далі — листок лікарських призначень), «позапланово» — у всіх випадках, які не відносяться до планової заміни сечового катетера. 10 по типу Тиман (з жорстким вигнутим кінцем), Малекота — встановлено відповідну систему в цистостомі, пристосування Пеццера зазначається, як Малекота. Підкреслюється «Фолея», якщо встановлено сечовий катетер Фолея: двоходовий — двотрубна система, трьоходовий — тритрубна. 11 зазначається виключно, якщо у виді катетера підкреслено «Фолея». Вписується розмір, який вказано на сечовому катетері (наприклад, 14 F). 12 матеріал, з якого виготовлено катетер, відповідно до інструкції до сечового катетера. Може бути підкреслено декілька позицій. 13 підкреслюється лише одна (найбільш відповідна) позиція відповідно до медичної карти хворого. 14 підкреслюється лише одна позиція: «відкрита» — сечовий катетер не з’єднано герметично зі збиральним/дренажним мішком; «закрита» — сечовий катетер герметично з’єднано зі збиральним мішком; «з асептичним картриджем» — сечовий катетер з’єднано герметично зі збиральним/дренажним мішком та наявний асептичний картридж між сечовим катетером (сечовим міхуром) і збиральним/дренажним мішком; «інше» і зазначається тип та/або особливості дренажної системи, якщо жодна з вищеперерахованих позицій не підходить або не повністю описує дренажну систему. 15 підкреслюється «не встановлено» або «встановлено», якщо під час використання сечового катетера та протягом 7 днів після його видалення, лікарем-епідеміологом або лікуючим лікарем не встановлено/встановлено катетер-асоційовану інфекцію сечовивідних шляхів, яка безпосередньо пов’язана з даним катетером. В разі підкреслення «встановлено» зазначається день, місяць і рік встановлення катетер-асоційованої інфекції сечовивідних шляхів. 16 день, місяць і рік взяття сечі для посіву на поживні середовища, на основі якого було встановлено катетер-асоційовану інфекцію сечовивідних шляхів. 17 кількість днів лікування катетер-асоційованої інфекції сечовивідних шляхів від дати встановлення катетер-асоційованої інфекції сечовивідних шляхів до дня закінчення лікування катетер-асоційованої інфекції сечовивідних шляхів або смерті пацієнта. 18 клас ASA визначається на основі даних, які отримані на момент поточного поступлення пацієнта в ЗОЗ та зазначені в медичній карті хворого. 19 вага та зріст пацієнта використовуються для розрахунку його індексу маси тіла. 20 відзначається за результатами огляду пацієнта у відповідний день (відмітити можна лише один з наведених ступенів запалення). 21 відмітки проставляються в залежності від комплексу проведених заходів по догляду за сечовим катетером відповідно до медичної карти хворого або іншого документа, що визначає процедури догляду за сечовими катетерами, затвердженого керівником закладу, може відмічатися декілька пунктів в один день догляду. Якщо захід з догляду проведено поза датою збору даних (наприклад, у неробочий день), помітка щодо його проведення робиться в день отримання даних (ретроспективно). 22 відмічається, якщо в медичній карті хворого або в іншому документі, що визначає процедури догляду за сечовими катетерами, затвердженому керівником закладу, зазначено на дату збору даних проведення заміни збирального/дренажного мішка. Якщо заміна відбулася позапланово або поза датою збору даних (наприклад, у неробочий день), помітка щодо проведення заміни збирального/дренажного мішка робиться в день отримання даних (ретроспективно). 23 відмічається, якщо в медичній карті хворого або в іншому документі, що визначає процедури догляду за сечовими катетерами, затвердженому керівником закладу, при постановці катетера було зазначено дату планового видалення сечового катетера і таке видалення виконано в поточний день. Якщо видалення відбулося поза датою збору даних (наприклад, у неробочий день) помітка щодо проведення видалення катетера робиться в день отримання даних (ретроспективно). 24 відмічається, якщо в медичній карті хворого або в іншому документі, що визначає процедури догляду за сечовими катетерами, затвердженому керівником закладу, при постановці катетера не було зазначено дату планового видалення сечового катетера і таке видалення виконано в поточний день. Якщо видалення відбулося поза датою збору даних (наприклад, у неробочий день) помітка щодо проведення видалення катетера робиться в день отримання даних (ретроспективно). 25 будь-які інші заходи з догляду за сечовим катетером, які зазначені в медичній карті хворого, листку лікарських призначень або в іншому документі, що визначає процедури догляду за сечовими катетерами, затвердженому керівником закладу, та відмітка щодо виконання яких на поточний день наявна. |
Додаток 4
до Порядку здійснення епідеміологічного нагляду
та ведення обліку інфекційних хвороб,
пов’язаних з наданням медичної допомоги
(підпункт 3 пункту 6 розділу II, пункт 7 розділу II)
Форма збору даних щодо вентилятор-асоційованих пневмоній
I |
Прізвище, ім’я та по батькові (за наявності) пацієнта, якому проведено інтубацію з ШВЛ: |
Вік: __ років |
№ медичної карти1: _________ |
Дата опрацювання4: ___ / ___ / __ Прізвище, ім’я та по батькові (за наявності) епідеміолога: ______________________ |
Діагноз2: |
Стать: |__| Ч |__| Ж |
Дослідний номер3: ______ |
||
1 |
Дата інтубації/екстубації5: ___ / ___ / ____ р. / ___ / ___ / ____ р. |
|||
2 |
Клас ASA21: Вага22: .............. кг |
|||
Догляд23, день |
|||||||
3 |
1 |
2 |
3 |
4 |
5 |
6 |
7 |
|__| оцінка необхідності подальшої ШВЛ |
|__| оцінка необхідності подальшої ШВЛ |
|__| оцінка необхідності подальшої ШВЛ |
|__| оцінка необхідності подальшої ШВЛ |
|__| оцінка необхідності подальшої ШВЛ |
|__| оцінка необхідності подальшої ШВЛ |
|__| оцінка необхідності подальшої ШВЛ |
|
Догляд23, день |
|||||||
3 |
8 |
9 |
10 |
11 |
12 |
13 |
14 |
|__| оцінка необхідності подальшої ШВЛ |
|__| оцінка необхідності подальшої ШВЛ |
|__| оцінка необхідності подальшої ШВЛ |
|__| оцінка необхідності подальшої ШВЛ |
|__| оцінка необхідності подальшої ШВЛ |
|__| оцінка необхідності подальшої ШВЛ |
|__| оцінка необхідності подальшої ШВЛ |
|
15 |
16 |
17 |
18 |
19 |
20 |
21 |
|
|__| оцінка необхідності подальшої ШВЛ |
|__| оцінка необхідності подальшої ШВЛ |
|__| оцінка необхідності подальшої ШВЛ |
|__| оцінка необхідності подальшої ШВЛ |
|__| оцінка необхідності подальшої ШВЛ |
|__| оцінка необхідності подальшої ШВЛ |
|__| оцінка необхідності подальшої ШВЛ |
|
Примітки. 1. трахеостомія — хірургічне втручання, рутинний епідеміологічний нагляд за яким проводиться окремо. Якщо пацієнту замінено інтубаційну трубку на трахеостому, форма збору даних щодо вентилятор-асоційованих пневмоній продовжується, при цьому додатково заповнюється форма щодо збору даних за інфекцією області хірургічного втручання. 2. неінвазивна вентиляція легень не підпадає під збір даних щодо вентилятор-асоційованих пневмоній, оскільки при цьому відсутній комплекс чинників, які сприяють розвитку вентилятор-асоційованої пневмонії. ________ 2 основний клінічний діагноз пацієнта на момент інтубації з штучною вентиляцією легень. 3 заповнюється при внесенні інформації з цієї форми збору даних до електронного інструменту та має відповідати номеру за порядком в ній. Рекомендовано зазначати номер з двох частин (наприклад, 23/22, де 23 — порядковий номер, 22 — поточний рік). 4 день, місяць та рік внесення даних з форми до електронного інструменту. 5 день, місяць та рік інтубації з переходом на штучну вентиляцію легень і день, місяць та рік припинення штучної вентиляції легень з використанням інвазивних пристроїв, а саме: дата екстубації з наступною трахеостомією і продовженням штучної вентиляції легень не є датою екстубації; дата припинення штучної вентиляції легень з використанням трахеостоми є датою екстубації; дата припинення штучної вентиляції легень із залишенням трахеостоми (наприклад, трахеостомія при неоперабельних пухлинах гортані) є датою екстубації; дата екстубації з наступною неінвазивною штучною вентиляцією легень є датою екстубації; дата екстубації з наступною реінтубацією протягом наступних 48 годин не є датою екстубації і не потребує оформлення нової форми збору даних щодо вентилятор-асоційованих пневмоній; дата інтубації, яку було проведено протягом 48 годин після екстубації, не є датою інтубації і в даній формі зазначається в розділі «Догляд, дні», як «інше» із зазначенням «інтубація після екстубації протягом 48 годин». 6 прізвище, ім’я та по батькові (за наявності) лікаря, який встановив інтубаційну трубку (провів інтубацію), про що наявний запис в медичній картці хворого. 7 прізвище, ім’я та по батькові (за наявності) медичного працівника (сестри медичної), який асистував під час встановлення інтубаційної трубки (проведення інтубації). 8 діаметр інтубаційної трубки, який вказано в інструкції до виробу або в іншому супровідному документі та/або на видимій частині інтубаційної трубки, який залишився видимим після встановлення. 9 номер партії, який вказаний на інтубаційній трубці (заборонено визначати номер партії по упаковці, інструкції або інших супровідних документів до виробу). 10 підкреслюється «так», якщо в медичній карті хворого в протоколі інтубації (постановки інтубаційної трубки) зазначено, що інтубація була складною. Необхідно підкреслити «ні», якщо в медичній карті в протоколі інтубації (постановки інтубаційної трубки) зазначено, що інтубація була не складною або не зазначена складність проведення інтубації (постановки інтубаційної трубки). 11 підкреслити «перша», якщо інтубаційна/трахеостомічна трубка встановлюється вперше протягом поточного перебування в ЗОЗ, або «повторно», якщо інтубаційна/трахеостомічна трубка встановлюється другий і наступні рази із зазначенням дати (день, місяць та рік) першої інтубації/трахеостомії. 12 запланована дата екстубації/трахеостомії (день, місяць і рік), яка зазначена в медичній карті хворого, в листку лікарських призначень (форма № 003-4/о «Листок лікарських призначень), затверджена наказом Міністерства охорони здоров’я України від 29 травня 2013 року № 435, зареєстрована в Міністерстві юстиції України 17 червня 2013 року за № 990/23522) (далі — листок лікарських призначень) або в іншому документі, що визначає процедури догляду за пацієнтами, які знаходяться на штучній вентиляції легень, затвердженому керівником закладу. 13 може бути підкреслено декілька позиції: «звичайна», якщо жоден із наступних пунктів не характеризує тип інтубаційної трубки; «ультратонка поліуретанова», якщо в інструкції до інтубаційної трубки зазначено, що вона є ультратонкою та виготовлена з поліуретану; «вкрита сріблом», якщо в інструкції до інтубаційної трубки зазначено, що поверхня інтубаційної трубки імпрегнована сріблом; «вкрита АМП», якщо в інструкції до інтубаційної трубки зазначено, що поверхня інтубаційної трубки вкрита антимікробним(и) агентом(ами); «інше» і зазначається матеріал та/або покриття поверхні інтубаційної трубки, які вказані в інструкції виробника, але відсутні в наведених вище графах. 14 може бути підкреслено лише одну (найбільш відповідну) позицію: «з дренажним портом», якщо в інструкції до інтубаційної трубки зазначено, що інтубаційна трубка має манжету та дренажний порт; «наявна», якщо в інструкції до інтубаційної трубки зазначено, що інтубаційна трубка має манжету; «відсутня», якщо в інструкції до інтубаційної трубки зазначено, що інтубаційна трубка не має манжети; «інше» і зазначається характеристики манжети, які вказані в інструкції виробника, але відсутні в наведених вище графах. 15 заповнюється при внесенні даних спостереження до електронного інструменту та має відповідати дослідному номеру форми збору даних щодо інфекцій області хірургічного втручання (рутинний епідеміологічний нагляд за інфекційними ускладненнями після проведеної трахеостомії, відповідно до додатку 5 до цього Порядку). 16 підкреслюється «не встановлено» або «встановлено», якщо під час використання інтубаційної/трахеостомічної трубки та протягом 48 годин після її видалення, лікарем-епідеміологом або лікуючим лікарем не було встановлено або було встановлено вентилятор-асоційовану пневмонію, яка безпосередньо пов’язана з даною інтубаційною/трахеостомічною трубкою. В разі зазначення «встановлено» вказується день, місяць і рік встановлення вентилятор-асоційованої пневмонії. 17 день, місяць і рік взяття мокроти для посіву на поживні середовища, на основі якого було встановлено вентилятор-асоційовану пневмонію. 18 підкреслюється лише одна (найбільш відповідна) позиція. 19 день, місяць і рік взяття крові для посіву на поживні середовища, якщо даний посів проводився з метою підтвердження/встановлення сепсису, як ускладнення вентилятор-асоційованої пневмонії. 20 кількість днів лікування вентилятор-асоційованої пневмонії від дати встановлення вентилятор-асоційованої пневмонії до дня закінчення лікування безпосередньо вентилятор-асоційованої пневмонії або смерті пацієнта. 21 клас ASA визначається на основі даних, які отримані на момент поточного поступлення пацієнта в ЗОЗ та зазначені в медичній карті хворого. 22 вага та зріст пацієнта необхідні для розрахунку індексу маси тіла пацієнта. 23 відмітки проставляються в залежності від комплексу проведених заходів по догляду за пацієнтом у відповідний день, який знаходиться на штучній вентиляції легень, тобто відзначається декілька заходів в одній графі за інформацією, наявною в медичній карті хворого або в іншому документі, що визначає процедури догляду за пацієнтами, які знаходяться на штучній вентиляції легень, затвердженому керівником закладу. Якщо пацієнта повторно переведено на інвазивну штучну вентиляцію легень протягом 48 годин (наприклад, повторна інтубація після екстубації), проведені заходи по догляду в дні коли інвазивна штучна вентиляція не проводилася не відзначаються. Дні без інвазивної штучної вентиляції легень не повинні бути враховані при розрахунку епідеміологічних показників щодо вентилятор-асоційованих пневмоній (наприклад, показників розповсюдженості вентилятор-асоційованих пневмоній на кількість днів інтубації). 24 відмічається, якщо в медичній карті хворого або в іншому документі зазначено, що дихальний контур замінюється планово (наприклад, кожні 7 днів) і таку заміну виконано в поточний день. Якщо заміна відбулася поза датою збору даних (наприклад, у неробочий день) помітку щодо проведення заміни дихального контура необхідно зробити в день отримання даних (ретроспективно). 25 відмічається, якщо в медичній карті хворого або в іншому документі не зазначено, що дихальний контур замінюється планово і таку заміну виконано в поточний день. Якщо заміна відбулася поза датою збору даних (наприклад, у неробочий день) помітку щодо проведення заміни дихального контура необхідно зробити в день отримання даних (ретроспективно). 26 будь-які інші заходи з догляду за пацієнтом, який знаходиться на штучній вентиляції легень, що зазначені в медичній карті хворого, листку лікарських призначень або в іншому документі і відмітка щодо виконання яких на поточний день наявна. |
Додаток 5
до Порядку здійснення епідеміологічного нагляду
та ведення обліку інфекційних хвороб,
пов’язаних з наданням медичної допомоги
(підпункт 4 пункту 6 розділу II, пункт 7 розділу II)
Форма збору даних щодо інфекцій області хірургічного втручання
I |
Прізвище, ім’я та по батькові (за наявності) пацієнта: |
Вік: __ |
№ медичної карти1: ____ |
Дата заповнення4: Дата опрацювання5: |
Діагноз2: |
Стать: |__| Ч |__| Ж |
Дослідний номер3: _____ |
||
1 |
Назва операції6: ........................................................................................................................ |
|||
2 |
Індекси ризику |
Клас ASA9: Вага10: ............. кг |
||
3 |
Клас рани11: |
|||
4 |
Початок12: |
Невідкладність операції: |
||
Периопераційні заходи |
||
5 |
Підготовка пацієнта: |
Хірургічна підготовка шкіри: |
Передопераційна профілактика АМП14: |
Хірургічна обробка рук20: |
|
Дренаж/імплант |
||
Післяопераційна АМП-терапія: |
||
6 |
Інші заходи28 (описати): _________________________________________________________________ |
|
Занесено в базу даних: |__| так |__| ні Прізвище, ім’я та по батькові (за наявності) епідеміолога: ______________________ Примітки. ________ 2 основний клінічний діагноз пацієнта на момент проведення хірургічного втручання. У випадках якщо основний клінічний діагноз не є показанням до проведення оперативного втручання, необхідно зазначати два діагнози за наступною формою: основний клінічний діагноз / діагноз, який є причиною проведення оперативного втручання (наприклад, лімфобластний лейкоз / гострий апендицит). 3 дослідний номер заповнюється при внесенні даних цієї форми до електронного інструменту та має відповідати номеру за порядком в ній. Рекомендовано зазначати номер з двох частин (наприклад, 11/25, де 11 — порядковий номер, 25 — поточний рік). 4 день, місяць та рік внесення даних в форму збору даних. 5 день, місяць та рік внесення даних з форми до електронного інструменту. 6 назва оперативного втручання із списку, що наведений нижче (зазначається назва оперативного втручання, яке найбільше підходить): 1) видалення аневризми черевного відділу аорти; 2) ампутація кінцівки; 3) оперативне втручання на апендикулярному відростку; 4) постановка шунта для діалізу; 5) хірургія жовчних протоків, печінки і підшлункової залози; 6) хірургія молочної залози; 7) операції на серці; 8) каротидна ендартеректомія; 9) шунтування коронарних артерій із розрізом грудної клітини та донорської ділянки; 10) шунтування коронарної артерії із розрізом лише грудної клітини; 11) хірургія жовчного міхура; 12) хірургія товстого кишківника; 13) краніотомія; 14) кесарів розтин; 15) спонділодез; 16) відкрите лікування перелому; 17) хірургія шлунку; 18) хірургія кил; 19) артропластика кульшового суглобу; 20) пересадка серця; 21) абдомінальна гістеректомія; 22) артропластика колінного суглобу; 23) пересадка нирки; 24) ламінектомія; 25) пересадка печінки; 26) хірургія ділянки шиї; 27) хірургія нирок; 28) хірургія яєчників; 29) оперативні втручання пов’язані із встановленням та обслуговуванням кардіостимулятора; 30) хірургія простати; 31) периферичне судинне шунтування; 32) проктологія; 33) хірургія хребта; 34) хірургія тонкої кишки; 35) хірургія селезінки; 36) торакальна хірургія; 37) хірургія щитовидної та паращитовидної залоз; 38) вагінальна гістеректомія; 39) шунтування шлуночків головного мозку; 40) діагностична лапаротомія. У випадках якщо пацієнту проводиться одночасно декілька видів оперативних втручань (наприклад, при політравмі), оформляються форми збору даних відповідно до кількості хірургічних бригад. 7 прізвище, ім’я та по батькові (за наявності) лікаря-хірурга, який проводив оперативне втручання. У випадках якщо хірургічна бригада складається з більше ніж двох лікарів хірургів, в графі «Прізвище, ім’я та по батькові (за наявності) хірурга» зазначається Прізвище, ім’я та по батькові (за наявності) керівника хірургічної бригади. У випадках якщо оперативне втручання проводить декілька хірургічних бригад (наприклад, оперативні втручання при політравмі), заповнюються форми збору даних окремо по кожному з втручань. 8 прізвище, ім’я та по батькові (за наявності) лікаря-хірурга, який асистував під час проведення оперативного втручання. У випадках якщо хірургічна бригада складається з більше ніж двох лікарів хірургів в графі «Прізвище, ім’я та по батькові (за наявності) асистента» зазначається Прізвище, ім’я та по батькові (за наявності) заступника керівника хірургічної бригади. 9 клас ASA визначається на основі даних, які отримані на момент поточного поступлення пацієнта в ЗОЗ та зазначені в медичній карті хворого. 10 вага та зріст пацієнта використовуються для розрахунку індексу маси тіла пацієнта. 11 зазначається клас рани відповідно до ризику розвитку ІОХВ (розділ III Порядку профілактики інфекційних хвороб, пов’язаних із наданням медичної допомоги, в закладах охорони здоров’я, які надають медичну допомогу в стаціонарних умовах, затвердженого цим наказом). 12 день, місяць, рік, година та хвилина початку та закінчення оперативного втручання, які зазначено в медичній карті хворого, тривалість оперативного втручання в годинах і хвилинах. 13 Заповнення розділу 5 «Периопераційні заходи» проводиться відповідно до даних медичної карти хворого. 14 якщо передопераційна антибіотикопрофілактика показана і була проведена, ця графа не заповнюється. 15 вказати «недоступність», якщо антимікробного лікарського засобу не було в наявності. 16 інша причина вказується, якщо лікарський засіб був в наявності, але його не ввели пацієнту. 17 заповнюється виключно, якщо передопераційна антибіотикопрофілактика була проведена. Відмічається антибактеріальний лікарський засіб або їх комбінація, що були введені пацієнту з метою проведення передопераційної антибіотикопрофілактики: амоксицилін в поєднанні з клавулановою кислотою, цефазолін, клоксацилін, ванкоміцин, ципрофлоксацин, гентаміцин, метронідазол, пеніцилін; відмічається «інший» та зазначається діюча речовина або речовини антибактеріального(их) препарату(ів), що були введені пацієнту з метою проведення передопераційної антибактеріальної профілактики, якщо у наведеному списку відсутній використаний лікарський засіб. 18 доза антибактеріального препарату, який було введено пацієнту з метою проведення передопераційної антибіотикопрофілактики в міліграмах; в разі, якщо використовувалися два або більше лікарських засобів (діючих речовин), зазначаються дози всіх засобів через скісну риску. 19 заповнюється виключно, якщо антибактеріальний препарат вводився повторно протягом оперативного втручання з метою проведення антибіотикопрофілактики. Зазначається година і хвилина повторного введення антибактеріального(их) препарату(ів). 20 якщо хірургічна обробка рук не проводилася, ця графа не заповнюється. 21 якщо використовувався інший антисептичний засіб, який не зазначено в переліку, відмічається «інший антисептик» і вписується його назва або діюча речовина. 22 заповнюється виключно, якщо хірургічна обробка рук проводилася. Вказується тривалість хірургічної обробки рук в хвилинах. 23 відмічається «так», якщо антибактеріальні препарати не вводилися пацієнту після накладання швів (закриття операційного поля) або «ні», якщо пацієнту продовжили вводити антибактеріальні препарати після закінчення оперативного втручання. 24 АМП 1 та АМП 2 — вказується діюча речовина антибактеріальних лікарських засобів, які були призначені пацієнту в післяопераційному періоді; у випадках, коли антибактеріальних препаратів призначено більше двох, в розділі 6 необхідно додати пункти АМП 3, АМП 4, АМП 5 і т. д. та вписати діючу речовину антибактеріального препарату, дозу введення, доз на день та днів призначення; якщо антибактеріальний лікарський засіб складається з двох діючих речовин (наприклад, амоксицилін в поєднанні з клавулановою кислотою), їх потрібно зазначати окремо: АМП 1 — амоксицилін, АМП 2 — клавуланова кислота, і подальші підпункти заповнювати відповідно до діючих речовин. 25 заповнюється виключно, якщо пацієнту продовжили вводити антибактеріальні препарати після закінчення оперативного втручання. Відмічається причина призначення антибактеріальних препаратів пацієнту відповідно до записів в медичній карті хворого: післяопераційна профілактика (відзначається виключно у випадках, коли післяопераційна профілактика проводиться більш тривалий термін в разі трансплантації органів, кардіохірургічних втручань або ендопротезування суглобів), лікування ІОХВ, виділення з рани/дренажу; відмічається «інше» і вписується причина, якщо в наведеному переліку причина призначення антибактеріальної терапії відсутня. 26 локалізація розміщення дренажу/імпланту; якщо дренажів/імплантів декілька, їх необхідно зазначати окремо із зазначенням типу дренування, відомостей щодо призначення АМП і виду імпланту в «інших заходах» (пункт 6 форми). 27 відмітити «інше» і вписати вид/тип імпланту, якщо в наведеному переліку він відсутній. 28 в цьому розділі зазначаються заходи, які важливі з точки зору епідеміологічного нагляду за ІОХВ, але які не увійшли до інших розділів цієї форми збору даних. Крім того, в даний розділ слід вносити дані, які не вмістилися у відповідний розділ форми (наприклад, призначені антибактеріальні засоби та вид імпланту). |
Додаток 6
до Порядку здійснення епідеміологічного нагляду
та ведення обліку інфекційних хвороб,
пов’язаних з наданням медичної допомоги
(підпункт 4 пункту 6 розділу II, пункт 7 розділу II)
Форма збору даних щодо інфекцій області хірургічного втручання в післяопераційний період
I |
Прізвище, ім’я та по батькові (за наявності) пацієнта: |
Вік: ....... років |
№ медичної карти: ......... |
Місце проживання: .......... |
Номер телефону пацієнта: ........................................................................................................ |
||||
Номер телефону контактної особи: ......................................................................................... Прізвище та ім’я контактної особи: ......................................................................................... |
||||
Дата поступлення: ...../...../.......... р. Дата виписки: ...../...../.......... р. |
День1 |
Дата |
Подія2 |
АМП3 |
Симптоми ІОХВ4 |
Прізвище, ім’я та по батькові (за наявності) лікуючого лікаря |
||||
1 |
ОВ |
||||||||
2–3 |
|||||||||
4–5 |
|||||||||
6–7 |
|||||||||
8–10 |
|||||||||
11–14 |
|||||||||
15–17 |
|||||||||
18–21 |
|||||||||
22–25 |
|||||||||
26–29 |
|||||||||
30 |
Кінець спостереження за ІОХВ (стандарт) |
||||||||
Інфекція області хірургічного втручання: |__| так |__| ні |
|||||||||
|__| Поверхнева ІОХВ |__| гнійні виділення із поверхневої післяопераційної рани або |__| ідентифіковано мікроорганізм із зразка, що взятий із рани5 або |__| післяопераційну рану розкрито повторно та |__| наявні симптоми гострого інфекційного захворювання або |__| лікуючий лікар встановив діагноз |
|__| Глибока ІОХВ |__| гнійні виділення із глибокої післяопераційної рани або |__| післяопераційну рану розкрито повторно та |__| ідентифіковано мікроорганізм із зразка, що взятий із рани5 або |__| наявні симптоми гострого інфекційного захворювання або |__| наявний глибокий запальний процес гнійного характеру, в тому числі абсцес візуально/пункційно/при повторному розтині |
|__| ІОХВ орган/порожнина |__| гнійні виділення по дренажу, який встановлений в порожнину/орган в нормі не колонізований мікроорганізмами або |__| при обстеженні (візуалізації) знайдено запальний процес або абсцес в органі/порожнині, що дотичні до оперативного втручання |__| ідентифіковано мікроорганізм із зразка, що взятий із органа/ порожнини5 |
|||||||
Інші післяопераційні ускладнення: |
|||||||||
Результати бактеріологічного обстеження* |
Зразок взято Дата: .../.../..... |
Ідентифікований мікроорганізм(и): 1. |
Чутливість до АМП: 1. |
||||||
Дата заповнення форми: ..../..../....... р. Форма перевірена6: |__| так |__| ні Підпис: ............ Примітки: ________ 2 взаємодія із пацієнтом починаючи з оперативного втручання (ОВ): видалення/заміна пов’язки (ЗП), огляд лікуючим лікарем в стаціонарі (ОЛ), виписка із стаціонару (ВС), огляд лікуючим лікарем на дому або в амбулаторних умовах (ОД), опитування лікуючим лікарем по телефону (ОТ), повторне поступлення (ПП), повторне оперативне втручання (ПОВ), нагляд завершено (НЗ) із вказанням причини (наприклад, відмова від подальшого лікування або виписка під нагляд сімейного лікаря). 3 для кожної події зазначається дата призначення антимікробного препарату (АМП) та його назва (якщо антибіотик не призначається, необхідно зазначити «ні»). 4 зазначаються (при наявності) та відмічаються у відповідній графі (поверхнева/глибока ІОХВ або ІОХВ орган/порожнина): виділення по дренажу (гнійні, кров’янисті, зміна кольору з/на, тощо; біль/болісність в області рани, якщо це є непритаманним симптомом; локальний набряк, почервоніння шкіри, підвищена температура шкіри в області післяопераційної рани; будь-яке погіршення стану хворого як суб’єктивного так і об’єктивного характеру (наприклад, гіпертермія, загальне нездужання, зниження артеріального тиску, підвищення частоти серцевих скорочень тощо). 5 більшість післяопераційних ран швидко колонізуються мікроорганізмами, тому виділення збудника має діагностичну цінність лише при правильно взятому зразку для дослідження (матеріал набирається в асептичних умовах лише у пацієнтів, які мають симптоми ІОХВ). 6 форма перевіряється та підписується працівником ВІК, який відповідальний за рутинний епіднагляд ІОХВ або статистиком. |
ЗАТВЕРДЖЕНО
Наказ Міністерства охорони здоров’я України
03 серпня 2021 року № 1614
Зареєстровано
в Міністерстві юстиції України
11 жовтня 2021 р. за № 1319/36941
Порядок профілактики інфекційних хвороб, пов’язаних з наданням медичної допомоги, в закладах охорони здоров’я, які надають медичну допомогу в стаціонарних умовах
I. Загальні положення
1. Цей Порядок визначає організацію профілактики інфекційних хвороб, пов’язаних з наданням медичної допомоги (далі — ІПНМД) в закладах охорони здоров’я, що надають медичну допомогу в стаціонарних умовах (далі — ЗОЗ), незалежно від форми власності та незалежно від їх відомчого підпорядкування.
2. Виконання цього Порядку у ЗОЗ забезпечує його керівник, у клінічних структурних підрозділах — відділ з інфекційного контролю (далі — ВІК) та керівники структурних підрозділів.
3. У цьому Порядку терміни та умовні скорочення вживаються у такому значенні:
вентилятор-асоційована пневмонія (далі — ВАП) — група ІПНМД, що розвиваються у пацієнта в результаті інтубації та подальшої механічної вентиляції легень;
група ризику — соціальна група, стосовно якої є прямі епідеміологічні дані про те, що у її представників через певні об’єктивні чинники частіше за представників загального населення розвиваються захворювання або щодо якої є обґрунтовані припущення фахівців про високий рівень такого ризику;
інфекція області хірургічного втручання (далі — ІОХВ) — група ІПНМД, що розвиваються у пацієнта в результаті хірургічного втручання;
катетер-асоційовані інфекції кровотоку (далі — КАІК) — група ІПНМД, що розвиваються у пацієнта в результаті використання судинного катетера для введення лікарських засобів, забору проб крові або інших медичних процедур;
катетер-асоційовані інфекції сечовивідних шляхів (далі — КАІСВШ) — група ІПНМД, що розвиваються у пацієнта в результаті використання сечового катетера;
фактори ризику — це потенційно небезпечні для здоров’я фактори поведінкового, біологічного, генетичного, екологічного, соціального характеру, навколишнього та виробничого середовищ, що підвищують вірогідність розвитку захворювань, їх прогресування та несприятливого результату;
фоновий рівень ІПНМД — мінімальний рівень захворюваності на ІПНМД, який притаманний окремому ЗОЗ. Фоновий рівень ІПНМД установлюється на підставі рутинного епідеміологічного нагляду за ІПНМД протягом не менше 12 місяців та епідеміологічного аналізу;
АМП — антимікробний препарат;
ГРДС — гострий респіраторний дистрес-синдром;
НІВПТ — неінвазивна вентиляція легень із позитивним тиском;
ПІІК — профілактика інфекцій та інфекційний контроль;
СОП — стандартна операційна процедура;
ШВЛ — штучна вентиляція легень.
Інші терміни у цьому Порядку вживаються у значеннях, наведених в Законах України «Основи законодавства України про охорону здоров’я», «Про захист населення від інфекційних хвороб» та інших нормативно-правових актах у сфері охорони здоров’я.
4. Загальними адміністративними заходами, які забезпечуються ЗОЗ для профілактики ІПНМД є:
1) створення ВІК, відповідно до Положення про відділ з інфекційного контролю закладу охорони здоров’я та установи / закладу надання соціальних послуг / соціального захисту населення, затвердженого наказом Міністерства охорони здоров’я України від 03 серпня 2021 року № 1614;
2) затвердження плану дій з ПІІК;
3) наявний електронний інструмент (програмне забезпечення), який дозволяє визначати кількість днів використання катетеру (катетер-днів) для КАІК, КАІСВШ, відсоток днів ШВЛ, в які визначалася необхідність в подальшій інтубації, та розповсюдженість ІПНМД в ЗОЗ;
4) затвердження СОП з постановки та догляду за внутрішньосудинними катетерами, сечовими катетерами, інтубаційними та трахеостомічними трубками, профілактики ІОХВ;
5) проведення навчання, підготовки і перевірки знань щодо виконання СОП з постановки та догляду за внутрішньосудинними катетерами, сечовими катетерами, інтубаційними та трахеостомічними трубками, профілактики ІОХВ;
6) наявність у ЗОЗ мікробіологічної лабораторії або договору із мікробіологічною лабораторією, або іншим ЗОЗ, у якого є мікробіологічна лабораторія;
7) затвердження щорічного звіту ВІК з ПІІК.
5. Результатом приєднання КАІК, ВАП, ІОХВ, КАІСВШ є подовження строків перебування пацієнта в стаціонарі та збільшення витрат на його лікування.
6. Контроль за КАІК, ВАП, ІОХВ, КАІСВШ здійснюється шляхом проведення рутинного епідеміологічного нагляду відповідно до Порядку здійснення епідеміологічного нагляду та ведення обліку інфекційних хвороб, пов’язаних з наданням медичної допомоги, затвердженого наказом Міністерства охорони здоров’я України від 03 серпня 2021 року № 1614.
II. Профілактика катетер-асоційованих інфекцій кровотоку
1. Групи ризику щодо КАІК:
1) пацієнти відділень анестезіології, реанімації та інтенсивної терапії (далі — ВАРІТ) та палат інтенсивної терапії, що обумовлено частим введенням декількох катетерів, використанням катетерів, які встановлюються виключно пацієнтам ВАРІТ і пов’язані з високими ризиками (наприклад, катетеризація легеневої артерії), довготривалим використанням катетерів, а також фактом постановки катетерів у надзвичайних обставинах;
2) пацієнти, які знаходяться на постійному гемодіалізі;
3) пацієнти з онкологічними захворюваннями;
4) пацієнти після оперативних втручань.
2. Фактори ризику щодо КАІК:
1) довготривале перебування в стаціонарі до катетеризації;
2) довготривале або більше рекомендованого терміну використання катетера;
3) високий ступінь мікробної колонізації в місці введення катетера (наприклад, пахова ділянка);
4) катетеризація внутрішньої яремної вени;
5) катетеризація стегнової вени у дорослих;
6) нейтропенія;
7) недоношеність;
8) недоукомплектованість ВАРІТ сестрами медичними;
9) повне парентеральне харчування;
10) нестандартизований догляд за катетером (наприклад, працівники не пройшли підготовку щодо правильного догляду за катетером);
11) переливання препаратів крові у дітей.
3. До основних заходів щодо профілактики і моніторингу КАІК входять: загальні адміністративні заходи ЗОЗ, що наведені у пункті 5 розділу I цього Порядку, та спеціальні адміністративні заходи, які наведені у пункті 4 цього розділу, моніторинг, оцінка і зворотній зв’язок щодо КАІК, заходи перед постановкою катетера, заходи після встановлення катетера, додаткові заходи профілактики КАІК.
4. Спеціальні адміністративні заходи профілактики КАІК:
1) співвідношення сестер медичних до пацієнтів у ВАРІТ — щонайменше одна сестра медична на двох пацієнтів;
2) забезпечити ВАРІТ сестрами медичними, які працюють на повний робочий день (ВАРІТ — основне місце роботи);
3) вносити в щоденник форми первинної облікової документації № 003/о «Медична карта стаціонарного хворого № ____», затвердженої наказом Міністерства охорони здоров’я України від 14 лютого 2012 року № 110 (у редакції наказу Міністерства охорони здоров’я України від 21 січня 2016 року № 29), зареєстрованої в Міністерстві юстиції України 12 лютого 2016 року за № 230/28360, форми первинної облікової документації № 097/о «Медична карта новонародженого № ____», затвердженої наказом Міністерства охорони здоров’я України від 21 січня 2016 року № 29, зареєстрованої в Міністерстві юстиції України 12 лютого 2016 року за № 233/28363, форми первинної облікової документації № 096/о «Історія вагітності та пологів № ___», затвердженої наказом Міністерства охорони здоров’я України від 21 січня 2016 року № 29, зареєстрованої в Міністерстві юстиції України 12 лютого 2016 року за № 232/28362), або до Реєстру медичних записів, записів про направлення та рецептів в електронній системі охорони здоров’я (далі — медична карта стаціонарного хворого) наступні дані:
покази для введення катетера;
дата і час введення катетера;
медичний працівник, який провів процедуру;
дата і час видалення катетера.
5. Моніторинг, оцінка і зворотній зв’язок щодо КАІК:
1) вимірювати частоту розвитку КАІК на 1000 катетер-днів в кожному із відділень окремо для центральних судинних катетерів;
2) вимірювати частоту розвитку КАІК на 1000 катетер-днів у ВАРІТ для периферичних катетерів;
3) порівнювати результати за квартал, півроку та рік і співставляти їх із регіональними або загальнонаціональними даними;
4) мінімум раз на рік, під час навчальних сесій, повідомляти отримані результати медичним працівникам та, під час затвердження щорічного звіту ВІК з ПІІК, керівництву ЗОЗ.
6. Заходи перед постановкою катетера:
1) щоденна обробка шкіри пацієнтів ВАРІТ (всього тіла) 2% розчином хлоргексидину, окрім дітей віком до двох місяців, у яких необхідно використовувати 70% розчин спирту;
2) гігієнічна обробка рук перед одяганням рукавичок відповідно до додатку 1 до Інструкції з впровадження покращення гігієни рук в закладах охорони здоров’я та установах / закладах надання соціальних послуг / соціального захисту населення, затвердженої наказом Міністерства охорони здоров’я України від 03 серпня 2021 року № 1614 (далі — Інструкція).
7. Заходи під час постановки катетера:
1) використання СОП із контрольним списком послідовності дій для постановки катетера, примірну СОП «Контрольний список послідовності дій для постановки центрального судинного катетера» наведено у додатку 1 до цього Порядку;
2) виконання процедури виключно у асептичних умовах;
3) використовуйте переносний маніпуляційний столик або набір для постановки/заміни центрального судинного катетера, що містять все необхідне для асептичної постановки/заміни (перелік слід зазначити у відповідному СОП), і легко доступні у відділеннях, де проводиться катетеризація центральних судин;
4) для забезпечення асептики під час постановки/заміни по провіднику центрального судинного катетера медичні працівники, які приймають участь у постановці катетера, мають бути одягнені у стерильні одноразові халат і шапочку/хустинку захисні від інфекційних агентів, медичну (хірургічну) маску, захисні окуляри/щиток і медичні рукавички;
5) під час процедури встановлення центрального судинного катетеру пацієнт накривається стерильною серветкою, яка покриває все тіло;
6) використовувати хлоргексидиновий антисептик для підготовки шкіри перед процедурою (слід нанести на шкіру спиртовмісний антисептик із 2% хлоргексидином або 70% спиртом у дитини до двох місяців, який має висохнути до початку процедури);
7) не рекомендовано катетеризувати стегнову вену у дорослих пацієнтів із ожирінням;
8) не рекомендовано катетеризувати яремну вену у пацієнтів із встановленою трахеостомою;
9) використовувати периферичний судинний доступ з метою зниження ризиків розвитку ІПНМД недоцільно;
10) катетеризацію внутрішньої яремної вени слід проводити в супроводі ультразвукової візуалізації.
8. Заходи після встановлення катетера:
1) продезінфікувати закрутки, порти та безголкові сполучення перед початком маніпуляцій із катетером:
у разі відсутності видимого забруднення — протерти 70% спиртом або 2% розчином хлоргексидину або повідон-йодом;
у разі видимого забруднення — очистити зони забруднення шляхом механічного тертя, протягом мінімум п’яти секунд, із застосуванням 70% спирту або 2% розчину хлоргексидину або повідон-йоду;
під час очищення і дезінфекції катетера особливу увагу звернути на порти та розгалуження, оскільки ці ділянки найчастіше колонізовані мікроорганізмами в більшості випадків при стандартному застосуванні катетера;
2) видаляти катетер одразу після зникнення необхідності в ньому (наприклад, оцінювати необхідність катетера під час щоденного обходу);
3) рекомендовано надавати перевагу прозорим пов’язкам просякнутих хлоргексидином перед марлевими, окрім випадків коли наявні виділення із місця проколу, до їх зникнення;
4) замінювати прозорі пов’язки і виконувати догляд за ділянками шкіри із антисептиком, що містить хлоргексидин, кожні п’ять-сім днів або одразу, якщо пов’язка забруднена чи пошкоджена;
5) марлеві пов’язки змінювати кожні два дні або одразу, якщо пов’язка забруднена, волога чи пошкоджена;
6) пов’язки можна замінювати рідше, ніж вказано вище, у випадках, коли існує великий ризик зміщення центрального судинного катетера;
7) використовувати антимікробні мазі під час догляду за катетерами (в області проколу), що використовуються для проведення гемодіалізу (повідон-йодову або поліспоринову мазь, у разі сумісності із матеріалом катетеру; заборонено використовувати мупіроцинову мазь через ризики формування резистентності та пошкодження поліуретанових катетерів).
9. Додаткові заходи з профілактики КАІК (використовуються лише у випадках високого рівня розповсюдженості КАІК в ЗОЗ, при умові, що всі заходи відповідно до пунктів 6–8 цього розділу запроваджені і дотримуються):
1) використання катетерів імпрегнованих антимікробними або антисептичними засобами (наприклад, міноциклін-рифампін або хлоргексидин-сульфадіазин срібла) у пацієнтів, які:
мають обмежений венозний доступ та рецидивуючу КАІК в анамнезі;
мають високий ризик ускладнень від КАІК (наприклад, після трансплантації серцевого клапану);
2) використання просякнених хлоргексидином пов’язок у пацієнтів віком від двох місяців у ВАРІТ (додатково до щоденної обробки шкіри хлоргексидином).
III. Профілактика інфекцій області хірургічного втручання
1. Фактори ризику щодо ІОХВ:
1) колонізація бактеріями області хірургічного втручання (наприклад, при оперативних утручаннях на кишківнику або в ротоглотці ризик розвитку ІОХВ вищий ніж при операціях на кістках);
2) вірулентність мікроорганізмів (наприклад, кількість коагулазопозитивних стафілококів, що необхідна для розвитку ІОХВ, нижча ніж кількість коагулазонегативних стафілококів);
3) середовище рани (наприклад, наявність некротичних залишків тканин в області хірургічної рани збільшує ризик розвитку ІОХВ);
4) захисні механізми організму, що ослаблені при наявності наступних захворювань та станів:
цукровий діабет;
тютюнопаління;
гормональна терапія;
недоїдання;
довготривале перебування в стаціонарі до оперативного втручання;
колонізація носоглотки Staphylococcus aureus;
периопераційне переливання крові;
5) використання медичних виробів обмеженого використання, що пройшли очищення, дезінфекцію і стерилізацію (репроцесинг), а не одноразових;
6) багаторазове використання одноразових медичних виробів.
2. Класифікація ран у відповідності до ризику розвитку ІОХВ:
1) чисті — під час оперативного втручання відсутнє проникнення у колонізовану нормальною мікрофлорою частину тіла або порожнину при запланованих та контрольованих обставинах (ризик розвитку ІОХВ мінімальний і пов’язаний із мікроорганізмами зовнішнього середовища, операційної бригади або мікроорганізмами, що знаходяться на шкірі пацієнта);
2) чисті забруднені — під час оперативного втручання наявне проникнення у колонізовану нормальною мікрофлорою частину тіла або порожнину при запланованих та контрольованих обставинах (ризик розвитку ІОХВ незначний та може бути знижений шляхом профілактичних заходів);
3) забруднені — місце оперативного втручання сильно забруднене при відсутності вираженого запального процесу інфекційного характеру (ризик розвитку ІОХВ середній та лише незначно може бути знижений шляхом профілактичних підходів);
4) брудні — оперативне втручання проводиться в місці вираженого запального процесу інфекційного характеру (високий ризик розвитку ІОХВ).
3. Профілактика ІОХВ включає, але не обмежується ними, наступні заходи: парентеральна АМП-профілактика, непарентеральна АМП-профілактика, забезпечення нормотермії, контроль глікемії, оксигенація, антисептична профілактика.
4. Заходи парентеральної периопераційної антибіотикопрофілактики проводяться відповідно до медико-технологічних документів, затверджених Міністерством охорони здоров’я України.
5. Заходи непарентеральної АМП-профілактики:
1) наносити АМП (наприклад, мазі, розчини, порошки) на хірургічний розтин для профілактики ІОХВ не рекомендовано;
2) шовний матеріал покритий триклозаном може використовуватися з метою профілактики ІОХВ;
3) пов’язки просякненні АМП можуть використовуватися після первинного закриття рани з метою профілактики ІОХВ.
6. Контроль глікемії:
1) забезпечити периопераційний рівень глюкози в крові менше 9,9 ммоль/л у пацієнтів з діабетом та без нього;
2) контролювати рівень глікованого гемоглобіну не обов’язково в периопераційний період.
7. В периопераційний період у пацієнта необхідно забезпечити нормотермію.
8. Оксигентерапія:
1) пацієнтам із нормальною функцією легень, яким проводиться загальна анестезія з ендотрахеальною інтубацією, вентиляція легень здійснюється із підвищеною фракцією кисню, як під час операції так і після екстубації в ранній післяопераційний період;
2) інтраопераційне ведення пацієнтів, яким проводиться нейроаксіальна анестезія, із нормальною функцією легень використання подачі повітря через маску із підвищеною фракцією кисню може застосовуватися з метою зменшення ризику розвитку ІОХВ;
3) післяопераційне ведення пацієнтів із нормальною функцією легень із використанням подачі повітря через маску або носові канюлі із підвищеною фракцією кисню малоефективне для зменшення ризику розвитку ІОХВ.
9. Заходи антисептичної профілактики:
1) пацієнт повинен прийняти ванну або душ із використанням мила або з іншим антисептичним засобом мінімум на ніч перед операційним днем;
2) для прийому душу пацієнтам може бути рекомендовано використання мочалок із хлоргексидину-глюконатом для зменшення ризику розвитку ІОХВ;
3) інтраопераційну підготовку шкіри необхідно проводити спиртовмісним розчином, у разі відсутності протипоказань у пацієнта;
4) використання адгезивів з/без АМП не є обов’язковим для профілактики ІОХВ;
5) замочування протезів в антисептичних розчинах перед імплантацією не є обов’язковим для профілактики ІОХВ;
6) проведення антисептичної обробки шкіри безпосередньо перед закриттям рани не показано для профілактики ІОХВ;
7) уникати видалення волосся у місці запланованого розрізу, а в разі необхідності, обстригати тримером безпосередньо перед початком оперативного втручання в передопераційній.
10. Профілактика ІОХВ, які пов’язані із протезуванням суглобів:
1) утримуватися від переливання крові або її препаратів з метою профілактики ІОХВ заборонено;
2) системна імуносупресивна терапія:
використання системних кортикостероїдів та інших системних імуносупресивних препаратів з метою зменшення ризику розвитку ІОХВ не показано;
у пацієнтів, які отримують системні кортикостероїди або інші системні імуносупресори, не рекомендовано повторне введення АМП із профілактичною метою після закриття рани в операційній, навіть при наявності дренажу;
внутрішньосуглобова ін’єкція кортикостероїдів не показана з метою зменшення ризику розвитку ІОХВ.
11. Фоновий відсоток розвитку ІОХВ для різних класів ран повинен становити:
1) чисті рани — менше 2%;
2) чисті забруднені рани — менше 5%;
3) забруднені рани — менше 10%;
4) брудні рани — менше 20%;
5) протезування суглобів — менше 6%.
Перевищення фонового відсотку розвитку ІОХВ свідчить про наявність спалаху ІПНМД в ЗОЗ та необхідність проведення його розслідування і ліквідації відповідно до розділу VIII цього Порядку.
IV. Профілактика катетер-асоційованих інфекцій сечовивідних шляхів
1. Групи ризику щодо КАІСВШ:
1) пацієнти ВАРІТ та палат інтенсивної терапії;
2) пацієнти після оперативних втручань;
3) люди похилого віку;
4) пацієнти жіночої статі;
5) пацієнти з імуносупресивними станами.
2. Фактори ризику щодо КАІСВШ:
1) довготривале або більше рекомендованого терміну використання катетера;
2) недоукомплектованість ВАРІТ сестрами медичними;
3) нестандартизований догляд за катетером (наприклад, працівники не пройшли підготовку щодо правильного догляду за катетером).
3. До основних заходів профілактики і моніторингу КАІСВШ входять: належне використання катетеру, загальні адміністративні заходи ЗОЗ наведені у пункті 5 розділу I цього Порядку та спеціальні адміністративні заходи, наведені у пункті 5 цього розділу, заходи щодо постановки сечового катетеру, догляд за сечовим катетером, додаткові заходи профілактики КАІСВШ.
4. Належне використання катетеру:
1) встановлювати катетер лише при наявності показань, що наведені в додатку 2 до цього Порядку;
2) звести до мінімуму постановки сечових катетерів у пацієнтів із високим ризиком розвитку КАІСВШ (групи ризику наведені в пункті 1 цього розділу);
3) використання сечових катетерів у пацієнтів похилого віку з метою контролю нетримання сечі заборонено;
4) використовувати сечові катетери у операційних пацієнтів лише за показаннями;
5) у операційних пацієнтів, при встановленні сечового катетера за показаннями, видалити його одразу після зникнення необхідності в його використанні;
6) не рекомендовано використовувати рутинну катетеризацію сечового міхура у пацієнток в периопераційний період кесаревого розтину;
7) розглянути можливість використання альтернатив уретральній катетеризації у деяких груп пацієнтів:
рекомендовано використовувати зовнішні катетери у пацієнтів чоловічої статі без затримки сечі або блоку сечового міхура;
рекомендовано використовувати періодичну катетеризацію сечового міхура у пацієнтів із пошкодженням спинного мозку (нейрогенна затримка сечі);
рекомендовано використовувати періодичну катетеризацію у пацієнтів із дисфункцією сечового міхура;
з метою зниження ризику погіршення функції сечовивідних шляхів у дітей з мієломенінгоцеле та нейрогенним сечовим міхуром рекомендовано використовувати періодичну катетеризацію.
5. Спеціальні адміністративні заходи для профілактики КАІСВШ:
1) до постановки і обслуговування сечових катетерів допускаються виключно медичні працівники, які пройшли навчання і підготовку;
2) вносити в щоденник медичної карти стаціонарного хворого наступні дані:
покази для введення катетера;
дата і час введення катетера;
медичний працівник, який провів процедуру;
позначення про заходи по догляду;
щоденне позначення щодо необхідності подальшого використання;
позначення щодо негативних подій (наприклад, ненавмисне видалення, обструкція, пошкодження катетеру із подальшою заміною);
дата і час видалення катетера;
3) використовувати трьохходові (трьохпортові) катетери;
4) проводити моніторинг, оцінку і надавати зворотній зв’язок щодо КАІСВШ:
вимірювати частоту розвитку КАІСВШ на 1000 катетер-днів в кожному із відділень;
порівнювати результати за квартал, півроку та рік і співставляти їх із регіональними або загальнонаціональними даними;
мінімум раз на рік, під час проведення навчання і підготовки з ПІІК, повідомляти отримані результати медичним працівникам та, під час затвердження щорічного звіту ВІК з ПІІК, керівництву ЗОЗ.
6. Заходи щодо постановки сечового катетеру:
1) виконати практику гігієни рук безпосередньо перед та після постановки сечового катетера або будь-яких маніпуляцій із ним відповідно до додатку 1 до Інструкції;
2) під час постановки катетера використовувати асептичну техніку і стерильне обладнання:
для постановки сечового катетеру підготувати стерильні медичні рукавички, пелюшку, одноразову губку, антисептик (використовувати лише після перевірки переносимості) або стерильний фізіологічний розчин для периуретральної очистки та одноразовий пакет із змащувальною речовиною для введення;
використовувати антисептичні змащувальні речовини не рекомендовано;
3) після введення катетера надійно його закріпити аби попередити розтягнення уретри;
4) рекомендовано використовувати катетери із найменшим можливим діаметром задля запобігання травм шийки сечового міхура і уретри;
5) якщо використовується періодична катетеризація, проводити її через однакові проміжки часу з метою попередження надмірного розширення сечового міхура;
6) рекомендовано використовувати ультразвукову візуалізацію для оцінки кількості сечі в міхурі та уникнення непотрібних періодичних катетеризацій.
Примірну СОП щодо постановки сечового катетеру наведено в додатку 3 до цього Порядку.
7. Догляд за сечовим катетером:
1) після асептичного введення сечового катетера підтримувати дренажну систему закритою;
2) у випадках коли відбулося роз’єднання дренажної системи, замінити катетер використовуючи асептичну техніку;
3) рекомендовано використовувати системи сечового катетеру з попередньо герметично з’єднаними трубками;
4) не рекомендовано планово замінювати катетер;
5) слідкувати за тим аби безперервний і безперешкодний відтік сечі не порушувався;
6) збірний мішок має знаходитися нижче рівня сечового міхура;
7) збірний мішок заборонено класти на підлогу;
8) спорожнювати збірний мішок регулярно (не чекати до повного заповнення), використовуючи чистий контейнер, окремий для кожного пацієнта;
9) при спорожненні збірного мішка заборонено допускати торкання зливного патрубку із контейнером;
10) при спорожненні збірного мішка дотримуватися стандартних заходів захисту — використовувати медичні рукавички і халат/фартух захисний від інфекційних агентів при будь-яких маніпуляціях із катетером або системою збору;
11) складні сечові дренажні системи із використанням механізмів для зменшення проникнення мікроорганізмів (наприклад, із антисептичним картриджем в дренажному порті) не є необхідними в повсякденному використанні;
12) заміну постійних сечових катетерів та збірних мішків здійснювати лише за показаннями (наприклад, КАІСВШ, обструкція або порушення цілісності закритої системи);
13) системні АМП у пацієнтів із безсимптомною бактеріурією після видалення катетера (наприклад, бактеріурія у пацієнтів після урологічного оперативного втручання) призначати не рекомендовано;
14) не рекомендовано обробляти периуретральну зону антисептиками після встановлення катетера, звичайного миття з милом (наприклад, під час прийняття щоденної ванни або душу) достатньо;
15) у випадках відсутності ризику обструкції катетера промивання (іригація) сечового міхура не рекомендоване;
16) у разі ризику обструкції катетера (наприклад, внаслідок кровотечі в післяопераційний період при утручаннях на сечовому міхурі чи простаті) рекомендована планова закрита іригація сечового міхура;
17) у разі відсутності клінічних показань, для промивання сечового міхура не рекомендовано використовувати АМП;
18) заповнення збиральних мішків розчинами АМП або антисептиками не рекомендовано;
19) при видаленні сечового катетера заборонено перекривати відтік сечі;
20) при необхідності забору сечі на аналіз (клінічний чи мікробіологічний) забір проводити в асептичних умовах, а саме:
перед маніпуляцією провести практику гігієнічної обробки рук;
обробити порт для забору зразків антисептиком;
аспірувати сечу за допомогою шприца;
повторно обробити порт антисептиком;
при необхідності забору великої кількості сечі для аналізу (окрім посіву на флору та чутливість) зразок набирати із збирального мішка із дотриманням правил асептики;
21) лікуючому лікарю проводити щоденний огляд всіх пацієнтів із сечовими катетерами з метою визначення необхідності їх подальшого використання.
8. Додаткові заходи профілактики КАІСВШ (використовуються лише у випадках високого рівня розповсюдженості КАІСВШ в ЗОЗ, при умові, що всі заходи відповідно до пунктів 4, 6, 7 цього розділу запроваджені і дотримуються):
1) використовувати просякненні антимікробними або антисептичними речовинами катетери;
2) рекомендовано надавати перевагу катетерам, що виготовлені із гідрофільних речовин при періодичній катетеризації;
3) рекомендовано використовувати силіконові або вкриті силіконом катетери.
V. Профілактика вентилятор-асоційованих пневмоній
1. Пацієнти, які знаходяться на ШВЛ мають високий ризик розвитку ВАП, що за різними даними коливається в межах 5–20%.
2. Окрім ВАП, пацієнти на ШВЛ схильні до багатьох інших ускладнень — ГРДС, пневмоторакс, тромбоемболія легеневої артерії, лобарний ателектаз і набряк легень.
3. ВАП та інші ускладнення ШВЛ збільшують витрати на лікування та відсоток летальності.
4. Групи ризику щодо ВАП:
1) пацієнти ВАРІТ;
2) пацієнти з онкологічними захворюваннями.
5. Фактори ризику щодо ВАП:
1) довготривале перебування в стаціонарі до інтубації;
2) довготривала або більше рекомендованого терміну ШВЛ;
3) нейтропенія;
4) недоношеність;
5) недоукомплектованість ВАРІТ середніми медичними працівниками;
6) нестандартизований догляд за ендотрахеальною трубкою (наприклад, працівники не пройшли підготовку щодо правильного догляду).
6. До основних заходів щодо профілактики ВАП у дорослих належать: за можливості уникати інтубації, мінімізація седації, ранні фізичні навантаження і мобілізація, мінімізація накопичення виділень над манжетою ендотрахеальної трубки, положення хворого в ліжку, спеціальні підходи та додаткові заходи профілактики ВАП.
7. Уникати інтубації, якщо це можливо:
1) НІВПТ рекомендовано використовувати у пацієнтів із гострою гіперкапнічною (гіперкабнічною) або гіпоксичною дихальною недостатністю, які вторинні по відношенню до хронічного обструктивного захворювання легень або кардіогенної застійної серцевої недостатності;
2) не рекомендовано використовувати НІВПТ у пацієнтів із порушенням свідомості, гострим пошкодженням легень, ГРДС, тяжких гіпоксемії та ацидемії і при подовженні термінів НІВПТ для пацієнтів, у яких ядуха або газообмін не здатні швидко реагувати на НІВПТ (застосування НІВПТ в таких випадках лише відстрочує необхідну інтубацію).
8. Мінімізувати седацію:
1) за можливості, інтубованих пацієнтів слід вести без застосування седативних препаратів;
2) не рекомендовано використовувати протоколи і схеми ведення пацієнтів, які знаходяться на ШВЛ, із включенням бензодіазепінів;
3) у інтубованих пацієнтів рекомендовано застосовувати:
анальгетики при вираженому больовому синдромі;
заспокійливі та антипсихотичні засоби при збудженні;
керовану седацію з щоденною оцінкою рівню болю та глибини седації;
4) застосовувати щоденне спонтанне пробудження у пацієнтів, які не мають протипоказів, що дозволяє оцінити необхідність подальшої планової седації;
5) щоденно визначати готовність до екстубації (дослідження спонтанного дихання) у пацієнтів, які не мають протипоказів;
6) рекомендовано поєднувати спонтанне пробудження із визначенням готовності до екстубації у пацієнтів, які не мають протипоказів (пацієнти в свідомості з більшою вірогідністю пройдуть випробування спонтанного дихання, аніж седовані).
9. Ранні фізичні навантаження і мобілізація — розпочаті в найкоротші терміни фізичні навантаження і мобілізація при ШВЛ сприяють ранній екстубації, зменшують тривалість перебування у ВАРІТ та пришвидшують повернення пацієнта в звичний ритм життя.
10. Мінімізувати накопичення виділень над манжетою ендотрахеальної трубки:
1) з метою інтубації пацієнтів, яким ШВЛ може знадобитися більше 48 годин, рекомендовано використовувати ендотрахеальні трубки із дренажним портом для відсмоктування секрету, що накопичується в субглотковій (надманжетковій) ділянці;
2) не рекомендована екстубація з метою подальшої інтубації для розміщення трубки із дренажним портом.
11. Головний кінець ліжка має бути піднятий під кутом 30 — 45° у пацієнтів, які знаходяться на ШВЛ.
12. Дихальний/вентиляційний контур необхідно замінювати лише у випадках забруднення або при несправності (планова заміна не впливає на ризик розвитку ВАП).
13. Спеціальні підходи:
1) проводити щоденну гігієнічну обробку ротоглотки (механічна чистка зубів, обробка рота антисептиками, в тому числі хлоргексидином, санація ротової порожнини);
2) не рекомендовано використання місцевих АМП для недопущення колонізації ротоглотки через ризик розвитку захворювань, що викликані Clostridium difficile;
3) не рекомендовано використовувати пробіотики для зниження ризику ВАП;
4) заборонено використовувати пробіотики у інтубованих пацієнтів із захворюваннями імунної системи або інфекційними захворюваннями шлунково-кишкового тракту;
5) рекомендовано використовувати ендотрахеальні трубки з ультратонкими поліуретановими манжетами (низького тиску, високого об’єму);
6) рекомендовано вводити в трахею невелику кількість фізіологічного розчину перед санацією.
14. Додаткові заходи профілактики ВАП (використовуються лише у випадках високої частоти розповсюдженості ВАП у ЗОЗ, при умові, що всі заходи відповідно до пунктів 7 — 13 цього розділу запроваджені і дотримуються):
1) ендотрахеальні трубки із покриттям сріблом;
2) кінетичне ліжко.
15. Заходи, що не рекомендовані для профілактики ВАП:
1) профілактика виразки шлунку:
профілактика виразки шлунку не знижує ризик розвитку ВАП, оскільки, зменшує кислотність (збільшує рівень pH) шлункового вмісту;
у пацієнтів, які отримують ентеральне харчування, профілактика виразки шлунку може збільшити ризик розвитку ВАП;
профілактика виразки шлунку може бути призначена з причин, відмінних від профілактики розвитку ВАП;
2) рання трахеостомія;
3) раннє парентеральне харчування — початок парентерального харчування в перші 48 годин після поступлення у ВАРІТ пов’язано із високим ризиком розвитку ІПНМД, в тому числі ВАП;
4) закриті системи санації трахеї і бронхів у інтубованих пацієнтів.
16. До основних заходів щодо профілактики ВАП у новонароджених належать: за можливості уникнення інтубації, мінімізація механічної вентиляції, догляд за ротовою порожниною та спеціальні підходи.
17. Слід уникати інтубації новонароджених, якщо це можливо, шляхом, наприклад використання безперервної назальної НІВПТ, як альтернативу інтубації.
18. Мінімізувати тривалість механічної вентиляції у новонароджених:
1) за можливості, інтубованих новонароджених вести без застосування седативних препаратів;
2) щоденно оцінювати необхідність подальшої ШВЛ;
3) уникати незапланованих екстубацій із наступною інтубацією.
19. Рекомендовано регулярно доглядати за ротовою порожниною інтубованих новонароджених із використанням стерильного фізіологічного розчину.
20. У інтубованих новонароджених дихальний/вентиляційний контур слід заміняти лише у випадку забруднення або при несправності.
21. Рекомендовані спеціальні підходи для недоношених новонароджених:
1) розміщувати дитину у ліжку на боці;
2) розміщувати дитину на ліжку під кутом 45°;
3) використання закритих систем для санації трахеї і бронхів.
22. Заходи, що не рекомендовані для профілактики ВАП у новонароджених:
1) використовувати для санації ротової порожнини антисептики;
2) антагоністи Н2-гістамінових рецепторів — підвищують ризик розвитку ІПНМД, в тому числі ВАП;
3) антибіотики широкого спектру дії з профілактичною метою — підвищують ризик розвитку некротичного ентероколіту, збільшують терміни перебування у ВАРІТ та летальність/смертність.
23. Заходи, що заборонені у недоношених новонароджених:
1) переривати седацію з метою оцінки необхідності подальшої седації;
2) використовувати пробіотики і синбіотики.
24. До основних заходів щодо профілактики ВАП у дітей відносять: за можливості уникайте інтубації, мінімізація тривалості механічної вентиляції, гігієна ротової порожнини, розміщення в ліжку та догляд за апаратом ШВЛ.
25. Уникати інтубації дітей, якщо це можливо:
1) НІВПТ рекомендовано використовувати у дітей із гострою гіперкапнічною (гіперкарбічною) або гіпоксичною дихальною недостатністю, які вторинні по відношенню до хронічного обструктивного захворювання легень або кардіогенної застійної серцевої недостатності;
2) не рекомендовано використовувати НІВПТ у дітей із порушенням свідомості, гострим пошкодженням легень, ГРДС, тяжких гіпоксемії та ацидемії і при подовженні термінів НІВПТ для дітей, у яких ядуха або газообмін не здатні швидко реагувати на НІВПТ (застосування НІВПТ в таких випадках лише відстрочує необхідну інтубацію);
3) рекомендовано використовувати седацію під час проведення НІВПТ.
26. Мінімізувати тривалість механічної вентиляції у дітей:
1) щоденно оцінювати готовність до екстубації у дітей, які не мають протипоказів;
2) уникати незапланованих екстубацій із наступними інтубаціями.
27. Забезпечити регулярний догляд за порожниною рота дитини:
1) рекомендовано починати гігієну ротової порожнини через 2 — 3 дні після народження — після кожного годування протирати ясна марлевою серветкою з метою видалення нальоту та залишків їжі;
2) при прорізуванні зубів, чистити їх двічі на день зубною щіткою і водою;
3) фторвмісні зубні пасти рекомендовані після досягнення дитиною дворічного віку;
4) після проведення гігієнічних процедур порожнини рота, прополоскати її та санувати;
5) для підтримки слизової оболонки рота і губ в чистоті та зволоженими, рекомендовано використовувати губки змочені в безалкогольному і непероксидному ополіскувачі для порожнини рота.
28. Слід тримати піднятим головний кінець ліжка у інтубованих дітей.
29. Замінювати дихальні контури у інтубованих дітей необхідно лише при видимому забрудненні або несправності.
30. У інтубованих дітей рекомендовано регулярно видаляти конденсат із дихального контуру, уникаючи його потрапляння на пацієнта.
31. Перед зміною позиції тіла дитини на ліжку слід проводити санацію ротової порожнини.
32. У дітей з метою інтубації слід використовувати ендотрахеальні трубки з манжетами. Підтримувати тиск в манжеті необхідно таким, аби забезпечити мінімальну оклюзію (попередити витік повітря навколо ендотрахеальної трубки) — зазвичай, тиск в манжеті повинен становити 200 мм водного стовпчика.
33. Інтубованим дітям не рекомендовано призначати пробіотики з профілактичною метою.
34. У дітей старше 10 років для довготривалої інтубації рекомендовано використовувати ендотрахеальні трубки із дренажним портом для відсмоктування секрету, що накопичується в субглотковій ділянці.
35. Не рекомендовано застосовувати для профілактики ВАП у дітей:
1) системну антибіотикотерапію при ШВЛ-асоційованому трахеобронхіті;
2) місцеві АМП для недопущення колонізації ротоглотки через ризик розвитку захворювань, що викликані Clostridium difficile;
3) хлоргексидинвмісні засоби для догляду за ротовою порожниною;
4) лікарські засоби для профілактики стресової виразки шлунку;
5) ранню трахеостомію;
6) ендотрахеальні трубки покриті сріблом;
7) закриті системи санації трахеї і бронхів.
VI. Профілактика захворювань, спричинених Clostridium difficile
1. До факторів ризику виникнення захворювань, спричинених Clostridium difficile відносять:
1) антибіотикотерапія:
захворювання, що викликані Clostridium difficile (далі — КДІ) спровоковані використанням антибіотиків (найбільший ризик пов’язаний із застосуванням фторхінолонів, цефалоспоринів третього та четвертого поколінь і кліндаміцину);
регулярне використання антибіотиків у тваринництві може призводити до спалахів КДІ на певній території;
2) ІПНМД:
пацієнти можуть інфікуватися в будинках для людей похилого віку та лікарнях (захворювання розвивається внаслідок перорального передавання збудника після контакту із контамінованими спорами предметами і поверхнями, при чому медичні працівники можуть бути переносниками клостридій у разі недотримання правил гігієни рук);
довготривала госпіталізація або перебування в будинку для людей похилого віку — незалежні фактори ризику розвитку КДІ;
постійне вживання лікарських засобів для зниження продукції шлункової кислоти (наприклад, антагоністи Н2-рецепторів та інгібітори протонної помпи).
2. Заходи з профілактики КДІ та ізоляції пацієнтів:
1) затвердити алгоритм дій медичних працівників при виявленні підозри, ймовірного або підтвердженого випадку КДІ;
2) пацієнтів із КДІ ізолювати у одномісну кімнату із туалетом;
3) контактних заходів захисту дотримуватися протягом всього часу перебування пацієнта в закладі;
4) дотримуватися рекомендованих практик гігієни рук відповідно до додатку 1 до Інструкції;
5) використовувати індивідуальні прилади для даної групи пацієнтів (наприклад, термометри, тонометри, стетоскопи тощо);
6) пацієнт має щоденно приймати душ або ванну із милом.
3. Підтвердження КДІ:
1) працівниками клінічного структурного підрозділу проводиться оцінка необхідності тестування — слід провести диференційну діагностику із іншими захворюваннями, що можуть супроводжуватися діареєю;
2) перед дослідженням калу на Clostridium difficile не менше ніж за 48 годин необхідно відмінити послаблюючі лікарські засоби та впевнитися, що симптоми зберігаються;
3) повторне дослідження калу на Clostridium difficile не рекомендовано проводити з метою оцінки ефективності лікування (результати можуть бути позитивними близько шести тижнів);
4) працівники лабораторії повинні проводити періодичні планові (щонайменше раз на півроку) перевірки несформованого калу, що доставлений в лабораторію, на Clostridium difficile та її токсини;
5) в разі підтвердження КДІ, працівники лабораторії повинні негайно сповістити лікуючого лікаря.
4. Заходи щодо очищення і дезінфекції:
1) розробити та затвердити СОП щоденного і генерального прибирань у палаті/кімнаті, де перебуває пацієнт із КДІ;
2) щоденне прибирання та обробку в палаті/кімнаті проводити із використанням дезінфекційних засобів із спороцидним ефектом;
3) проводити щоденну обробку дезінфекційним засобом всіх поверхонь, що мають безпосередній контакт із пацієнтом та в зоні догляду пацієнта, в тому числі туалетної/ванної кімнати, всіх поверхонь, що мають високий ризик доторкування (наприклад, ручки дверей);
4) в разі необхідності використання медичного обладнання для іншого пацієнта, провести обробку такого обладнання дезінфекційним засобом;
5) при відвідуванні пацієнтом підрозділів лікарні (наприклад, кабінет УЗД або відділення радіології) слід провести обробку дезінфекційним засобом об’єктів середовища до яких він торкався;
6) необхідно проводити обробку дезінфекційним засобом рухомих об’єктів у лікарні (наприклад, маніпуляційний столик) після перебування їх у палаті/кімнаті, де знаходиться пацієнт із КДІ;
7) як додатковий захід із профілактики розповсюдження КДІ рекомендовано використовувати ультрафіолетове опромінення поверхонь після проведення їх очищення і дезінфекції.
5. Клінічний провізор ВІК проводить оцінку доцільності призначення антибіотиків, особливо із групи фторхінолонів, цефалоспоринів третього і четвертого поколінь і кліндаміцину.
6. Під час спалаху КДІ, працівникам, які проводить догляд за пацієнтами із КДІ, заборонено приймати участь у догляді за пацієнтами без КДІ.
VII. Профілактика інфекційних хвороб, пов’язаних із наданням медичної допомоги серед медичних працівників
1. Керівник ЗОЗ повинен забезпечити умови для здійснення заходів щодо охорони здоров’я медичних працівників.
2. При прийомі на роботу в ЗОЗ медичні працівники інформуються про фактори ризику при виконанні своїх професійних обов’язків, дотримання правил попередження професійних захворювань. У подальшому не менше одного разу на півроку всі медичні працівники повинні проходити інструктаж з питань профілактики ІПНМД та безпеки праці, один раз на місяць — навчання відповідно до графіку навчання з ПІІК, затвердженого керівником ЗОЗ.
3. Обов’язкові профілактичні медичні огляди медичних працівників ЗОЗ проводяться відповідно до наказу Міністерства охорони здоров’я України від 23 липня 2002 року № 280 «Щодо організації проведення обов’язкових профілактичних медичних оглядів працівників окремих професій, виробництв і організацій, діяльність яких пов’язана з обслуговуванням населення і може призвести до поширення інфекційних хвороб», зареєстрованого у Міністерстві юстиції України 08 серпня 2002 року за № 639/6927.
4. Профілактика професійних заражень передбачає використання заходів захисту, імунізацію та хіміопрофілактику, які наведені в Заходах та Засобах щодо попередження інфікування при проведенні догляду за пацієнтами, затверджених наказом Міністерства охорони здоров’я України від 03 серпня 2020 року № 1777, зареєстрованих в Міністерстві юстиції України 10 листопада 2020 року за № 1110/35393.
5. У випадку професійної аварії, яка мала місце під час роботи з ВІЛ-інфікованим або біологічним матеріалом від ВІЛ-інфікованого, проводиться екстрена післяконтактна профілактика відповідно до Порядку проведення екстреної постконтактної профілактики ВІЛ-інфекції у працівників при виконанні професійних обов’язків, затвердженого наказом Міністерства охорони здоров’я України від 05 листопада 2013 року № 955, зареєстрованого Міністерством юстиції України 20 листопада 2013 року за № 1980/24512.
6. Щодо кожного нещасного випадку або аварії в ЗОЗ проводяться їх облік та розслідування відповідно до Порядку розслідування та обліку нещасних випадків, професійних захворювань та аварій на виробництві, затвердженого постановою Кабінету Міністрів України від 17 квітня 2019 року № 337.
VIII. Порядок розслідування та ліквідації спалаху інфекцій, що пов’язані із наданням медичної допомоги
1. ВІК проводить попередню порівняльну оцінку випадків захворювання з фоновим рівнем ІПНМД в ЗОЗ. У разі підтвердження наявності спалаху ВІК складає попередній план розслідування спалаху та попередження його поширення, який затверджується керівником ЗОЗ та узгоджується із закладом громадського здоров’я, на який покладено виконання функцій епідеміологічного нагляду (спостереження) у відповідній адміністративно-територіальній одиниці (далі — ЗГЗ).
2. Для проведення розслідування причин виникнення спалаху ІПНМД та його ліквідації ЗГЗ створюється протиепідемічна комісія (далі — комісія), до складу якої входять:
1) представник(и) ЗГЗ;
2) керівник ВІК, координатор з гігієни рук та лікар-епідеміолог ЗОЗ, в якому є спалах;
3) представник державної установи «Центр громадського здоров’я Міністерства охорони здоров’я України» (за згодою);
4) представник Міністерства охорони здоров’я України (за згодою);
5) представник структурного підрозділу з питань охорони здоров’я виконавчого органу влади у відповідній адміністративно-територіальній одиниці (за згодою);
6) співробітники кафедр закладів вищої медичної освіти та науково-дослідних інститутів (за згодою);
7) інші члени за необхідності.
Головою протиепідемічної комісії є представник ЗГЗ.
3. У разі необхідності комісія, з урахуванням конкретних обставин, уточнює попередній план розслідування і ліквідації спалаху ІПНМД. Уточнений план розслідування і ліквідації спалаху підписується всіма членами комісії.
4. При проведенні розслідування причин виникнення спалаху ІПНМД головою комісії визначається завдання та об’єм роботи кожного члена комісії.
5. Основні етапи розслідування:
1) збір та вивчення інформації, а саме:
звітів щодо ПІІК в ЗОЗ;
поточного та п’ятирічного планів дій з ПІІК;
результати оцінки знань медичних працівників про гігієну рук;
результати оцінки наявної інфраструктури і ресурсів для гігієни рук;
форм збору даних рутинного епідеміологічного нагляду;
2) верифікація діагнозу в усіх зареєстрованих випадках захворювань з використанням Критеріїв, за якими визначаються випадки інфекційних та паразитарних захворювань, які підлягають реєстрації, затверджених наказом Міністерства охорони здоров’я України від 28 грудня 2015 року № 905, зареєстрованих у Міністерстві юстиції України 12 березня 2016 року за № 379/28509;
3) підтвердження наявності спалаху;
4) активне виявлення всіх випадків захворювання;
5) оцінка стану впровадження ПІІК за наступними протоколами:
протокол системної самооцінки ПІІК в ЗОЗ (додаток 4 до Порядку впровадження профілактики інфекцій та інфекційного контролю в закладах охорони здоров’я, які надають медичну допомогу в стаціонарних умовах, затвердженого наказом Міністерства охорони здоров’я України від 03 серпня 2021 року № 1614;
протокол системної самооцінки гігієни рук в ЗОЗ/ЗСЗ (додаток 10 до Інструкції);
6) формулювання попередньої гіпотези щодо факторів ризику виникнення спалаху (динаміки захворюваності, установлення ризику зараження, вивчення структури захворілих та співставлення з проведенням діагностичних і медичних маніпуляцій);
7) розробка і організація заходів щодо ліквідації спалаху, з урахуванням властивостей встановленого збудника, шляхів і факторів передавання;
8) оцінка ефективності заходів.
5. Комісія організовує проведення внутрішньовидового типування та, за необхідності, секвенування виділених мікроорганізмів з визначенням сероварів, фаговарів, антибіотикограм і профілів АМР. Аналіз отриманих даних використовується для визначення шляхів і факторів передавання ІПНМД, заходів щодо їх недопущення в майбутньому.
6. Під час спалаху, з метою виявлення можливого джерела збудників інфекції, комісія організовує проведення серед медичних працівників позачергове бактеріологічне обстеження з дослідженням біологічного матеріалу залежно від етіології та нозологічної форми ІПНМД, наприклад:
1) при стафілококовій етіології спалаху — слизові оболонки передніх відділів носа;
2) при стрептококовій етіології — матеріал із зіву;
3) при виникненні захворювань на сальмонельоз та інші гострі кишкові інфекції, в тому числі вірусної етіології, проводяться необхідні мікробіологічні та вірусологічні дослідження.
7. В разі спалаху ІОХВ комісія організовує проведення оцінки ефективності всіх етапів очищення, дезінфекції і стерилізації (репроцесингу) медичних виробів обмеженого використання на підставі позачергових бактеріологічних досліджень та/або позапланової валідації процесів очищення, дезінфекції і стерилізації.
8. Комісією проводиться співставлення збудників ІПНМД, виділених від пацієнтів, та мікроорганізмів, виділених від медичних працівників, інструментарію, за типовою належністю, а також за біологічними властивостями, зокрема за профілями АМР.
9. Висновки про характер спалаху, шляхи та фактори передавання інфекційних агентів (наприклад, руки медичних працівників, лікарські засоби, інструменти) визначаються комісією на основі обстеження пацієнтів, медичних працівників, інструментарію і проведених оцінювань відповідно до пункту 5 цього розділу.
10. Комісія виявляє обставини, що сприяли виникненню групових захворювань, наприклад:
1) несвоєчасна ізоляція та переведення захворілих;
2) порушення в роботі централізованого стерилізаційного відділення, аптеки, пральні тощо;
3) недотримання медичними працівниками санітарно-гігієнічних та протиепідемічних правил і вимог;
4) аварійні ситуації в системі водопостачання, каналізації, вентиляції, електромережі, а також постійні перебої у водопостачанні;
5) нерегулярні навчання і підготовка медичних працівників з ПІІК;
6) недостатня забезпеченість мийними та/або дезінфекційними засобами, засобами стерилізації або їх використання з порушенням інструкції;
7) недостатня матеріально-технічна забезпеченість ЗОЗ.
11. На основі аналізу захворюваності на ІПНМД, їх етіологічної структури, особливостей клінічного перебігу, умов, що сприяли виникненню спалаху, біологічної характеристики штамів, які циркулюють в закладі, комісія робить висновки про причини спалаху, джерело інфекції, шляхи та фактори передавання, що обумовили виникнення захворювання. З урахуванням цих висновків в ЗОЗ терміново розробляється та реалізується комплекс протиепідемічних і профілактичних заходів щодо локалізації та ліквідації спалаху ІПНМД.
12. У комплексі заходів щодо ліквідації спалаху відображаються вимоги для усунення виявлених порушень в роботі ЗОЗ та пропозиції щодо запобігання епідемічним ускладненням в майбутньому.
13. Результати розслідування спалаху та розроблені заходи щодо його ліквідації доводяться до відома керівника та медичних працівників ЗОЗ.
14. Звіт щодо результатів проведеного розслідування спалаху і прийняті заходи підписується всіма членами комісії, зберігається у ЗОЗ та ЗГЗ протягом п’яти років і враховується при розробці щорічного і п’ятирічного планів дій з ПІІК.
Генеральний директор Директорату громадського здоров’я
та профілактики захворюваності
І. Руденко
Додаток 1
до Порядку профілактики інфекційних хвороб, пов’язаних
з наданням медичної допомоги, в закладах охорони здоров’я,
які надають медичну допомогу в стаціонарних умовах
(підпункт 1 пункту 7 розділу II)
Примірна стандартна операційна процедура «Контрольний список послідовності дій для постановки центрального судинного катетеру»
Відділення: _______________________________________________________ Палата № : ______________ Дата: ___ /____ / ___ р. Початок: __ Закінчення: ______ Процедура відбувається: ВАРІТ/операційна/радіологія/інші: ___________________________ Прізвище, ім’я та по батькові (за наявності) лікаря, що виконує процедуру: ___________ Прізвище, ім’я та по батькові (за наявності) особи, що заповнює форму: ______________ Тип катетера: діалізний/ тунельований/ нетунельований/ імплантований/ неімплантований/ встановлений периферично центральний катетер Імпрегнація: так/ні Кількість ліній: ______ Номер партії катетера: ______________________ Судина: яремна/грудна/підключична/стегнова/тім’ячко/пупкова/ ____________________ Частина тіла: права/ліва Використання провідника: так/ні Причина постановки: новий доступ / несправність / планова заміна / аварійна заміна |
|||||
Крок |
Так |
Так з нагадуванням |
Ні* |
Не застосовується |
Коментарі |
1 |
2 |
3 |
4 |
5 |
6 |
До процедури: |
|||||
Пацієнта інформують щодо необхідності і наслідках постановки центрального судинного катетеру, а також про процедуру введення і догляду за ним |
|||||
Визначення наявності алергії на латекс і, за необхідності, заміна витратних матеріалів |
|||||
Оцінка ризику зараження пацієнта (якщо високий, необхідно зазначити причину) |
|||||
Оцінка наявної антикоагуляційної терапії |
|||||
Форма згоди та інші супутні документи заповнені (за виключення постановки у надзвичайній або екстреній ситуації) |
|||||
Лікар та його помічник провели гігієнічну обробку рук |
|||||
Витратні матеріали і необхідне обладнання наявні та перевірені |
|||||
Метод підтвердження правильного розміщення обрано |
|||||
Пацієнт ідентифікований щонайменше з двох джерел (за виключення постановки у надзвичайній або екстреній ситуації) |
|||||
Визначено максимальний термін проведення процедури |
|||||
Визначено та позначено місце проколу |
|||||
Пацієнт укладений для проведення процедури |
|||||
Шкіра в місці майбутнього проколу оброблена 2% розчином хлоргексидину або 70% спиртом у дитини до 2 місяців |
|||||
Шкіра висохла після обробки |
|||||
Тіло пацієнта покрите стерильною серветкою від голови до п’ят |
|||||
Всі, хто бере участь у постановці, одягнені в стерильні медичні рукавички, стерильний халат захисний від інфекційних агентів, шапочку медичну, медичну (хірургічну) маску і захисні окуляри/щиток |
|||||
Всі інші, хто знаходиться у приміщенні, одягнені в хірургічну маску |
|||||
Катетер попередньо промитий стерильним розчином 0,9 % натрію хлориду, герметичність закруток/портів перевірено |
|||||
Виконана місцева анестезія або загальна седація |
|||||
Під час процедури (допустимо заповнити після закінчення процедури, якщо вона проводиться у екстреній/невідкладній ситуації та потребує залучення в процес особи, яка заповнює форму) |
|||||
Підтвердження розташування катетера за допомогою ультразвукової діагностики/ черезстравохідної ехокардіограми/ флюороскопії/ манометрії тощо |
|||||
Кров аспірується із кожної лінії (правильність внутрішньосудинного розташування кінчика катетера підтверджено) |
|||||
Яким розчином та яким об’ємом (мл) було промито катетер: __________ |
|||||
Всі закрутки розміщені правильно |
|||||
Всі закрутки затиснені |
|||||
Катетер закріплено (пришито/пристептовано/ закріплено стерильною клейкою пов’язкою) |
|||||
Розміщення кінчика катетеру підтверджено методом рентгенографії або рентгеноскопії |
|||||
Стерильність поля дотримана |
|||||
Під час процедури катетер не був пошкоджений |
|||||
Лікар, який виконував процедуру, був замінений після третьої невдалої спроби постановки катетеру |
|||||
Кров прибрана із області місця проколу |
|||||
Накладено стерильну пов’язку |
|||||
Після процедури |
|||||
На пов’язці зазначено дату накладення |
|||||
Рентгенологічно перевірено відсутність ускладнень маніпуляцій та правильність розташування катетеру |
|||||
Заплановано заміну катетеру |
|||||
Пацієнт отримав необхідну інформацію щодо правильного поводження і догляду за катетером |
|||||
________ Виміри катетеру: внутрішня частина: ____ мм. зовнішня частина: ____ мм. |
Додаток 2
до Порядку профілактики інфекційних хвороб, пов’язаних з наданням
медичної допомоги, в закладах охорони здоров’я,
які надають медичну допомогу в стаціонарних умовах
(підпункт 1 пункту 4 розділу IV)
Показання до постановки сечового катетеру
Показання |
Недоречне застосування |
1. Гостра затримка сечі або блок сечового міхура. |
1. Пацієнтам із нетриманням сечі без показань. |
Додаток 3
до Порядку профілактики інфекційних хвороб, пов’язаних
з наданням медичної допомоги, в закладах охорони здоров’я,
які надають медичну допомогу в стаціонарних умовах
(підпункт 6 пункту 6 розділу IV)
Примірна стандартна операційна процедура «Катетеризація сечового міхура»
Умова |
Алгоритм виконання |
1 |
2 |
Вимоги до безпеки праці |
1. До і після процедури провести практику з гігієни рук. |
Інформування пацієнта |
1. Лікар отримує від пацієнта (або законного представника) згоду на проведення процедури. |
Необхідний набір матеріалів та засобів |
1. Медичні рукавички. |
Методика виконання |
Підготовка до процедури: |
Методика виконання |
Виконання процедури у жінок: |
Додаткові відомості |
1. Заборонено виконувати дві неуспішні спроби катетеризації сечового міхура. |
Результат |
Виділення сечі. |
ЗАТВЕРДЖЕНО
Наказ Міністерства охорони здоров’я України
03 серпня 2021 року № 1614
Зареєстровано
в Міністерстві юстиції України
11 жовтня 2021 р. за № 1320/36942
Порядок впровадження профілактики інфекцій та інфекційного контролю в закладах охорони здоров’я, які надають медичну допомогу в стаціонарних умовах
I. Загальні положення
1. Цей Порядок визначає порядок організації профілактики інфекцій та інфекційного контролю в закладах охорони здоров’я, які надають медичну допомогу у стаціонарних умовах (далі — ЗОЗ).
2. Цей Порядок є обов’язковим для ЗОЗ незалежно від форми власності та їх відомчого підпорядкування.
3. Відповідальними за виконання цього Порядку у ЗОЗ є його керівник, а у структурних підрозділах ЗОЗ — керівники структурних підрозділів та керівник відділу з інфекційного контролю.
4. У цьому Порядку терміни та умовні скорочення вживаються у такому значенні:
EUCAST — Європейський комітет з визначення чутливості до антимікробних препаратів;
інфекційні хвороби, пов’язані із наданням медичної допомоги — хвороби, що виникають у пацієнта під час догляду. Інфекційні захворювання, що наявні або знаходяться в інкубаційному періоді на момент госпіталізації або початку лікування, до ІПНМД не відносяться. До ІПНМД належать інфекційні захворювання, які набуті в ЗОЗ, але клінічно проявилися після закінчення лікування, у разі достовірно доведеного зв’язку із проведеними лікувальними або діагностичними заходами. Окремою групою ІПНМД є інфекційні захворювання серед працівників, що надбані безпосередньо під час виконання професійних обов’язків;
інфекційний контроль — комплекс організаційних, профілактичних та протиепідемічних заходів, спрямованих на попередження виникнення та розповсюдження ІПНМД, що базується на результатах епідеміологічного нагляду;
стандартна операційна процедура — набір покрокових інструкцій, що складаються в організації з метою допомогти працівникам виконувати рутинні операції найбільш ефективним чином;
АМР — антимікробна резистентність;
ВІЛ — вірус імунодефіциту людини;
ВІК — відділ з інфекційного контролю;
ІПНМД — інфекційні хвороби, пов’язані з надання медичної допомоги;
МАМР — множинна резистентність мікроорганізмів до антимікробних препаратів;
ММС — мультимодальна стратегія або комплексний спосіб досягнення змін у системі, мікрокліматі колективу та його поведінці, що підтримує прогрес в профілактиці інфекцій та інфекційному контролі в ЗОЗ та в результаті приносить позитивні зміни як для пацієнтів, так і для працівників ЗОЗ;
ПІІК — профілактика інфекцій та інфекційний контроль;
СОП — стандартна операційна процедура.
Інші терміни у цьому Порядку вживаються у значеннях, наведених в Законах України «Основи законодавства України про охорону здоров’я», «Про захист населення від інфекційних хвороб» та інших нормативно-правових актах у сфері охорони здоров’я.
5. Запровадження ПІІК в ЗОЗ відіграє вирішальну роль не тільки в профілактиці ІПНМД, а й у забезпеченні готовності і реагуванні при критичних ситуаціях, що пов’язані із розповсюдженням інфекційних захворювань.
Цим Порядком встановлюється комплексний підхід до впровадження ПІІК в ЗОЗ.
6. Основоположними принципами ПІІК є:
1) основа профілактики розповсюдження ІПНМД та АМР — безпечна практика надання медичної допомоги в безпечних умовах;
2) більшість видів ІПНМД можна попередити шляхом проведення тривалих та стійких, затратоефективних утручань;
3) ПІІК в ЗОЗ має вирішальне значення для зведення до мінімуму передавання збудників інфекційних хвороб, а також для забезпечення готовності та попередження спалахів;
4) для ефективного забезпечення ПІІК необхідне впровадження всіх основних компонентів ПІІК;
5) кожен основний компонент ПІІК запроваджується відповідно до місцевих пріоритетів і наявних ресурсів та адаптується до загальнонаціонального рівня і до рівня окремих ЗОЗ;
6) упродовж всіх етапів впровадження ПІІК проводиться повсякденна діяльність ЗОЗ.
7. До основних компонентів ПІІК відносяться:
1) план дій з ПІІК;
2) СОП, що базуються на доказовій базі;
3) навчання та підготовка;
4) епідеміологічний нагляд за ІПНМД;
5) моніторинг, оцінка та зворотній зв’язок;
6) режим роботи, штатний розпис та навантаження на ліжко;
7) приміщення, матеріали та обладнання.
Основні компоненти ПІІК впроваджуються із застосуванням ММС щодо кожного з них.
8. ММС має першорядне значення для реалізації ПІІК на практиці та включає:
1) зміни в системі;
2) навчання і підготовку;
3) моніторинг, оцінку та зворотній зв’язок;
4) нагадування та комунікацію;
5) культуру безпеки.
9. Метою ПІІК із застосуванням ММС є вдосконалення надання медичної допомоги і зниження кількості ІПНМД, в тому числі викликаних збудниками з АМР.
10. Застосування ММС забезпечує комплексний підхід до реалізації ПІІК. ММС застосовується від початку розробки заходів з ПІІК. Алгоритм розробки плану дій з ПІІК в ЗОЗ із застосуванням ММС наведено у додатку 1 до цього Порядку.
11. При розгляді компонентів ПІІК із застосуванням ММС враховується наступне:
1) матеріально-технічні та інфраструктурні зміни, які необхідні для полегшення введення в дію заходів з ПІІК (включає в себе розгляд механізмів закупівлі та постачання, доступності води та вивчення ергономічних факторів, що впливають на робочий процес);
2) необхідність в навчанні та підготовці (включає в себе друковані, електронні та усні джерела інформації, інтерактивні тренінги та симуляції біля ліжка хворого);
3) визначення індикаторів (включає моніторинг виконання заходів з ПІІК та вивчення індикаторних показників);
4) визначення типів і методів нагадування на робочому місці (натяки на дії, інформаційні матеріали, прямі втручання та заохочення);
5) пріоритет ПІІК в ЗОЗ (працівники ВІК, керівники закладу та структурних підрозділів є прикладом для наслідування).
12. Розробку заходів та впровадження ПІІК у ЗОЗ здійснює ВІК, який створюється відповідно до Положення про відділ з інфекційного контролю закладу охорони здоров’я та установи / закладу надання соціальних послуг / соціального захисту населення, затвердженого наказом Міністерства охорони здоров’я України від 03 серпня 2021 року № 1614.
II. Основні компоненти ПІІК
1. ВІК при розробці плану дій з ПІІК розглядає кожен із основних компонентів ПІІК. Кінцевою метою ВІК має стати повне впровадження та всебічна підтримка ПІІК.
2. План дій з ПІІК затверджується в кожному ЗОЗ з метою профілактики ІПНМД та боротьби із АМР. Приклади заходів для впровадження основних компонентів ПІІК наведено у додатку 2 до цього Порядку.
3. При розробці плану дій з ПІІК враховується наступне:
1) план дій розробляється на основі епідеміологічних даних і пріоритетів, що були виявлені після проведення базової оцінки у ЗОЗ, на період не менше одного року;
2) заходи плану дій забезпечуються ресурсами (фінансовими, кадровими та іншими);
3) заходи мають бути чіткими, реалістичними та із визначеними індикаторами виконання, цілями (досягнутим результатом);
4) деякі компоненти ПІІК можуть бути впроваджені та виконані в рамках інших програм ЗОЗ (наприклад, інфекційний контроль в закладах, що надають допомогу хворим на туберкульоз, протидія розповсюдженню ВІЛ/СНІДу, покращення практик гігієни рук);
5) підходи до моніторингу і оцінки, навчання та підготовки;
6) забезпечення зворотного зв’язку;
7) інструменти (протоколи, анкети, тести), які будуть використовуватися для перевірки теоретичних та практичних знань працівників ЗОЗ;
8) для розробки заходів застосовується ММС відповідно до додатку 1 до цього Порядку.
4. СОП з ПІІК розробляються ВІК:
1) із залученням відповідних зацікавлених сторін (наприклад, керівники структурних підрозділів, провідні спеціалісти, старші сестри медичні, менеджери з якості);
2) з використанням даних доказової медицини та адаптуються до місцевих умов ЗОЗ.
5. ВІК в своїй роботі використовує як мінімум наступні СОП з ПІІК:
1) стандартні заходи захисту, відповідно до розділу XI Заходів та Засобів щодо попередження інфікування при проведенні догляду за пацієнтами, затверджених наказом Міністерства охорони здоров’я України від 03 серпня 2020 року № 1777, зареєстрованих в Міністерстві юстиції України 10 листопада 2020 року за № 1110/35393 (далі — Заходи);
2) заходи захисту засновані на недопущенні інфікування, відповідно до Заходів;
3) профілактика інфікування під час оперативних втручань;
4) профілактика катетер-асоційованих інфекцій кровотоку;
5) профілактика вентилятор-асоційованих пневмоній;
6) профілактика катетер-асоційованих інфекцій сечовивідних шляхів;
7) профілактика передавання МАМР;
8) очищення і дезінфекції поверхонь, відповідно до додатку 8 до Заходів та Засобів щодо попередження інфікування при проведенні догляду за пацієнтами, затверджених наказом Міністерства охорони здоров’я України від 03 серпня 2020 року № 1777, зареєстрованих в Міністерстві юстиції України 10 листопада 2020 року за № 1110/35393;
9) очищення, дезінфекція і стерилізація (репроцесинг) медичних виробів;
10) раціональне використання антимікробних препаратів;
11) готовність до спалахів інфекційних хвороб та управління ними.
6. Перед введенням в дію нових СОП обов’язково проводиться навчання для працівників із відпрацюванням практичних навичок.
7. Проста форма і доступність СОП для працівників мають вирішальне значення для їх застосування, тому СОП рекомендується розповсюджувати різними способами (електронна пошта, роздруківки, соціальні мережі).
8. Послідовність імплементації СОП, навчання і підготовки, моніторингу, оцінки, зворотного зв’язку та епіднагляду визначається із урахуванням місцевого контексту.
9. Виконання СОП підлягає регулярному моніторингу.
10. Навчання і підготовка з ПІІК проводяться для всіх працівників та включають теоретичні і практичні навчання, симуляції ІПНМД, захворювань викликаних мікроорганізмами з АМР та перевірку знань.
Використовується змішаний підхід до навчання — письмові матеріали, електронне або дистанційне навчання та лекції поєднуються з інтерактивними і практичними заняттями, у тому числі біля ліжка хворого. В ЗОЗ запроваджуються індивідуальні, колективні та колегіальні механізми наставництва, які контролюють та допомагають працівникам підвищувати продуктивність. Рекомендується навчання та наставництво без відриву від роботи — проведення фахівцями з ПІІК тренінгів, майстер-класів або моделювання ситуацій біля ліжка хворого.
11. Виконання функцій координації навчання і підготовки з ПІІК покладається на одного із працівників ВІК (далі — координатор навчання і підготовки з ПІІК). Координатор навчання і підготовки з ПІІК повинен постійно підвищувати свій рівень теоретичних та практичних знань.
12. Розробка навчальних та підготовчих занять включається до плану дій з ПІІК в ЗОЗ.
13. Перед початком навчання і підготовки проводиться оцінка базового рівня знань з ПІІК у працівників ЗОЗ.
У випадку відсутності в ЗОЗ фахівців для проведення оцінки та навчання з ПІІК, розглядається питання залучення зовнішніх консультантів з ПІІК.
14. Плани та програми навчання працівників готуються з урахуванням їх функціональних обов’язків з ПІІК:
1) спеціалізоване навчання та підготовка фахівців з ПІІК (лікарі, сестри медичні та інші працівники, які входять до складу ВІК), забезпечення їх безперервного професійного розвитку (включаючи передові технології і практики, наставницькі навики, методики реалізації та підтримки тощо);
2) базове навчання та підготовка із ПІІК для всіх медичних працівників, які беруть участь у наданні медичних послуг та догляді за пацієнтами. Для медичних працівників, що надають вторинну (спеціалізовану) медичну допомогу (наприклад, працівники відділень хірургії) проводяться додаткові (вузьконаправлені) навчання і підготовка з ПІІК;
3) ознайомче навчання із ПІІК для працівників адміністративних та управлінських структурних підрозділів, обслуговуючого персоналу, прибиральників тощо.
15. У ЗОЗ проводиться регулярна (не менше одного разу на рік) оцінка ефективності навчання.
16. Навчання з ПІІК інтегрується у різні кадрові процеси в ЗОЗ (наприклад, під час випробувального терміну медичний працівник проходить навчання та підготовку із ПІІК та складає іспит). ЗОЗ забезпечує навчання для всіх нових співробітників, а також безперервне підвищення обізнаності з ПІІК з врахуванням нових даних для всіх працівників щорічно.
17. Компонент навчання і підготовки з ПІІК у ЗОЗ включає також навчання і підготовку пацієнтів та їхніх родичів (першочергово правильний догляд за хворими із особливими потребами), відповідні заходи відображаються у плані дій з ПІІК в ЗОЗ.
18. Епідеміологічний нагляд за ІПНМД у ЗОЗ проводиться з метою виявлення найбільш розповсюджених ІПНМД та реєстрації їх спалахів, включаючи викликані мікроорганізмами з АМР, відповідно до Порядку здійснення епідеміологічного нагляду та ведення обліку інфекційних хвороб, пов’язаних з наданням медичної допомоги, затвердженого наказом Міністерства охорони здоров’я України від 03 серпня 2021 року № 1614.
19. Мікробіологічна лабораторія із можливістю визначення АМР, в якій впроваджено методику EUCAST, є невід’ємною частиною епідеміологічного нагляду за ІПНМД.
20. Показники розповсюдженості ІПНМД та мікроорганізмів з АМР в ЗОЗ, що отримані шляхом епідеміологічного нагляду, використовуються для:
1) управління стратегіями і пріоритетами ПІІК, а також оцінки ефективності і результативності вжитих заходів;
2) порівняльного аналізу з метою оцінки тенденцій розповсюдженості ІПНМД та мікроорганізмів з АМР в часі;
3) виявлення важливих епідеміологічних тенденцій або спалахів для забезпечення прийняття консолідованих рішень та дій в сфері громадського здоров’я.
21. Питання епідеміологічного нагляду за ІПНМД розглядаються під час розробки плану дій з ПІІК. Проведення епідеміологічного нагляду за всіма видами ІПНМД є необов’язковим, за виключенням катетер-асоційованих інфекцій кровотоку (далі — КАІК), катетер-асоційованих інфекцій сечовивідних шляхів, вентилятор-асоційованих пневмоній та інфекцій області хірургічного втручання (далі — ІОХВ).
22. ВІК визначає на які ІПНМД буде направлений епідеміологічний нагляд, враховуючи місцеві особливості, та використовує Критерії, за якими визначаються випадки інфекційних та паразитарних захворювань, які підлягають реєстрації, затверджені наказом МОЗ України від 28 грудня 2015 року № 905, зареєстровані в Міністерстві юстиції України 12 березня 2016 року за № 379/28509.
23. Додатковими рекомендованими інфекційними захворюваннями (окрім девайс-асоційованих ІПНМД та ІОХВ) для епідеміологічного нагляду можуть бути:
1) пріоритетні місцеві інфекційні хвороби, що здатні спричинити спалах (наприклад, норовіруси, ротавіруси, вірус грипу, туберкульоз, тяжкий гострий респіраторний синдром);
2) інфекційні хвороби серед сприятливих груп населення (наприклад, новонароджені, хворі відділень інтенсивної терапії, пацієнти з опіками, ВІЛ-інфіковані);
3) інфекційні хвороби, що пов’язані із професійною медичною діяльністю (наприклад, гепатити В і С, ВІЛ, туберкульоз, грип, кір, кашлюк).
24. Заходи з проведення епідеміологічного нагляду за ІПНМД пов’язані із оцінкою безпеки та якості надання медичних послуг пацієнтам і погоджуються із керівництвом ЗОЗ та керівниками цільових клінічних структурних підрозділів. Ці заходи можуть потребувати залучення додаткових ресурсів.
25. Основною метою практики моніторингу, оцінки і зворотного зв’язку з ПІІК є підтримка досягнутих результатів у ПІІК в ЗОЗ та сприяння покращенню їх в майбутньому, що зменшує ризик розповсюдження ІПНМД та мікроорганізмів з АМР.
Цей основний компонент ПІІК включає оцінку ступеню відповідності стандартам та вимогам, оцінку дій та цілей, які вже досягнуті та оцінку тих аспектів, що потребують покращення.
Хірургічна та гігієнічна обробка рук медичних працівників є критичним показником, включаючи моніторинг її дотримання.
26. Моніторинг та зворотній зв’язок направлено на залучення зацікавлених сторін, створення партнерських відносин і робочих груп, формування професійних мереж.
27. Реалізація моніторингу, оцінки та зворотного зв’язку з ПІІК в ЗОЗ потребує проходження навчання фахівцями ВІК.
28. Навчання із використанням даних, які отримані шляхом моніторингу, оцінки і зворотного зв’язку є інструментом в переконанні працівників ЗОЗ щодо існування проблеми та в тому, що вибране рішення було правильним.
29. Питання моніторингу, оцінки і зворотного зв’язку є невід’ємною частиною процесу впровадження ПІІК та розглядаються на етапі розробки плану дій з ПІІК.
Необхідність у впровадженні моніторингу, оцінки і зворотного зв’язку виникає після проведення системної самооцінки ПІІК у ЗОЗ і отримання її результатів.
Практики і процеси, обрані для моніторингу повинні базуватися на результатах оцінювання. Також слід враховувати можливість зворотного зв’язку по обраним видам діяльності та варіанти його здійснення.
Індикатори, які використовуються для моніторингу, визначаються відповідно до практик/процедур, що є пріоритетними у ЗОЗ.
Обрані індикатори, практики, структурні підрозділи і відповідальні особи із чітким зазначенням обов’язків, частоти моніторингу і оцінки, графіку проведення зворотного зв’язку затверджуються керівництвом закладу.
План дій з моніторингу має містити чітко визначені заходи, індикатори їх виконання та інструменти (чек-листи, контрольні списки, форми тощо) для збору даних, які розробляються ВІК відповідно до заходів, визначених планом дій з ПІІК.
30. Моніторинг і оцінка проводиться мінімум по наступним видам діяльності та їх показниках:
1) дотримання правил гігієни рук;
2) постановка та догляд за внутрішньосудинним катетером;
3) постановка та догляд за сечовим катетером;
4) заходи по запобіганню ІОХВ;
5) реалізація заходів безпеки по недопущенню інфікування мікроорганізмами із АМР та висококонтагіозних інфекційних хвороб;
6) якість поточного та генерального прибирань;
7) очищення, дезінфекція і стерилізація (репроцесинг) медичного обладнання та інструментарію;
8) очищення і дезінфекція поверхонь;
9) використання антисептику для рук та рідкого мила;
10) використання антимікробних препаратів.
31. Для отримання зворотного зв’язку від зацікавлених сторін встановлюються механізми зворотного зв’язку (наприклад, наради, зустрічі, обговорення в групах, звіти, інформаційні бюлетені, публікації в журналах тощо), проводяться регулярні зібрання (мінімум раз на рік) для оприлюднення інформації по даним моніторингу з використанням аналізу тенденцій (помісячно, поквартально, по рокам тощо).
В навчанні використовується двонаправлений зворотній зв’язок з метою забезпечення підтримки культури навчання та поліпшення його якості.
32. Режим роботи, штатний розпис та зайнятість ліжка є основним компонентом ПІІК, що включає:
1) зайнятість ліжка в ЗОЗ не повинна перевищувати місткість — один пацієнт на одному ліжку та не менше одного метру між ліжками. У виняткових обставинах, при перевищенні пропускної спроможності ліжка, керівництво ЗОЗ повинно забезпечити залучення додаткових кадрів та достатню відстань між ліжками. Зайнятість ліжка, що перевищує місткість один пацієнт на одному ліжку та не менше одного метру між ліжками, невідповідний рівень укомплектованості медичними працівниками підвищують ризики спалахів ІПНМД та розповсюдження мікроорганізмів з АМР. Переповненість є визнаною проблемою громадського здоров’я, що може призводити до передавання інфекційних хвороб;
2) розгляд питань робочого навантаження, укомплектованості працівниками та зайнятості ліжок має стати частиною першочергових обговорень під час розробки плану дій з ПІІК. При цьому дотримання вимог щодо місткості, робочого навантаження та укомплектованості, штатного розпису працівників мають бути збалансованими із необхідністю надання невідкладної допомоги якомога більшій кількості пацієнтів при надзвичайних ситуаціях;
3) рішення, що стосуються робочого навантаження, укомплектування штатами і розміщення ліжок, приймаються на рівні керівництва ЗОЗ за погодженням з ВІК в частині забезпечення ПІІК. ВІК надає рекомендації з цих питань.
Цей основний компонент впливає на впровадження ПІІК в цілому та на реалізацію інших основних компонентів ПІІК.
33. Діяльність з догляду за хворими повинна проводитися у чистому приміщенні, що полегшує профілактику і контроль за ІПНМД та АМР. Це включає в себе всі елементи інфраструктури і наявність відповідних матеріалів та обладнання (наприклад, рукомийники, антисептики для рук, рідке мило, засоби індивідуального захисту).
Обладнання та засоби для гігієни рук мають бути легко доступні в точці догляду.
34. В ЗОЗ мають бути забезпечені:
1) наявність засобів для гігієни рук відповідно до Інструкції з впровадження покращення гігієни рук в закладах охорони здоров’я та установах / закладах надання соціальних послуг / соціального захисту населення, затвердженої наказом Міністерства охорони здоров’я України від 03 серпня 2021 року № 1614;
2) окремі кімнати гігієни для працівників і пацієнтів;
3) безпечне поводження з медичними відходами;
4) очищення та дезінфекція поверхонь;
5) очищення, дезінфекція і стерилізація (репроцесинг) виробів медичного призначення перед повторним використанням.
35. Ремонт та переобладнання приміщень, забезпечення необхідними матеріалами та обладнанням повинні стати частиною першочергових обговорень при розробці плану дій з ПІІК.
Цей основний компонент впливає на впровадження ПІІК в цілому, так як без сприятливого внутрішнього середовища, забезпеченості матеріалами і обладнанням для ПІІК покращення є недосяжними. Виявлення проблем в інфраструктурі і забезпеченні, які перешкоджають впровадженню ПІІК, є завданням ВІК.
36. Рішення, що стосуються приміщень, матеріалів та обладнання, приймаються на рівні керівництва ЗОЗ за погодженням з ВІК в частині забезпечення ПІІК. ВІК надає рекомендації з цих питань.
III. Етапи впровадження ПІІК
1. Підготовчий етап (крок 1) пов’язаний із підготовкою до оцінювання та покращення ПІІК в ЗОЗ.
2. Завдання та необхідні дії для реалізації підготовчого етапу, потенційні бар’єри та рішення для їх подолання наведено у додатку 3 до цього Порядку.
3. Показниками виконання підготовчого етапу (крок 1) є:
1) створено ВІК та призначено його керівника;
2) керівництво ЗОЗ ознайомлено із рекомендаціями по основним компонентам;
3) підготовано сценарії зустрічей керівника ВІК із керівництвом ЗОЗ та основні питання для дискусій;
4) створено список зацікавлених сторін;
5) зібрано попередні дані по впровадженню ПІІК в ЗОЗ;
6) вивчено можливості інтеграції ПІІК із іншими програмами, що вже впроваджені в ЗОЗ;
7) визначено перелік громадських об’єднань, що потенційно можуть допомогти у впровадженні та адвокації ПІІК;
8) проведено серію зустрічей із заінтересованими сторонами, лідерами думки і керівництвом ЗОЗ;
9) отримано погодження керівництва ЗОЗ для впровадження ПІІК;
10) визначено можливості для залучення людських та фінансових ресурсів для розробки, впровадження та підтримки плану дій з ПІІК.
4. Етап базової оцінки (крок 2) проводиться з урахуванням наступного:
1) проведення базової оцінки поточної ситуації із ПІІК в ЗОЗ для виявлення сильних та слабких сторін є важливим для постійного підвищення якості надання медичних послуг;
2) оцінка створює відчуття необхідності змін, що потрібні для покращення ПІІК, із урахуванням поточних ризиків, фактичних потреб і наявних ресурсів;
3) оцінка виявляє сильні сторони та позитивні досягнення задля переконання керівництва ЗОЗ у тому, що прогрес та успіх можливі.
5. Для проведення базової та подальших оцінок ЗОЗ використовується протокол системної самооцінки ПІІК у ЗОЗ відповідно до додатку 4 до цього Порядку.
6. Завдання та необхідні дії для реалізації етапу базової оцінки (кроку 2), потенційні бар’єри та рішення для їх подолання наведено у додатку 5 до цього Порядку.
7. Показниками виконання етапу базової оцінки (кроку 2) є:
1) працівники ВІК ознайомлені із системою самооцінки ПІІК у ЗОЗ;
2) план проведення оцінювання обговорений із керівництвом ЗОЗ та іншими зацікавленими сторонами, затверджений керівництвом ЗОЗ;
3) визначено працівника ВІК, який буде збирати дані оцінювання та формувати звіт, і терміни проведення оцінювання;
4) зібрано дані по кожному із основних компонентів ПІІК;
5) проаналізовано результати системної самооцінки ПІІК в ЗОЗ;
6) результати оцінювання представлені ВІК;
7) визначено дати проведення наступного оцінювання (не пізніше ніж через 12 місяців);
8) оформлено звіт відповідно до рекомендацій щодо підготовки звіту, наведених у додатку 4 до цього Порядку;
9) звіт представлено керівництву ЗОЗ та іншим зацікавленим сторонам.
8. Розробка та виконання плану дій з ПІІК (крок 3) здійснюється з урахуванням наступного:
1) план дій базується на результатах проведеної системної самооцінки ПІІК у ЗОЗ та результатах інших проведених оцінок, які вказують на пріоритетні сфери для втручання та сприяють досягненню згоди щодо підходів до зміцнення сильних та нівелювання дії слабких сторін у ПІІК ЗОЗ;
2) використання ММС відповідно до додатку 1 до цього Порядку полегшить розробку плану дій;
3) важливо на початку сконцентруватися на досягненні короткострокових результатів — почати з невеликого, але мислити масштабно (реалістичний пріоритетний план дій, що враховує місцеві особливості, є основною задачею);
4) довгостроковий план дій з ПІІК (наприклад, п’ятирічний) є важливим для загальної оцінки впливу заходів з ПІІК.
9. Завдання та необхідні дії для реалізації етапу розробки та виконання плану дій з ПІІК (крок 3), потенційні бар’єри та рішення для їх подолання наведені у додатку 6 до цього Порядку. Бар’єри і рішення на етапі розробки та виконання плану дій з ПІІК розглядаються по кожному із основних компонентів окремо.
10. Показниками виконання кроку 3 є:
1) розроблено план дій;
2) визначені пріоритетні дії для кожного основного компоненту ПІІК, що планується для впровадження;
3) розглянуті потенційні бар’єри та приклади їх усунення;
4) наявні інструменти і ресурси для підтримки в реалізації заходів з ПІІК;
5) розроблено заходи для кожного основного компоненту ПІІК;
6) план дій затверджено керівництвом ЗОЗ;
7) узгоджено графік проведення моніторингу, оцінки та дати перегляду плану дій з ПІІК.
11. Оцінка впливу (крок 4) є критичним етапом для прийняття рішень, залучення підтримки і внесення змін в щорічний план дій з ПІІК.
12. Метою проведення оцінки впливу є збір даних для виявлення дій, які справили позитивний влив, та заходів і ресурсів, що потрібні додатково для досягнення поставлених задач.
13. Оцінка впливу включає в себе оцінювання проведених заходів і визначення їх ефективності.
14. Для моніторингу і оцінки використовуються інструменти/протоколи, які застосовувались на етапі базової оцінки. Такий підхід допомагає визначити, на яких ділянках досягнуто покращення, а на яких — проблеми залишилися.
15. Завдання та необхідні дії для реалізації етапу оцінки впливу (крок 4) наведено у додатку 7 до цього Порядку.
16. Показниками виконання кроку 4 є:
1) розглянуто результати базової оцінки;
2) розглянуто заходи з ПІІК або план дій з ПІІК в цілому;
3) переглянуто план дій з ПІІК на поточний рік;
4) затверджено графік і строки проведення повторних оцінювань (системної самооцінки з ПІІК або/та інших інструментів);
5) завершено проведення повторних оцінювань;
6) результати повторних оцінювань розглянуто і проведено порівняльний аналіз із базовою оцінкою, сформовано відповідні звіти та представлено їх зацікавленим сторонам;
7) розроблено та затверджено новий план дій з ПІІК із урахуванням виявлених проблем та слабких сторін;
8) затверджено графік проведення наступних моніторингових оцінок (не рідше одного разу на рік).
17. Етап формування культури безпеки (крок 5) включає:
1) визначення набутих покращень та проблем, що залишаються, з урахуванням даних, отриманих на попередньому етапі;
2) регулярний перегляд і покращення ПІІК за допомогою нововведень (проекти, програми, кампанії) з метою інституціювання культури ПІІК в ЗОЗ;
3) підтримку налагодженого на попередніх етапах співробітництва із зацікавленими сторонами;
4) додаткове укомплектування ВІК фахівцями, в разі потреби, проведення їх додаткового навчання для гарантування постійної підтримки ПІІК у ЗОЗ;
5) ВІК постійно бере участь у розбудові та підтримці ПІІК, в тому числі надає консультації, розповсюджує новітні дані в області ПІІК, підтримує культуру безпеки в ЗОЗ;
6) створення циклу аналізу і взаємодії, з метою підтримки переваг ПІІК і забезпечення її впровадження у існуючі практики ЗОЗ для сприяння її стійкості та всеохоплюючому впливу.
18. Завдання та необхідні дії для реалізації етапу формування культури безпеки (крок 5), потенційні бар’єри та рішення для їх подолання наведено у додатку 8 до цього Порядку.
19. Показниками виконання цього етапу є:
1) керівництвом ЗОЗ затверджено п’ятирічний (або на більший строк) план дій з ПІІК;
2) керівництвом ЗОЗ затверджений щорічний графік проведення системної самооцінки з ПІІК;
3) керівник ВІК мінімум один раз на рік проводить зустріч із лідерами думок і чемпіонами, виказує їм подяку та заручається їхньою підтримкою на майбутнє;
4) успіхи, що були досягнені за звітний період, розповсюджено серед усіх зацікавлених сторін;
5) ВІК налагодило на постійній основі співпрацю з громадськими об’єднаннями з питань ПІІК.
Генеральний директор Директорату громадського здоров’я
та профілактики захворюваності
І. Руденко
Додаток 1
до Порядку впровадження профілактики інфекцій
та інфекційного контролю в закладах охорони здоров’я,
які надають медичну допомогу в стаціонарних умовах
(пункт 10 розділу I, підпункт 8 пункту 3 розділу II,
підпункт 2 пункту 8 розділу III)
Алгоритм розробки плану дій з ПІІК в ЗОЗ із застосуванням ММС
Компонент ММС |
Короткий опис |
||
Питання |
Відповіді |
План дій |
|
1 |
2 |
3 |
4 |
Зміни в системі |
1. Які інженерні рішення, зміни в матеріально-технічному забезпеченні та людські ресурси необхідні для впровадження ПІІК? |
1. |
1. |
Навчання та підготовка |
1. Кого потрібно навчити? Який метод навчання має використовуватися та як часто мають проходити заняття? |
1. |
1. |
Моніторинг, оцінка та зворотній зв’язок |
1. Як ви можете виявити невиконання або невідповідне виконання пунктів плану дій з ПІІК? Які індикатори можна використати? |
1. |
1. |
Нагадування і комунікація |
1. Яким чином ви будете займатися популяризацією заходів з ПІІК? |
1. |
1. |
Культура безпеки |
1. Чи є підтримка ПІІК в ЗОЗ серед працівників? Наприклад, чи є можливість заохочувати працівників ВІК та чи готові вони бути прикладом для наслідування? |
1. |
1. |
Додаток 2
до Порядку впровадження профілактики інфекцій
та інфекційного контролю в закладах охорони здоров’я,
які надають медичну допомогу в стаціонарних умовах
(пункт 2 розділу II)
Приклади заходів для впровадження основних компонентів ПІІК
I. Приклади заходів для розробки плану дій з ПІІК
Дія/захід |
Відповідальна особа |
Період впровадження (початок і закінчення) |
Бюджет (грн.) |
Індикатор виконання |
Досягнений результат (із коротким описом та датою завершення) |
1 |
2 |
3 |
4 |
5 |
6 |
Призначити керівника ВІК |
Керівник ЗОЗ, начальник відділу кадрів |
Призначено керівника ВІК. |
|||
Розробити і затвердити положення про ВІК та посадові інструкції працівників ВІК відповідно до Положення про ВІК в ЗОЗ, установах/закладах надання соціальних послуг/соціального захисту населення. |
Начальник відділу кадрів |
1 місяць |
Затверджено положення про ВІК та посадові інструкції координатора з гігієни рук, лікаря-епідеміолога, координатора навчання і підготовки з ПІІК, клінічного провізора, статистика та інших працівників ВІК. |
||
Проаналізувати системну самооцінку ПІІК у ЗОЗ і розробити письмовий план дій на певний час роботи (наприклад, річний план) на основі визначених пріоритетів |
Керівництво ЗОЗ, керівник ВІК |
2–3 місяці |
Проведена системна самооцінка ПІІК в ЗОЗ. |
||
Розрахувати і затвердити бюджет для закупівлі офісного обладнання (комп’ютер і програмне забезпечення, телефон, підключення до мережі Інтернет) і запланованих заходів (наприклад, навчальні курси). |
Керівник ЗОЗ, фінансовий відділ, керівник ВІК |
1–3 місяці |
Розраховано, затверджено керівником ЗОЗ бюджет для фінансування закупівлі офісного обладнання і запланованих заходів для потреб ВІК. |
||
Провести зустріч та обговорити ПІІК із керівництвом ЗОЗ, керівниками суміжних програм/служб (наприклад, якості надання медичних послуг). |
Керівник ВІК |
1–2 місяці |
Проведено зустрічі з керівництвом ЗОЗ та керівниками суміжних програм/служб, оговорені і погоджені спільні заходи. |
II. Приклади заходів для розробки і впровадження СОП з ПІІК
Дія/захід |
Відповідальна особа |
Період впровадження (початок і закінчення) |
Бюджет (грн.) |
Індикатор виконання |
Досягнений результат (із коротким описом та датою завершення) |
1 |
2 |
3 |
4 |
5 |
6 |
Розробити/адаптувати і затвердити СОП |
Керівник ВІК |
6–12 місяців |
Розроблені/адаптовані і затверджені керівником ЗОЗ наступні СОП: |
||
Переглянути наявні СОП (доповнити їх положеннями з ПІІК) |
Керівник ВІК, керівники структурних підрозділів ЗОЗ |
3–12 місяців |
Проведено зустрічі з керівниками структурних підрозділів ЗОЗ. |
||
Організувати співпрацю із громадськими або професійними об’єднаннями в сфері ПІІК для забезпечення підтримкою ЗОЗ з ПІІК (наприклад, шляхом дистанційного наставництва або телефонних консультацій). |
Керівник ЗОЗ, керівник ВІК |
1–6 місяців |
Заключено договір або підписано меморандум про співпрацю з громадським або професійним об’єднанням в сфері ПІІК. |
III. Приклади заходів з навчання і підготовки з ПІІК
Дія/захід |
Відповідальна особа |
Період впровадження (початок і закінчення) |
Бюджет (грн.) |
Індикатор виконання |
Досягнений результат (із коротким описом та датою завершення) |
1 |
2 |
3 |
4 |
5 |
6 |
Визначити координатора навчання і підготовки з ПІІК |
Керівник ВІК |
Визначено координатора навчання і підготовки з ПІІК або запрошено зовнішнього консультанта для проведення навчання і підготовки з ПІІК. |
|||
Розробити і затвердити програму навчання і підготовки з ПІІК для працівників ЗОЗ |
Координатор навчання і підготовки з ПІІК, керівник ВІК, керівники структурних підрозділів ЗОЗ, керівник ЗОЗ |
3–12 місяців |
Розроблено і затверджено керівником ЗОЗ програму навчання і підготовки з ПІІК для працівників ЗОЗ. |
||
Розрахувати і затвердити бюджет для закупівлі необхідного обладнання і витратних матеріалів для забезпечення програми навчання і підготовки з ПІІК |
Координатор навчання і підготовки з ПІІК, керівник ВІК, фінансовий відділ, керівник ЗОЗ |
1–3 місяці |
Розраховано, затверджено керівником ЗОЗ бюджет для закупівлі необхідного обладнання і витратних матеріалів для забезпечення програми навчання і підготовки з ПІІК. |
||
Розробити і затвердити графік навчання і підготовки з ПІІК для працівників ЗОЗ |
Координатор навчання і підготовки з ПІІК, керівник ВІК, керівники структурних підрозділів ЗОЗ, керівник ЗОЗ |
1–2 місяці |
Розроблено і затверджено керівником ЗОЗ графік навчання і підготовки з ПІІК для працівників ЗОЗ. |
||
Розробити і затвердити чек-листи (контрольні списки, анкети) перевірки знань і практичних навичок з ПІІК працівників ЗОЗ |
Координатор навчання і підготовки з ПІІК, керівник ВІК, керівник ЗОЗ |
3–12 місяців |
Розроблено і затверджено керівником ЗОЗ чек-листи (контрольні списки, анкети) перевірки знань і практичних навичок з ПІІК працівників ЗОЗ. |
||
Розробити і затвердити чек-листи (контрольні списки, анкети) перевірки якості проведених навчання і підготовки (оцінка працівниками координатора навчання і підготовки з ПІІК) |
Керівник ВІК, керівник ЗОЗ |
1–3 місяці |
Розроблено і затверджено керівником ЗОЗ чек-листи (контрольні списки, анкети) перевірки якості проведених навчання і підготовки. |
||
Розробити і затвердити систему допуску працівників до виконання професійних обов’язків залежно від пройдених навчання і підготовки з ПІІК (отриманих результатів перевірки знань і практичних навичок) |
Координатор навчання і підготовки з ПІІК, керівник ВІК, начальник відділу кадрів, керівники структурних підрозділів ЗОЗ, керівник ЗОЗ |
3–6 місяців |
Розроблено і затверджено керівником ЗОЗ систему допуску працівників до виконання професійних обов’язків залежно від пройдених навчання і підготовки з ПІІК (наприклад, недопущення сестер медичних до постановки периферійних венозних катетерів без проходження відповідних навчання, підготовки і перевірки знань). |
||
Розробити і затвердити систему зовнішнього моніторингу для оцінки знань і практичних навичок з ПІІК у працівників ЗОЗ |
Керівник ВІК, керівник ЗОЗ |
3–12 місяців |
Заключено договір або підписано меморандум про співпрацю з громадським або професійним об’єднанням в сфері ПІІК для проведення моніторингу та/або залучено зовнішнього консультанта та/або заключено договір щодо проведення перехресного моніторингу з іншим ЗОЗ для оцінки знань і практичних навичок з ПІІК у працівників ЗОЗ. |
||
Розробити і затвердити програму навчання і підготовки з ПІІК для пацієнтів та членів їх родин |
Координатор навчання і підготовки з ПІІК, керівник ВІК, керівники клінічних структурних підрозділів ЗОЗ, керівник ЗОЗ |
3–12 місяців |
Розроблено і затверджено керівником ЗОЗ програму навчання і підготовки з ПІІК для пацієнтів та членів їх родин. |
||
Розрахувати і затвердити бюджет для розробки макетів і закупівлі пам’яток для пацієнтів та членів їх родин |
Координатор навчання і підготовки з ПІІК, керівник ВІК, керівники клінічних структурних підрозділів ЗОЗ, фінансовий відділ, керівник ЗОЗ |
1–3 місяці |
Розроблено і затверджено керівником ЗОЗ макети пам’яток для пацієнтів та членів їх родин. |
||
Визначити потребу в додаткових навчанні і підготовці з ПІІК працівників ЗОЗ та провести його |
Керівник ВІК, начальник відділу кадрів, фінансовий відділ (за необхідності), керівник ЗОЗ |
1–3 місяці |
Визначено потребу в додаткових навчанні і підготовці з ПІІК працівників ЗОЗ. |
IV. Приклади заходів з епідеміологічного нагляду за ІПНМД
Дія/захід |
Відповідальна особа |
Період впровадження (початок і закінчення) |
Бюджет (грн.) |
Індикатор виконання |
Досягнений результат (із коротким описом та датою завершення) |
1 |
2 |
3 |
4 |
5 |
6 |
Прийняти на роботу лікаря-епідеміолога ВІК (в тому числі шляхом перепрофілювання іншої посади) |
Керівник ВІК |
1–12 місяців |
Прийнято на роботу лікаря-епідеміолога ВІК. |
||
Прийняти на роботу помічника(ів) лікаря-епідеміолога ВІК (за необхідності) |
Лікар-епідеміолог ВІК, керівник ВІК |
1–12 місяців |
Прийнято на роботу помічника(ів) лікаря-епідеміолога ВІК (з розрахунку один помічник лікаря-епідеміолога на кожні 250 ліжок ЗОЗ). |
||
Визначити ресурси (кадрові і фінансові), які необхідні для проведення епідеміологічного нагляду в ЗОЗ |
Лікар-епідеміолог ВІК, завідувач мікробіологічної лабораторії (за наявності), керівник ВІК, начальник відділу кадрів, фінансовий відділ, керівник ЗОЗ |
1–3 місяці |
Визначено ресурси (кадрові і фінансові), які необхідні для впровадження в мікробіологічній лабораторії методології EUCAST. |
||
Розрахувати і затвердити бюджет для впровадження в мікробіологічній лабораторії методики EUCAST (за наявності лабораторії) |
Завідувач мікробіологічної лабораторії, лікар-епідеміолог ВІК, фінансовий відділ, керівник ЗОЗ |
1–3 місяці |
Розраховано, затверджено керівником ЗОЗ бюджет для закупівлі необхідного обладнання і витратних матеріалів для впровадження в мікробіологічній лабораторії методики EUCAST. |
||
Розробити і затвердити СОП із забору, зберігання і транспортування зразків біологічних матеріалів для проведення мікробіологічних (бактеріологічних) досліджень |
Завідувач мікробіологічної лабораторії, лікар-епідеміолог ВІК, координатор навчання і підготовки з ПІІК, керівник ВІК, керівники клінічних структурних підрозділів ЗОЗ, керівник ЗОЗ |
3–6 місяців |
Розроблені і затверджені керівником ЗОЗ СОП із забору, зберігання і транспортування зразків біологічних матеріалів для проведення мікробіологічних (бактеріологічних) досліджень. |
||
Провести пілотне визначення розповсюдженості інфекційних хвороб, пов’язаних з наданням медичної допомоги (наприклад, інфекцій області хірургічного втручання) |
Лікар-епідеміолог ВІК, керівник ВІК |
2–6 місяців |
Проведено пілотне визначення розповсюдженості інфекцій області хірургічного втручання. |
||
Впровадити епідеміологічний нагляд за інфекціями області хірургічного втручання |
Лікар-епідеміолог ВІК, керівник ВІК |
3–6 місяців |
Впроваджено епідеміологічний нагляд за інфекціями області хірургічного втручання. |
||
Впровадити епідеміологічний нагляд за девайс-асоційованими інфекційними хворобами, пов’язаними з наданням медичної допомоги |
Лікар-епідеміолог ВІК, керівник ВІК |
6–24 місяців |
Впроваджено епідеміологічний нагляд за вентилятор-асоційованими пневмоніями, катетер-асоційованими інфекціями кровотоку (периферичний венозний та центральні внутрішньосудинні катетери), катетер-асоційованими інфекціями сечовивідних шляхів. |
||
Впровадити епідеміологічний нагляд за бактеріями з множинною та панрезистентністю до антибактеріальних препаратів |
Лікар-епідеміолог ВІК, керівник ВІК |
6–12 місяців |
Впроваджено епідеміологічний нагляд за бактеріями з множинною та панрезистентністю до антибактеріальних препаратів. |
V. Приклади заходів з моніторингу, оцінки і зворотного зв’язку
Дія/захід |
Відповідальна особа |
Період впровадження (початок і закінчення) |
Бюджет (грн.) |
Індикатор виконання |
Досягнений результат (із коротким описом та датою завершення) |
1 |
2 |
3 |
4 |
5 |
6 |
Розрахувати і затвердити бюджет для впровадження в ЗОЗ моніторингу, оцінки і зворотного зв’язку |
Керівник ВІК, статистик ВІК, фінансовий відділ, керівники структурних підрозділів ЗОЗ, керівник ЗОЗ |
1–3 місяці |
Визначити метод(и), що будуть використовуватися, і дані, які будуть аналізуватися, при проведенні моніторингу і оцінки. |
||
Розробити і затвердити чек-листи (контрольні списки, алгоритми) для проведення моніторингу і оцінки |
Керівник ВІК, статистик ВІК, керівники структурних підрозділів ЗОЗ, керівник ЗОЗ |
3–6 місяців |
Розроблені і затверджені керівником ЗОЗ чек-листи (контрольні списки, алгоритми) для проведення моніторингу і оцінки. |
||
Розробити і затвердити графік проведення моніторингу і оцінки |
Керівник ВІК, статистик ВІК, керівники структурних підрозділів ЗОЗ, керівник ЗОЗ |
1–2 місяці |
Розроблений і затверджений керівником ЗОЗ графік проведення моніторингу і оцінки. |
||
Розробити і затвердити графік проведення зворотного зв’язку |
Керівник ВІК, статистик ВІК, керівники структурних підрозділів ЗОЗ, керівник ЗОЗ |
1–2 місяці |
Розроблений і затверджений керівником ЗОЗ графік проведення зворотного зв’язку |
VI. Приклади заходів з режиму роботи, штатного розпису і навантаження на ліжко
Дія/захід |
Відповідальна особа |
Період впровадження (початок і закінчення) |
Бюджет (грн.) |
Індикатор виконання |
Досягнений результат (із коротким описом та датою завершення) |
Розрахувати необхідну кількість працівників відповідно до посадових обов’язків і робочого навантаження |
Начальник відділу кадрів, керівники структурних підрозділів ЗОЗ, медичний директор (начмед) ЗОЗ, медичний директор з медсестринства (головна медична сестра) ЗОЗ, керівник ЗОЗ, керівник ВІК (як консультант) |
3–6 місяців |
Проведено розрахунок необхідної кількості працівників в структурних підрозділах ЗОЗ відповідно до посадових обов’язків і робочого навантаження. |
||
Дотримання правила «один пацієнт на одне ліжко» |
Медичний директор (начмед) ЗОЗ, медичний директор з медсестринства (головна медична сестра) ЗОЗ, керівники клінічних структурних підрозділів ЗОЗ, керівник ЗОЗ, керівник ВІК (як консультант) |
6–24 місяців |
Проведено аналіз причин недотримання правила «один пацієнт на одне ліжко». |
VII. Приклади заходів: приміщення, матеріали і обладнання
Дія/захід |
Відповідальна особа |
Період впровадження (початок і закінчення) |
Бюджет (грн.) |
Індикатор виконання |
Досягнений результат (із коротким описом та датою завершення) |
1 |
2 |
3 |
4 |
5 |
6 |
Вирішити проблему водопостачання (вода для гігієни рук, пиття, особистої гігієни, надання медичної допомоги, стерилізації, дезактивації, прибирання і прання недоступна або поганої якості) |
Заступник керівника з технічних питань, керівник ЗОЗ, керівник ВІК (як консультант) |
3–24 місяці |
Зроблено відбір зразків води та проведено аналіз якості води. |
||
Впровадити реєстрацію проведених прибирань |
Медичний директор з медсестринства (головна медична сестра) ЗОЗ, керівник ЗОЗ, керівник ВІК (як консультант) |
1–3 місяці |
Впроваджено чек-листи реєстрації поточних і генеральних прибирань в структурних підрозділах ЗОЗ. |
||
Обладнати палати ізоляції пацієнтів в ЗОЗ |
Заступник керівника з технічних питань, фінансовий відділ, керівник ЗОЗ, керівник ВІК (як консультант) |
12–60 місяців |
Визначені та приведені у відповідність до вимог інфекційного контролю приміщення для ізоляції пацієнтів, які інфіковані/колонізовані мікроорганізмами з множинною або панрезистентністю. |
||
Обладнати вентиляційні системи в ЗОЗ |
Заступник керівника з технічних питань, фінансовий відділ, керівник ЗОЗ, керівник ВІК (як консультант) |
24–60 місяців |
Визначені приміщення, які першочергово потребують механічної вентиляції (наприклад, операційні, палати для ізоляції пацієнтів з аерогенними інфекціями, приміщення відділення невідкладної медичної допомоги). |
||
Забезпечити ЗОЗ обладнанням для прибирання |
Медичний директор з медсестринства (головна медична сестра) ЗОЗ, фінансовий відділ, керівник ЗОЗ, керівник ВІК (як консультант) |
6–24 місяці |
Клінічні структурні підрозділи ЗОЗ забезпечені візками для прибирання та витратними матеріалами. |
||
Забезпечити ЗОЗ ємностями для збирання і транспортування медичних відходів |
Заступник керівника з технічних питань, відповідальна особа за поводження з відходами в ЗОЗ, фінансовий відділ, керівник ЗОЗ, керівник ВІК (як консультант) |
3 — 12 місяців |
Клінічні структурні підрозділи ЗОЗ забезпечені контейнерами для збирання особливо небезпечних гострих відходів категорії В. |
VIII. Приклади заходів для застосування мультимодальної стратегії з впровадження ПІІК
Дія/захід |
Відповідальна особа |
Період впровадження (початок і закінчення) |
Бюджет (грн.) |
Індикатор виконання |
Досягнений результат (із коротким описом та датою завершення) |
Впровадження ПІІК в ЗОЗ базується на мультимодальній стратегії |
Керівник ВІК |
постійно |
Розроблені та проведені навчальні заходи із працівниками (з обов’язковим залученням керівництва ЗОЗ) щодо необхідності ММС. |
||
Дії/заходи планів дій з ПІІК враховують всі компоненти ММС |
Керівник ВІК |
постійно |
При розробці / внесенні змін в плани дій з ПІІК (річний і довгостроковий) враховуються всі компоненти ММС. |
||
Актуалізація ММС під час засідань в ЗОЗ з ПІІК |
Керівник ВІК |
постійно |
За результатами засідань, на яких розглядаються питання ПІІК, ухвалені рішення направлені на системні зміни, що включають навчання, моніторинг, промоцію ПІІК та зміну поведінки працівників ЗОЗ, які сприяють формуванню культури безпеки. |
Додаток 3
до Порядку впровадження профілактики інфекцій
та інфекційного контролю в закладах охорони здоров’я,
які надають медичну допомогу в стаціонарних умовах
(пункт 2 розділу III)
Реалізація підготовчого етапу (крок 1) впровадження ПІІК в ЗОЗ
1. Завдання та необхідні дії
Завдання |
Необхідні дії |
1 |
2 |
1. ВІК популяризує та впроваджує ПІІК |
1. Визначити не менше однієї компетентної особи (керівник ВІК) та надати їй повноваження щодо керування процесом впровадження ПІІК. |
2. Взаємодія із зацікавленими сторонами |
1. Виявити у ЗОЗ зацікавлені сторони, особливу увагу приділити виявленню потенційних чемпіонів і лідерів думок. |
3. Виділення бюджету |
1. Розробити обґрунтування бюджету ПІІК для керівництва ЗОЗ. |
4. Міждисциплінарна співпраця |
1. Провести зустрічі із працівниками ЗОЗ, відповідальними за підвищення якості медичних послуг, акредитацію та ліцензування, на яких продемонструвати переваги включення ПІІК для досягнення їхніх цілей. Впровадити та закріпити співпрацю для взаємних результатів. |
5. ПІІК розглядається як найважливіший фактор для успішного функціонування ЗОЗ |
1. Зміни, що необхідні для покращення ПІІК, встановлюються послідовно та із визначенням термінів. |
2. Потенційні бар’єри та рішення для їх подолання
Потенційний бар’єр |
Потенційні рішення |
Приклади реалізації |
1 |
2 |
3 |
ПІІК не на часі в ЗОЗ |
1. Проілюструвати факти спалахів ІПНМД в ЗОЗ та які недоліки в ПІІК сприяли їм. |
1. Забезпечення пріоритету ПІІК за допомогою створення бази даних: |
Відсутність лідерів думки |
1. Почати впровадження ПІІК з пошуку лідерів думки (рекомендовано залучати не тільки лікарів та керівників, але й сестер медичних). |
1. Винайдення лідерів думки шляхом навчання та підготовки. |
Недостатність досвіду впровадження ПІІК |
1. Визначити, яким чином можливо посилити потенціал ВІК (у тому числі проведення навчання закордоном та/або онлайн-навчання). |
Використати покроковий підхід у підготовці кадрового ресурсу. |
Обмежені фінансові ресурси |
Визначити, розглянути та затвердити фінансування заходів з ПІІК. |
Приклад. Використати покроковий підхід у фінансуванні заходів з ПІІК |
3. Примірна схема доповіді щодо стану ПІІК у ЗОЗ
1. ПІІК сприяє зниженню поширення АМР, захищає матерів та новонароджених від інфекцій, включаючи сепсис, та захищає всіх пацієнтів від шкоди та смертей, яких можна уникнути. Ефективна ПІІК буде досягнута лише у випадку розробки та впровадження плану дій, що відповідає цьому Порядку. Реалізація плану дій з ПІІК допоможе заощадити кошти, шляхом уникнення додаткового лікування та збільшення тривалості перебування на ліжку через ІПНМД, а також підвищить якість надання медичних послуг. Впровадження плану дій з ПІІК у співробітництві та координації із іншими програмами, які стосуються якості медичних послуг та інфекційної безпеки, відіграє критичну роль.
Додайте інформацію про заходи з ПІІК, які були запроваджені в ЗОЗ та дані про ІПНМД. Застосовуйте фото, статистичні дані, виписки із медичних карт стаціонарних хворих тощо.
2. Наявність плану дій з ПІІК — необхідна, але недостатня умова на шляху досягнення безпечної високоякісної медичної допомоги в ЗОЗ. Крім того, нам потрібно забезпечити належне внутрішнє середовище в ЗОЗ (інфраструктура, матеріали та обладнання, зайнятість та розміщення ліжок, кадрове забезпечення у відповідності до робочого навантаження) як основу для реалізації всіх інших основних компонентів ПІІК.
Додайте інформацію про нинішню ситуацію в ЗОЗ та необхідні зміни для досягнення кінцевої мети.
3. Ці дві передумови (тобто, план дій з ПІІК, що включає людський ресурс, та належне внутрішнє середовище) сприяють ефективному впровадженню СОП з ПІІК, навчанню та підготовці медичних працівників, моніторингу, оцінці, зворотному зв’язку та епідеміологічного нагляду за ІПНМД/АМР. Однак, нам необхідні кваліфіковані координатори та чемпіони в ВІК для опрацювання та розробки цих заходів.
Додайте інформацію щодо СОП, навчання і підготовки, моніторингу, оцінки та зворотного зв’язку, які реалізовані в ЗОЗ (якщо вони є).
4. Успіх реалізації будь-яких зусиль з покращення ПІІК також залежить від застосування мультимодальної стратегії, що складається з декількох компонентів інтегрованих між собою з метою поліпшення результатів лікування пацієнтів та зміни поведінки працівників ЗОЗ (усвідомлення необхідності культури безпеки). Ваша підтримка допоможе ЗОЗ покращити ПІІК та впровадити її основні компоненти. Це підвищить якість та інфекційну безпеку, розширить можливості в протидії загрозам спалахів хвороб, зупинить розповсюдження АМР та зменшить витрати на лікування пацієнтів.
Додайте інформацію про стратегії, які використовувалися раніше з якості надання медичних послуг та інфекційної безпеки в ЗОЗ. Зробіть акцент на перевагах ММС над унімодальними стратегіями.
Додаток 4
до Порядок впровадження профілактики інфекцій
та інфекційного контролю в закладах охорони здоров’я,
які надають медичну допомогу в стаціонарних умовах
(пункт 5 розділу III, підпункт 8 пункту 7 розділу III)
Протокол системної самооцінки ПІІК в ЗОЗ
I. Вступна частина
1. Системна самооцінка ПІІК в ЗОЗ проводиться відповідно до цього Протоколу з метою оцінки поточної ситуації впровадження в ЗОЗ основних компонентів ПІІК в контексті мультимодальної стратегії (далі — ММС) та є діагностичним інструментом для визначення сильних та слабких сторін по кожному основному компоненту ПІІК.
2. Цей Протокол включає:
1) опитувальник щодо реалізації основних компонентів ПІІК та ММС відповідно до розділів «План дій/заходи з профілактики інфекцій та інфекційного контролю», «СОП з профілактики інфекцій та інфекційного контролю», «Навчання і підготовка з профілактики інфекцій та інфекційного контролю», «Епіднагляд за інфекційними хворобами, пов’язаними з наданням медичної допомоги», «Моніторинг, оцінка та зворотній зв’язок», «Режим роботи, штатний розпис та навантаження на ліжко», «Приміщення, матеріали та обладнання», «Мультимодальна стратегія впровадження ПІІК», «Компонент інфекційного контролю за туберкульозом (лише для закладів, що надають стаціонарну допомогу хворим на туберкульоз)»;
2) таблицю результатів оцінки;
3) таблицю інтерпретації результатів оцінки — визначення рівня ПІІК у ЗОЗ;
4) рекомендації щодо підготовки звіту.
3. Оцінка здійснюється по кожному з питань у відповідному розділі та у підсумку по кожному з розділів по кількості балів, зазначених у колонці «Оцінка (балів)». Загальна сума балів по всіх розділах порівнюється із значеннями загальної суми балів для визначення рівня ПІІК. Визначений рівень ПІІК використовується для проведення відповідних заходів з ПІІК.
II. Опитувальник щодо реалізації основних компонентів ПІІК та ММС
План дій / заходи з профілактики інфекцій та інфекційного контролю |
|||
№ з/п |
Питання |
Відповідь |
Оцінка (балів) |
1 |
2 |
3 |
4 |
1 |
Чи має ЗОЗ затверджений план дій/заходи з ПІІК? |
Ні |
0 |
Так, фінансування із загального фонду видатків |
5 |
||
Так, з окремо виділеним бюджетом |
10 |
||
2 |
Чи підтримуються заходи з ПІІК ВІК? |
Ні |
0 |
ВІК відсутній або є лише один фахівець |
5 |
||
Так |
10 |
||
3 |
Чи входить до складу ВІК хоча б один фахівець з ІК з повною зайнятістю або лікар/медсестра, які виконують функції ІК на повну ставку? |
Ні |
0 |
Ні, наявний фахівець з ІК на неповну ставку |
2,5 |
||
Так, з розрахунку один фахівець на > 250 ліжок |
5 |
||
Так, з розрахунку один фахівець на <= 250 ліжок |
10 |
||
4 |
Чи мають працівники ВІК/фахівець з ІК спеціально відведений час для заходів з ПІІК? |
Ні |
0 |
Так |
10 |
||
5 |
Чи входять до ВІК лікарі та медичні сестри? |
Ні |
0 |
Так |
10 |
||
6 |
Чи наявна міждисциплінарна робоча група з ПІІК в закладі, яка співпрацює та підтримує ВІК)? |
Ні |
0 |
Так |
10 |
||
7 |
Чи входить до міждисциплінарної робочої групи з ПІІК керівництво закладу? |
Ні |
0 |
Так |
5 |
||
8 |
Чи входять до міждисциплінарної робочої групи з ПІІК керівники структурних підрозділів та старші медичні сестри? |
Ні |
0 |
Так |
2,5 |
||
9 |
Чи входять до міждисциплінарної робочої групи з ПІІК інженери з охорони праці, фахівці задіяні у безпеці та біобезпеці закладу, фахівці з оцінки якості надання медичних послуг тощо? |
Ні |
0 |
Так |
2,5 |
||
10 |
Чи наявні чітко визначені заходи та індикатори з ПІІК? |
Ні |
0 |
Так, визначені тільки заходи |
2,5 |
||
Так, визначені заходи та індикатори їх виконання |
10 |
||
11 |
Чи демонструє керівництво ЗОЗ підтримку заходів ПІІК шляхом виділення коштів? |
Ні |
0 |
Так |
5 |
||
12 |
Чи демонструє керівництво ЗОЗ підтримку заходів з ПІІК (наприклад, на оперативних нарадах, круглих столах, нарадах по захворюваності та смертності)? |
Ні |
0 |
Так |
5 |
||
13 |
Чи має ЗОЗ мікробіологічну лабораторію, яка надає щоденну підтримку ВІК? |
Ні |
0 |
Так, але результати надаються з затримкою/недостатньої якості |
5 |
||
Так, результати надаються вчасно/задовільної якості |
10 |
||
Сума балів оцінки по розділу «План дій/заходи з профілактики інфекцій та інфекційного контролю» |
|||
СОП з профілактики інфекцій та інфекційного контролю |
|||
1 |
Чи має ЗОЗ фахівців (з ПІІК, інфекційних хвороб) з достатнім рівнем знань для створення/адаптації СОП? |
Ні |
0 |
Так |
7,5 |
||
2 |
Чи є у закладі СОП щодо: |
||
Стандартних заходів захисту, окрім гігієни рук (використання медичних (хірургічних) масок, медичних рукавичок, халатів захисних від інфекційних агентів, захисних окулярів або щитків відповідно до методів надання медичної допомоги, респіраторна гігієна і гігієна/етикет кашлю, безпека при виконанні ін’єкцій, використання чистих і безпечних білизни, обладнання та інструментарію для надання медичної допомоги, безпечне поводження з медичними відходами, очищення приміщень) |
Ні |
0 |
|
Так |
10 |
||
Гігієни рук |
Ні |
0 |
|
Так |
2,5 |
||
Заходів захисту, що направлені на унеможливлення передавання інфекцій / засновані на шляхах інфікування |
Ні |
0 |
|
Так |
2,5 |
||
Заходів щодо виявлення та боротьби зі спалахами |
Ні |
0 |
|
Так |
2,5 |
||
Профілактики інфекцій області хірургічного втручання |
Ні |
0 |
|
Так |
2,5 |
||
Профілактики катетер-асоційованих інфекцій кровотоку |
Ні |
0 |
|
Так |
2,5 |
||
Профілактики нозокоміальних пневмоній, в тому числі вентилятор-асоційованих |
Ні |
0 |
|
Так |
2,5 |
||
Профілактики катетер-асоційованих інфекцій сечовивідних шляхів |
Ні |
0 |
|
Так |
2,5 |
||
Профілактики передавання мікроорганізмів із множинною резистентністю до антимікробних препаратів |
Ні |
0 |
|
Так |
2,5 |
||
Очищення, дезінфекції та стерилізації (репроцесингу) медичного інструментарію/обладнання |
Ні |
0 |
|
Так |
2,5 |
||
Раціонального використання антимікробних препаратів |
Ні |
0 |
|
Так |
2,5 |
||
3 |
Чи узгоджуються СОП у вашому закладі з національними/міжнародними керівництвами? |
Ні |
0 |
Так |
10 |
||
4 |
Чи відповідають СОП потребам вашого закладу та наявним ресурсам? |
Ні |
0 |
Так |
10 |
||
5 |
Чи залучені медичні працівники, які безпосередньо надають допомогу хворим, у розробку та впровадження СОП? |
Ні |
0 |
Так |
10 |
||
6 |
Чи залучені зацікавлені сторони (завідувачі відділень, старші медичні сестри, керівництво тощо, окрім фахівців ВІК) у розробку та адаптацію СОП? |
Ні |
0 |
Так |
7,5 |
||
7 |
Чи відбуваються тренінги стосовно впровадження нових СОП у закладі? |
Ні |
0 |
Так |
10 |
||
8 |
Чи проводиться регулярний моніторинг впровадження СОП з ПІІК? |
Ні |
0 |
Так |
10 |
||
Сума балів оцінки по розділу «СОП з профілактики інфекцій та інфекційного контролю» |
|||
Навчання і підготовка з профілактики інфекцій та інфекційного контролю |
|||
1 |
Чи наявні працівники з належним рівнем знань в профілактиці інфекцій та інфекційному контролі для проведення заходів з навчання і підготовки? |
Ні |
0 |
Так |
10 |
||
2 |
Чи наявні співробітники (не працівники ВІК) які мають належний рівень знань для проведення заходів з навчання і підготовки? |
Ні |
0 |
Так |
10 |
||
3 |
Як часто медичні працівники проходять навчання і підготовку з питань ПІІК? |
Ніколи або зрідка |
0 |
Тільки для нових медичних працівників під час прийому на роботу або випробувального терміну |
5 |
||
Для нових медичних працівників та щонайменше щорічно для усіх медичних працівників (навчання і підготовка не обов’язкові) |
10 |
||
Для нових медичних працівників та щонайменше щорічно для усіх працівників (навчання і підготовка обов’язкові) |
15 |
||
4 |
Як часто молодші медичні працівники/помічники сестер медичних та інший допоміжний персонал проходить навчання і підготовку з питань ПІІК? |
Ніколи або зрідка |
0 |
Тільки для нових співробітників |
5 |
||
Для нових працівників та щонайменше щорічно для усіх працівників (навчання і підготовка не обов’язкові) |
10 |
||
Для нових працівників та щонайменше щорічно для усіх працівників (навчання і підготовка обов’язкові) |
15 |
||
5 |
Чи проходять загальні навчальні сесії з ПІІК для керівництва ЗОЗ? |
Ні |
0 |
Так |
5 |
||
6 |
У якій формі проходять навчання і підготовка для працівників? |
Навчання і підготовка відсутні |
0 |
Використовується тільки довідникова інформація, усні настанови, електронні ресурси |
5 |
||
Запроваджені інтерактивні/симуляційні тренінги, навчання біля ліжка хворого |
10 |
||
7 |
Чи наявна періодична оцінка ефективності навчання і підготовки (наприклад, дотримання правил і практик з гігієни рук)? |
Ні |
0 |
Так, але нерегулярно |
5 |
||
Так, регулярно (щонайменше щорічно) |
10 |
||
8 |
Чи інтегровані навчання і підготовка з ПІІК у навчання за іншими напрямами (наприклад, проведення догляду за пацієнтами, надання медичної допомоги відповідно до патології)? |
Ні |
0 |
Так, деякі напрями навчання |
5 |
||
Так, усі напрями навчання |
10 |
||
9 |
Чи існують спеціальні навчання і підготовка з ПІІК для пацієнтів та їх родин? |
Ні |
0 |
Так |
5 |
||
10 |
Чи проходить постійне навчання працівників з питань ПІІК (шляхом відвідування конференцій, курсів, семінарів тощо)? |
Ні |
0 |
Так |
10 |
||
Сума балів оцінки по розділу «Навчання і підготовка з профілактики інфекцій та інфекційного контролю» |
|||
Епіднагляд за інфекційними хворобами, пов’язаними з наданням медичної допомоги |
|||
1 |
Чи впроваджено епіднагляд за ІПНМД у закладі? |
Ні |
0 |
Так |
5 |
||
2 |
Чи наявні працівники, які здійснюють епіднагляд у закладі? |
Ні |
0 |
Так |
5 |
||
3 |
Чи працівники відповідальні за епіднагляд проходили відповідне навчання з епідеміології та ПІІК? |
Ні |
0 |
Так |
5 |
||
4 |
Чи має заклад електронні інструменти (програмне забезпечення) для епіднагляду (наприклад, електронне ведення медичної документації)? |
Ні |
0 |
Так |
5 |
||
5 |
Чи проводиться пріоритетизація важливості епіднагляду за ІПНМД (враховуючи захворюваність та смертність у закладі)? |
Ні |
0 |
Так |
5 |
||
6 |
Епіднагляд встановлено за: |
||
Інфекціями області хірургічного втручання |
Ні |
0 |
|
Так |
2,5 |
||
Девайс-асоційованими ІПНМД (катетер-асоційовані інфекції сечових шляхів, катетер-асоційовані інфекції кровотоку, вентилятор-асоційовані пневмонії) |
Ні |
0 |
|
Так |
2,5 |
||
Інфекційними захворюваннями, для встановлення яких не обов’язкове використання бактеріологічних методів обстеження (наприклад, пролежні) |
Ні |
0 |
|
Так |
2,5 |
||
Інфекційними захворюваннями (в тому числі колонізацією), що викликані мікроорганізмами із стійкістю до антимікробних препаратів (АМР і МАМР) у відповідності до місцевого контексту |
Ні |
0 |
|
Так |
2,5 |
||
Пріоритетними місцевими інфекціями, що здатні спричинити спалах (захворюваннями викликаними норо- або ротавірусами, вірусами грипу, туберкульозом, тяжким гострим респіраторним синдромом тощо) |
Ні |
0 |
|
Так |
2,5 |
||
Інфекційними захворюваннями серед сприятливих груп населення (новонародженими, пацієнтами відділень інтенсивної терапії, пацієнтами з опіками, ВІЛ-інфікованими тощо) |
Ні |
0 |
|
Так |
2,5 |
||
Інфекційними захворюваннями, що пов’язані із професійною медичною діяльністю (гепатити B і C, ВІЛ, туберкульоз, грип, кір, кашлюк тощо) |
Ні |
0 |
|
Так |
2,5 |
||
7 |
Чи пріоритетизація інфекцій за якими встановлюється епідеміологічний нагляд проводиться регулярно? |
Ні |
0 |
Так |
5 |
||
8 |
Чи використовуєте ви надійні показники/індикатори для епідеміологічного нагляду (чисельник і знаменник відповідають національним/міжнародним визначенням)? |
Ні |
0 |
Так |
5 |
||
9 |
Чи використовуються стандартизовані методи збору інформації для епідеміологічного нагляду? |
Ні |
0 |
Так |
5 |
||
10 |
Чи наявний механізм перевірки якості отриманої інформації (оцінка форм звітності, перегляд результатів мікробіологічної лабораторії, підрахунок знаменника тощо)? |
Ні |
0 |
Так |
5 |
||
11 |
Чи обладнання мікробіологічної лабораторії достатнє для забезпечення епідеміологічного нагляду? |
Ні |
0 |
Так, можливе розрізнення на Грам+/- бактерії, ідентифікація неможлива |
2,5 |
||
Так, своєчасна ідентифікація мікроорганізмів |
5 |
||
Так, своєчасна ідентифікація мікроорганізмів та визначення чутливості до антимікробних препаратів |
10 |
||
12 |
Чи використовуються епідеміологічні дані для покращення ПІІК у клінічних структурних підрозділах? |
Ні |
0 |
Так |
5 |
||
13 |
Чи регулярно аналізується локальна антимікробна резистентність мікроорганізмів до антимікробних препаратів у закладі (щонайменше щорічно)? |
Ні |
0 |
Так |
5 |
||
14 |
Чи має ВІК регулярний зворотній зв’язок щодо показників епіднагляду (щонайменше щорічно) з: |
||
Медичними працівниками, які безпосередньо надають медичну допомогу |
Ні |
0 |
|
Так |
2,5 |
||
Завідувачами клінічних структурних підрозділів |
Ні |
0 |
|
Так |
2,5 |
||
Міждисциплінарною робочою групою з ПІІК |
Ні |
0 |
|
Так |
2,5 |
||
Керівництвом ЗОЗ |
Ні |
0 |
|
Так |
2,5 |
||
15 |
Яким чином реалізується зворотній зв’язок? |
Зворотній зв’язок відсутній |
0 |
Наявний в письмовій, усній формі |
2,5 |
||
Наявний у вигляді презентацій |
7,5 |
||
Сума балів оцінки по розділу «Епіднагляд за інфекційними хворобами, пов’язаними з наданням медичної допомоги» |
|||
Моніторинг, оцінка та зворотній зв’язок |
|||
1 |
Чи наявні у вашому закладі працівники, які відповідають за моніторинг та оцінку і мають відповідну підготовку? |
Ні |
0 |
Так |
10 |
||
2 |
Чи існує план моніторингу з визначеними цілями та заходами, включно із визначеними інструментами для систематичного збору даних? |
Ні |
0 |
Так |
7,5 |
||
3 |
Які процеси чи індикатори ви оцінюєте у ЗОЗ? |
Жодного |
0 |
Дотримання працівниками правил і практик гігієни рук |
5 |
||
Постановка та догляд за внутрішньосудинними катетерами |
5 |
||
Догляд за хірургічною раною |
5 |
||
Заходи запобігання (спрямовані на унеможливлення інфікування та ізоляційно-обмежувальні) розповсюдженню мікроорганізмів з множинною резистентністю до антимікробних препаратів |
5 |
||
Прибирання палат |
5 |
||
Очищення, дезінфекція та стерилізація (репроцесинг) медичного інструментарію/обладнання |
5 |
||
Споживання спиртовмісних антисептиків для рук та рідкого мила |
5 |
||
Споживання та використання антимікробних препаратів |
5 |
||
Поводження з відходами |
5 |
||
4 |
Як часто використовується протокол системної самооцінки гігієни рук в ЗОЗ/ЗСЗ? |
Ніколи або рідко |
0 |
Періодично, але нерегулярно |
2,5 |
||
Мінімум щороку |
5 |
||
5 |
Чи здійснюється зворотній зв’язок щодо діяльності ВІК? |
Ні |
0 |
Так, для працівників ВІК |
2,5 |
||
Так, завідувачам клінічних структурних підрозділів |
2,5 |
||
Так, всім медичним працівникам, які безпосередньо надають медичну допомогу |
2,5 |
||
Так, міждисциплінарній робочій групі з ПІІК та фахівцям з оцінки якості надання медичних послуг |
2,5 |
||
Так, керівництву ЗОЗ |
2,5 |
||
6 |
Чи звітування про результати моніторингу проводяться регулярно (щонайменше щорічно)? |
Ні |
0 |
Так |
10 |
||
7 |
Чи здійснюється моніторинг і зворотній зв’язок щодо процесів та показників ПІІК в умовах корпоративної культури, де не шукають винних, а збирають дані з метою формування культури безпеки? |
Ні |
0 |
Так |
5 |
||
8 |
Чи оцінюєте ви показники культури безпеки у вашому закладі? |
Ні |
0 |
Так |
5 |
||
Сума балів оцінки по розділу «Моніторинг, оцінка та зворотній зв’язок» |
|||
Режим роботи, штатний розпис та навантаження на ліжко |
|||
1 |
Чи проводиться оцінка забезпеченості медичними працівниками відповідно до кількості пацієнтів із використанням національних або міжнародних стандартів/інструментів? |
Ні |
0 |
Так |
5 |
||
2 |
Чи підтримується у вашому закладі встановлене (національними або міжнародними стандартами/інструментами) співвідношення між кількістю медичних працівників та кількістю пацієнтів? |
Ні |
0 |
Так, у менше ніж 50 % відділень |
5 |
||
Так, у більше ніж 50 % відділень |
10 |
||
Так, для усіх відділень |
15 |
||
3 |
Чи існує система реагування на результати оцінки кадрових потреб, в разі якщо укомплектованість визнається занадто низькою? |
Ні |
0 |
Так |
10 |
||
4 |
Чи відповідає устрій палат у вашому закладі міжнародним стандартам щодо кількості ліжок? |
Ні |
0 |
Так, у деяких відділеннях |
5 |
||
Так, у всіх відділеннях |
15 |
||
5 |
Чи відповідає зайнятість ліжок у закладі положенню «одне ліжко — один пацієнт»? |
Ні |
0 |
Так, у деяких відділеннях |
5 |
||
Так, у всіх відділеннях |
15 |
||
6 |
Чи розміщуються пацієнти на ліжках, що знаходяться у коридорах клінічних структурних підрозділів або поза зоною пацієнтів у відділенні невідкладної допомоги? |
Так, частіше ніж двічі на тиждень |
0 |
Так, рідше ніж двічі на тиждень |
5 |
||
Ні |
15 |
||
7 |
Чи наявний простір між ліжками пацієнтів, який складає мінімум 1 метр? |
Ні |
0 |
Так, у деяких відділеннях |
5 |
||
Так, у всіх відділеннях |
15 |
||
8 |
Чи існує у вашому закладі система оцінки і реагування на випадки коли кількість пацієнтів перевищує кількість ліжко-місць? |
Ні |
0 |
Так, це входить в обов’язки завідувача відділенням |
5 |
||
Так, це входить в обов’язки керівництва закладу |
15 |
||
Сума балів оцінки по розділу «Режим роботи, штатний розпис та навантаження на ліжко» |
|||
Приміщення, матеріали і обладнання |
|||
№ з/п |
Питання |
Відповідь |
Оцінка (балів) |
1 |
Чи доступне водопостачання в будь-який час і в достатній кількості для всіх видів використання (наприклад, миття рук, пиття, особиста гігієна, медична діяльність, стерилізація, санітарна обробка, прибирання та прання)? |
Ні, доступне менш ніж п’ять днів на тиждень |
0 |
Так, доступне в середньому п’ять днів на тиждень або щодня, але в недостатній кількості |
2,5 |
||
Так, щоденно в достатній кількості |
7,5 |
||
2 |
Чи наявні безпечні джерела питної води для працівників, пацієнтів та їх відвідувачів в будь-який час і у всіх палатах та кімнатах працівників ЗОЗ? |
Ні |
0 |
Інколи або лише в деяких місцях, або не доступні для всіх |
2,5 |
||
Так, доступні в будь-який час для всіх |
7,5 |
||
3 |
Чи наявне облаштування для гігієни рук у всіх точках догляду (тобто наявність диспенсерів із рідким милом, спиртовмісним антисептиком для рук та одноразовими паперовими рушниками (диспенсер закритого типу)? |
Ні |
0 |
Так, але недообладнані |
2,5 |
||
Так |
7,5 |
||
4 |
Туалети у закладі наявні з розрахунку 1 туалет на максимум 20 ліжок в стаціонарі? |
Недостатня кількість туалетів |
0 |
Достатня кількість, але не усі функціонують |
2,5 |
||
Достатня кількість та усі функціонують |
7,5 |
||
5 |
Чи забезпечений ваш заклад достатньою кількістю електроенергії вдень та вночі (для подачі та нагріву води, стерилізації та санітарної обробки, спалювання або інших способів знешкодження відходів, забезпечення роботи медичного обладнання, загального освітлення території закладу, забезпечення безпечного надання медичних послуг, освітлення туалетів та душових)? |
Ні |
0 |
Так, але не завжди або не всюди |
2,5 |
||
Так |
5 |
||
6 |
Чи наявна у вашому закладі система вентиляції (механічна чи природна) в місцях догляду за пацієнтом? |
Ні |
0 |
Так |
5 |
||
7 |
Чи здійснюються письмові відмітки про прибирання підлог та горизонтальних поверхонь (наявність загальнодоступних графіків прибирання із відмітками щодо їх виконання)? |
Графік відсутній |
0 |
Графік наявний, але не заповнюється і не підписується щоденно або застарів |
2,5 |
||
Так, графік наявний та заповнюється щодня |
5 |
||
8 |
Чи наявні відповідні (дозволені/рекомендовані для використання в ЗОЗ), якісні (відповідають національним та міжнародним стандартам) і в належному стані приладдя та засоби для прибирання (швабри, відра, мийні засоби тощо)? |
Ні |
0 |
Так, але в поганому стані |
2,5 |
||
Так |
5 |
||
9 |
Чи має ваш заклад ізолятори/палати індивідуального перебування для пацієнтів із аерогенними інфекційними захворюваннями (наприклад, туберкульоз, кір)? |
Ні |
0 |
Відсутні окремі палати, але наявні палати для групування пацієнтів з однаковими патологіями |
2,5 |
||
Так |
7,5 |
||
10 |
Чи засоби індивідуального захисту доступні для усіх працівників постійно (проведені розрахунки необхідної кількості для кожного з підрозділів та забезпечено фактичну наявність з урахуванням можливої необхідності надання допомоги при надзвичайних ситуаціях)? |
Ні |
0 |
Так, але не завжди наявні в достатній кількості або не забезпечено запасу |
2,5 |
||
Так, завжди наявні в достатній кількості та забезпечено запас |
7,5 |
||
11 |
Чи наявні контейнери для збору інфекційних/неінфекційних відходів та гострих медичних предметів в безпосередній близькості до їх утворення? |
Ні, відсутні окремі контейнери |
0 |
Так, окремі контейнери наявні, але кришки відсутні або контейнери більш як на 3/4 заповнені; наявні лише два контейнери замість трьох; контейнери наявні але не у всіх місцях утворення відходів |
2,5 |
||
Так |
5 |
||
12 |
Чи наявна система муніципального вивезення неінфекційного сміття для утилізації? |
Ні |
0 |
Так, але нерегулярний вивіз відходів |
2,5 |
||
Так |
5 |
||
13 |
Чи наявний інсинератор/муфельна піч або альтернативна технологія для знешкодження або обробки з метою наступного транспортування (наприклад, стерилізація парою), що знаходяться на території закладу або заключено договір із суб’єктом господарювання, який має ліцензію на провадження господарської діяльності з поводження з небезпечними відходами, та чи достатня його/їх потужність? |
Ні |
0 |
Так, але функціонує(ють) неналежним чином |
2,5 |
||
Так |
5 |
||
14 |
Чи існує система менеджменту стічних вод (наприклад, септик із дренажною ямою) в закладі або за його межами? |
Ні |
0 |
Так, але функціонує неналежним чином |
2,5 |
||
Так |
5 |
||
15 |
Чи є у вашому закладі відведена та сертифікована зона/приміщення/підрозділ для репроцесингу медичних виробів та інших предметів/обладнання (наприклад, для прання білизни) або заключено договір із суб’єктом господарювання, який має ліцензію на провадження господарської діяльності з поводження з небезпечними відходами? |
Ні |
0 |
Так, але функціонує неналежним чином |
2,5 |
||
Так |
5 |
||
16 |
Чи завжди у вашому закладі в достатній кількості наявне продезінфіковане та стерильне медичне приладдя/обладнання готове до використання? |
Ні, доступне в середньому менш ніж п’ять днів на тиждень |
0 |
Так, доступне в середньому близько п’яти днів на тиждень або щодня але в недостатній кількості |
2,5 |
||
Так, доступне щоденно і в достатній кількості |
5 |
||
17 |
Чи доступні одноразові медичні вироби за необхідності (наприклад, шприци, системи для внутрішньовенного вливання)? |
Ні |
0 |
Так, але не завжди |
2,5 |
||
Так, доступні постійно |
5 |
||
Сума балів оцінки по розділу «Приміщення, матеріали і обладнання» |
|||
Мультимодальна стратегія впровадження ПІІК |
|||
1 |
Чи використовується мультимодальна стратегія для впровадження ПІІК у вашому ЗОЗ? |
Ні |
0 |
Так |
15 |
||
2 |
Чи включає мультимодальна стратегія заходів з ПІІК у вашому ЗОЗ компонент змін в системі? |
Ні |
0 |
Здійснюються інтервенції для забезпечення наявності необхідної інфраструктури та матеріалів |
5 |
||
Здійснюються інтервенції для забезпечення наявності необхідної інфраструктури та матеріалів з урахуванням ергономічності та доступності |
10 |
||
3 |
Чи включає мультимодальна стратегія заходів з ПІІК у вашому ЗОЗ компонент навчання і підготовки? |
Ні |
0 |
Навчання на основі довідникової інформації, усних рекомендацій, аонних ресурсів |
5 |
||
Навчання проводиться на основі інтерактивних тренінгів, симуляцій біля ліжка хворого, наставництва |
10 |
||
4 |
Чи включає мультимодальна стратегія заходів з ПІІК у вашому закладі компонент моніторингу, оцінки та зворотного зв’язку? |
Ні |
0 |
Моніторинг дотримання процесу або отримання результату (наприклад, дотримання правил і практик гігієни рук, постановки катетера) |
5 |
||
Моніторинг дотримання процесу або отримання результату та своєчасний зворотній зв’язок із медичними працівниками та відповідними зацікавленими сторонами |
10 |
||
5 |
Чи включає мультимодальна стратегія заходів з ПІІК у вашому закладі компонент комунікації та нагадування на робочому місці? |
Ні |
0 |
Наявні нагадування у вигляді інформаційних стендів, плакатів тощо |
5 |
||
Наявні заходи для покращення комунікації (наприклад, зустрічі у загальному та індивідуальному форматах, розбір клінічних випадків) |
10 |
||
6 |
Чи включає мультимодальна стратегія заходів з ПІІК у вашому закладі компонент формування культури безпеки? |
Ні |
0 |
Керівництво закладу та керівники структурних підрозділів підтримують заходи з ПІІК та є прикладами для наслідування |
5 |
||
Додатково, групи і окремі працівники закладу наділені повноваженнями, що дозволяють їм збагнути свою причетність до впроваджуваних заходів (наприклад, участь у круглих столах, розробці/адаптації СОП) |
10 |
||
7 |
Чи укомплектована ВІК повністю відповідно до Положення про відділ з інфекційного контролю в закладах охорони здоров’я та установах / закладах надання соціальних послуг / соціального захисту населення, затвердженого наказом МОЗ України (керівником, епідеміологом, координатором з гігієни рук, координатором навчання і підготовки з ПІІК, клінічним провізором і статистиком)? |
Ні |
0 |
Так |
15 |
||
8 |
Чи приймають участь фахівці з підвищення якості та безпеки надання медичних послуг в розробці та реалізації мультимодальної стратегії заходів з ПІІК? |
Ні |
0 |
Так |
10 |
||
9 |
Чи здійснюється у вашому закладі моніторинг виконання показників етапів впровадження ПІІК? |
Ні |
0 |
Так |
10 |
||
Сума балів оцінки по розділу «Мультимодальна стратегія впровадження ПІІК» |
|||
Компонент інфекційного контролю за туберкульозом |
|||
1 |
Чи наявна можливість проведення швидкої ідентифікації бактеріовиділювачів у закладі? |
Ні |
0 |
Так |
5 |
||
2 |
Протягом якого часу відбувається переведення пацієнтів із МБТ «-» у відділення для хворих без бактеріовиділення або направлення їх на амбулаторне лікування? |
Більше трьох діб |
0 |
До трьох діб |
2,5 |
||
До однієї доби |
5 |
||
3 |
Чи визначені приміщення ЗОЗ по зонам ризику? |
Не визначені |
0 |
Визначені, але відсутні план-схеми у підрозділах |
0 |
||
Визначені, але план-схеми наявні не у всіх підрозділах та/або неналежної якості |
2,5 |
||
Визначені, план-схеми наявні у всіх підрозділах та належної якості |
10 |
||
4 |
Чи наявний розподіл потоків хворих? |
Потоки хворих не розділені |
0 |
Розділені потоки лише для пацієнтів, які госпіталізуються (на приймальному відділенні) |
2,5 |
||
Розділені потоки для пацієнтів, які госпіталізуються; пацієнтів з та без бактеріовиділення |
5 |
||
Розділені потоки для пацієнтів, які госпіталізуються; пацієнтів з та без бактеріовиділення; пацієнтів з МРТБ/РРТБ та пацієнтів, які отримують паліативну допомогу |
10 |
||
5 |
Яка захворюваність на туберкульоз серед працівників за останні три роки? |
Не реєструвалася |
0 |
Відповідає загально національному показнику |
2,5 |
||
Вища за загально національні показники |
5 |
||
6 |
Чи є у вашому закладі СОП щодо: |
||
Проведення якісного фіт-тесту |
Ні |
0 |
|
Так |
2,5 |
||
Правил користування УФ-опромінювачами |
Ні |
0 |
|
Так |
2,5 |
||
Правил збирання зразків мокротиння |
Ні |
0 |
|
Так |
2,5 |
||
Правил транспортування зразків мокротиння до мікробіологічної лабораторії |
Ні |
0 |
|
Так |
2,5 |
||
Порядку дій медичного працівника при виникненні аварійної ситуації, що пов’язана з розливом біологічного матеріалу |
Ні |
0 |
|
Так |
2,5 |
||
Правил використання засобів індивідуального захисту органів дихання (респіраторів) |
Ні |
0 |
|
Так |
2,5 |
||
Правил поведінки пацієнта із кашлем (етикет кашлю) |
Ні |
0 |
|
Так |
2,5 |
||
Розподілу потоку хворих (план-схема або блок-схема) |
Ні |
0 |
|
Так |
2,5 |
||
Порядку оформлення та госпіталізації пацієнта із встановленим діагнозом |
Ні |
0 |
|
Так |
2,5 |
||
Порядку обстеження, оформлення та госпіталізації пацієнта, який не обстежений на догоспітальному етапі або потребує дообстеження |
Ні |
0 |
|
Так |
2,5 |
||
Правил поводження лікаря-бактеріолога під час дослідження культури мікобактерій туберкульозу |
Ні |
0 |
|
Так |
2,5 |
||
Правил посіву біологічного матеріалу |
Ні |
0 |
|
Так |
2,5 |
||
Правил прийому та реєстрації біологічного матеріалу в лабораторії |
Ні |
0 |
|
Так |
2,5 |
||
Процедури реєстрації аварій при виконанні медичних маніпуляцій і нагляду за потерпілими |
Ні |
0 |
|
Так |
2,5 |
||
Заходів попередження професійного зараження |
Ні |
0 |
|
Так |
2,5 |
||
Правил проведення інгаляції пацієнту із туберкульозом легень |
Ні |
0 |
|
Так |
2,5 |
||
Правил транспортування пацієнта на додаткові обстеження в межах закладу та поза ним |
Ні |
0 |
|
Так |
2,5 |
||
Правил видачі лікарських засобів медичною сестрою |
Ні |
0 |
|
Так |
2,5 |
||
Організації хірургічного лікування пацієнтів на туберкульоз |
Ні |
0 |
|
Так |
2,5 |
||
Правил використання масок пацієнтами |
Ні |
0 |
|
Так |
2,5 |
||
7 |
Які види вентиляції використовуються в закладі? |
Не використовується |
0 |
Природна |
5 |
||
Механічна локальна |
7,5 |
||
Механічна загальна |
10 |
||
8 |
Яким чином здійснюється внутрішній контроль за вентиляцією (щонайменше один раз на рік)? |
Не проводиться |
0 |
Проводиться оцінка напряму повітряного потоку |
5 |
||
Проводиться оцінка напряму повітряного потоку та кратності повітрообміну |
10 |
||
9 |
Як часто проводиться оцінка ефективності роботи УФ-ламп за допомогою УФ-радіометра? |
Не проводиться |
0 |
Щонайменше один раз на рік |
2,5 |
||
Щонайменше один раз на шість місяців |
5 |
||
10 |
Як часто проводиться розрахунок потреби в УФ-опромінювачах та УФ-лампах? |
Не проводиться |
0 |
Проводиться з періодичністю в більше як один рік |
2,5 |
||
Проводиться щорічно |
5 |
||
11 |
Яка забезпеченість УФ-опромінювачами та УФ-лампами в зонах високого ризику? |
Менше за 50% або не оцінювалася |
0 |
51–74% |
2,5 |
||
75–99% |
5 |
||
100% |
10 |
||
12 |
Чи проведені розрахунки часу безпечного перебування працівників на робочих місцях де встановлені екрановані УФ-опромінювачі? |
Ні |
0 |
Так |
5 |
||
13 |
Чи наявний у закладі (або заключено договір оренди) комплект для проведення якісного фіт-тесту? |
Ні |
0 |
Так |
5 |
||
14 |
Чи наявна у закладі відповідальна особа, яка пройшла відповідне навчання, за проведення якісного фіт-тестування? |
Ні |
0 |
Так |
5 |
||
15 |
Чи проводиться якісний фіт-тест у закладі? |
Не проводиться |
0 |
Проводиться для працівників, які працюють в зонах високого ризику не рідше одного разу на рік та додатково за потреби |
5 |
||
Проводиться для всіх медичних працівників не рідше одного разу на рік та додатково за потреби |
7,5 |
||
Проводиться для всіх працівників закладу не рідше одного разу на рік та додатково за потреби |
15 |
||
16 |
Як часто проводиться розрахунок потреби в респіраторах? |
Не проводиться |
0 |
Проводиться з періодичністю в більше як один рік |
2,5 |
||
Проводиться раз на рік без врахування індивідуальних особливостей працівників (без врахування проведених якісних фіт-тестувань) |
5 |
||
Проводиться раз на рік із врахуванням індивідуальних особливостей працівників (із врахуванням проведених якісних фіт-тестувань) |
10 |
||
17 |
Яка забезпеченість працівників закладу респіраторами? |
Працівники не забезпечені респіраторами або розрахунки не проводяться |
0 |
Забезпечені всі медичні працівники в зонах високого ризику |
2,5 |
||
Забезпечені всі медичні працівники |
5 |
||
Забезпечені всі працівники закладу |
10 |
||
Забезпечені всі працівники закладу та наявний трьохмісячний запас |
15 |
||
18 |
Яка забезпеченість пацієнтів масками? |
Не забезпечені |
0 |
Забезпечені, але в недостатній кількості |
2,5 |
||
Забезпечені лише пацієнти |
5,0 |
||
Забезпечені пацієнти та їх родичі під час відвідувань |
7,5 |
||
19 |
Який відсоток дотримання пацієнтами правил носіння масок під час проведення оцінювання (в присутності медичних працівників)? |
Не одягають або одягають менше як 75% пацієнтів |
0 |
Одягають, але не закривають ніс або не фіксують обтюратор; одягають після нагадування |
0 |
||
Одягають правильно 75–94% пацієнтів |
2,5 |
||
95% і більше пацієнтів одягають маску правильно |
7,5 |
||
20 |
Чи кімната/майданчик для збору мокротиння облаштовані відповідно до вимог? |
Ні |
0 |
Так |
5 |
||
Сума балів оцінки по розділу "Компонент інфекційного контролю за туберкульозом (лише для закладів, що надають стаціонарну допомогу хворим на туберкульоз) |
|||
III. Таблиця результатів оцінки
Розділ |
Оцінка (балів) |
План дій/заходи з профілактики інфекцій та інфекційного контролю |
|
СОП з профілактики інфекцій та інфекційного контролю |
|
Навчання і підготовка з профілактики інфекцій та інфекційного контролю |
|
Епіднагляд за інфекційними хворобами, пов’язаними з наданням медичної допомоги |
|
Моніторинг, оцінка та зворотній зв’язок |
|
Режим роботи, штатний розпис та навантаження на ліжко |
|
Приміщення, матеріали та обладнання |
|
Мультимодальна стратегія впровадження ПІІК |
|
Компонент інфекційного контролю за туберкульозом (лише для закладів, що надають стаціонарну допомогу хворим на туберкульоз) |
|
Загальна сума балів |
IV. Таблиця інтерпретації результатів оцінки
Загальна сума балів |
Рівень профілактики інфекцій та інфекційного контролю |
0–200 (0–250*) |
Незадовільний |
201–400 (251–500*) |
Базовий |
401–600 (501–750*) |
Середній |
601–800 (751–1000*) |
Достатній |
____________
* лише для закладів, що надають стаціонарну допомогу хворим на туберкульоз.
V. Рекомендації щодо підготовки звіту за результатами оцінки
Звіт за результатами системної самооцінки з ПІІК у ЗОЗ має містити таку інформацію:
1) назву закладу та дату проведення оцінки (число, місяць, рік);
2) прізвище, ім’я та по-батькові (за наявності), посади осіб, які проводили оцінку;
3) рівень ПІІК відповідно до таблиці інтерпретації результатів оцінки, наведеної у розділі IV цього додатку, та загальну суму балів відповідно до таблиці результатів оцінки, наведеної у розділі III цього додатку;
4) резюме щодо успішності впровадження основних компонентів ПІІК у ЗОЗ в залежності від результатів оцінки та затвердженого плану дій/заходів з ПІІК у ЗОЗ;
5) резюме за результатами співставлення прогресу ЗОЗ із впровадження ПІІК:
з попередніми результатами оцінки (у разі проведення);
з положеннями Порядку;
розподіл балів по кожному із основних компонентів ПІІК відповідно до таблиці результатів оцінки, наведеної у розділі III цього додатку;
висновки за результатами аналізу результатів: сильні та слабкі сторони по всім основним компонентам ПІІК та ММС;
рекомендації щодо плану дій з ПІІК для усунення недоліків;
термін (місяць, рік) проведення наступної самооцінки з ПІІК у ЗОЗ;
дату (число, місяць, рік) підпису звіту та прізвище, ім’я та по-батькові (за наявності), посаду особи, яка підписує звіт.
Додаток 5
до Порядку впровадження профілактики інфекцій
та інфекційного контролю в закладах охорони здоров’я,
які надають медичну допомогу в стаціонарних умовах
(пункт 6 розділу III)
Реалізація етапу базової оцінки (крок 2) для впровадження ПІІК в ЗОЗ
1. Завдання та необхідні дії
Завдання |
Необхідні дії |
1 |
2 |
Впровадити систему самооцінки ПІІК у ЗОЗ |
1. Розглянути протокол системної самооцінки ПІІК у ЗОЗ на нараді ВІК, за участі керівництва закладу та лідерів думки. |
Графік роботи |
Затвердити графік проведення самооцінки по структурним підрозділам та дату підсумкового засідання. |
Проведення самооцінки ПІІК у ЗОЗ не повинно обтяжувати працівників |
1. Зібрати всю необхідну інформацію та визначити співробітників кожного із структурних підрозділів, що будуть сприяти проведенню оцінки (наприклад, надавати доступ до баз даних). |
Завершити проведення самооцінки ПІІК у ЗОЗ |
1. Використовувати роздруковані протоколи для збору даних. |
Аналіз результатів |
Підрахувати результати для кожного із розділів та розрахувати загальний бал. |
Підготувати висновки за результатами самооцінки ПІІК у ЗОЗ |
1. По отриманню результатів самооцінки провести нараду ВІК та обговорити їх. |
Презентація отриманих результатів |
1. Запланувати серію зустрічей з метою представлення результатів оцінювання, обов’язково із зазначенням сильних та слабких сторін і шляхів покращення результатів, наступним категоріям: |
Ідентифікувати основні компоненти, що потребують покращення |
1. В процесі обговорення на нараді ВІК, визначте наявні проблеми і виберіть одну або декілька з них, що потребують негайного втручання. |
2. Потенційні бар’єри та рішення для їх подолання
Потенційний бар’єр |
Потенційні рішення |
Приклади реалізації |
1 |
2 |
3 |
Небажання проводити системну самооцінку ПІІК у ЗОЗ |
1. Переконати керівництво ЗОЗ та інші зацікавлені сторони в тому, що результати оцінювання будуть лише для внутрішнього використання, а не для «покарання винних». Важливо щоб система самооцінки позиціонувалася як критично важливий діагностичний інструмент, що дозволить легко розробити чіткий план дій. |
Використати пробну самооцінку: |
Втомленість від постійного проведення оцінювання |
1. Об’єднати проведення декількох оцінювань. |
При проведенні оцінювання слід дотримуватися таких правил: |
Відсутність кваліфікованих працівників з оцінювання |
1. Визначити лідерів думки з ПІІК та розвивати їхні навики шляхом систематичного навчання і підвищення кваліфікації. |
1. Проходження навчання в закладах освіти або в спеціалізованих центрах. |
Несприйняття на рівні медичних працівників |
Почати з малого — спираючись на існуючі підходи до збору даних, поступово впровадити компонент моніторингу, оцінки та зворотного зв’язку. |
Включити оцінку та зворотній зв’язок у повсякденне життя: |
Додаток 6
до Порядку впровадження профілактики інфекцій
та інфекційного контролю в закладах охорони здоров’я,
які надають медичну допомогу в стаціонарних умовах
(пункт 9 розділу III)
Реалізація етапу розробки та виконання плану дій з ПІІК (крок 3)
1. Завдання та необхідні дії
Завдання |
Необхідні дії |
1 |
2 |
Розробити план дій із урахуванням СОП з ПІІК і ММС |
1. Опрацювати із фахівцями ВІК результати моніторингу та обговорити їх. Визначити основний компонент ПІІК з дуже низьким або нульовим результатом. Розробити план впровадження даного основного компоненту ПІІК, визнавши його пріоритетом в короткостроковій перспективі. |
Забезпечення підтримки та затвердження плану дій |
1. Визначити склад групи, що має приймати участь в розробці та затвердженні плану дій. Звернутися до відповідних структурних підрозділів ЗОЗ для досягнення найкращого ефекту від впроваджуваних дій. |
Забезпечення ресурсами, що необхідні для усунення слабких сторін, які були виявлені в ході оцінювання |
1. Визначити, чи не змінилася потреба в ресурсах (людських або фінансових) для впровадження основних компонентів ПІІК, що була визначена на підготовчому етапі (крок 1). В першу чергу потрібно реалізовувати заходи, які не потребують ресурсів. |
Використовувати системний підхід |
Кінцевою метою розробки та реалізації плану дій є систематичне виявлення проблем та слабких сторін, визначення шляхів їх усунення і оцінка ефективності виконаних заходів. Для досягнення цієї мети слід дотримуватися такої послідовності: |
2. Потенційні бар’єри та рішення для їх подолання
2.1. Потенційні бар’єри для затвердження плану дій з ПІІК
Потенційний бар’єр |
Потенційні рішення |
Приклади реалізації |
1 |
2 |
3 |
Керівництво ЗОЗ заперечує необхідність затвердження плану дій з ПІІК |
1. Дані відіграють вирішальну роль в переконанні керівництва у необхідності дій: «немає даних — немає проблем». При наявності результатів системної самооцінки ПІІК у ЗОЗ, їх використання допоможе забезпечити підтримку для розробки і впровадження плану дій з ПІІК. |
1. «Є дані — є проблема, немає даних — немає проблеми». |
План дій з ПІІК не сприймається серед працівників ЗОЗ |
1. Визначити та надавати всебічну підтримку лідеру думки з ПІІК. |
1. Визначити лідерів думки: |
Відсутність досвіду у фахівців ВІК у розробці та впровадженні заходів ПІІК |
Почати з малого — визначити принаймні одну особу для проходження навчання з ПІІК. |
1. Навчання крок за кроком: |
Відсутні кошти та технічне забезпечення для плану дій з ПІІК |
1. Розглянути можливість перепрофілювання коштів з інших програм/заходів. |
1. Переорієнтація витрат: |
2.2. Потенційні бар’єри при розробці та затвердженні СОП з ПІІК
Потенційний бар’єр |
Потенційні рішення |
Приклади реалізації |
1 |
2 |
3 |
Забезпечення постійного оновлення СОП |
1. Регулярно перевіряти чи є відповідні оновлення доказової бази або появу нових підходів і практик. |
Графік семінарів для ВІК, що проводяться на регіональному і національному рівнях: |
Відсутній досвід в розробці або адаптації СОП з ПІІК |
1. Залучити якомога більшу кількість зацікавлених сторін, в тому числі керівництво закладу і різні категорії медичних працівників, для досягнення консенсусу. Особливу увагу слід звернути на викладенні СОП зрозумілою мовою і простоті їх виконання. |
1. Використання зовнішнього досвіду як каталізатора для дії: |
Оперативність розповсюдження і впровадження СОП |
1. Паралельно із розробкою СОП визначити, яким чином вони будуть розповсюджуватися і впроваджуватися. |
Використання ММС: |
Інтеграція СОП з ПІІК у інші суміжні програми/плани/заходи |
Обговорити із зацікавленими сторонами і суміжними з ВІК структурними підрозділами СОП та можливість спільного впровадження на етапі розробки (використати відносини, що були сформовані на етапах кроків 1 та 2). СОП з ПІІК можуть посилатися на інші, вже впроваджені програми/плани/заходи, або навпаки. |
Забезпечення інтеграції СОП з ПІІК у суміжні програми/плани/заходи, що вже впроваджені в ЗОЗ: |
2.3. Потенційні бар’єри при розробці та затвердженні заходів з навчання та підготовки з ПІІК
Потенційний бар’єр |
Потенційні рішення |
Приклади реалізації |
1 |
2 |
3 |
Недостатність навчальних матеріалів |
1. Почати з основ. Наприклад, провести навчання з гігієни рук, використовуючи наявні матеріали. |
Почати з малого: |
Недостатність досвіду в проведенні навчання |
1. Використати підхід «вчитель готує вчителя». |
Підхід «вчитель готує вчителя»: |
Відсутність у працівників бажання навчатися |
Навчанням мають бути охоплені всі без винятку працівники ЗОЗ (керівний склад, лікарі, середні і молодші медичні працівники, працівники допоміжних служб). |
1. Міждисциплінарний підхід до навчання: залучити до навчання представників всіх структурних підрозділів (від керівництва до прибиральників) — такий підхід забезпечує прихильність працівників до ПІІК. |
Відсутність у працівників часу на навчання |
1. Розглянути можливість проведення навчання на робочому місці, а також наставництва. |
1. Навчання без відриву. |
Працівники не бажають долучатися до навчання інших |
Розглянути можливість використання симуляції ситуацій. |
Використання симуляції ситуацій — перетворення навчання на гру або театральну постановку допомагає із більшою ефективністю залучити працівників до навчання інших. |
2.4. Потенційні бар’єри при розробці та затвердженні заходів з епідеміологічного нагляду за ІПНМД
Потенційний бар’єр |
Потенційні рішення |
Приклади реалізації |
1 |
2 |
3 |
Відсутність досвіду в проведенні епідеміологічного нагляду за ІПНМД |
1. Вивчити існуючі національні чи регіональні програми та можливість підтримки вашого ЗОЗ з метою отримання знань і досвіду для реалізації запланованих заходів. |
1. Співпраця із регіональними або національними програмами: |
Відсутнє розуміння з чого почати |
1. Направити зусилля на структурні підрозділи високого ризику (наприклад, відділення анестезіології, реанімації та інтенсивної терапії — девайс-асоційовані інфекції або хірургічні відділення — ІОХВ). |
Почати з впровадження епіднагляду в структурних підрозділах високого ризику: |
Необхідність епіднагляду відсутня |
1. Забезпечити на постійній основі надання даних епіднагляду керівництву ЗОЗ і керівникам структурних підрозділів на зібраннях і зустрічах. |
1. Використати стратегію зворотного зв’язку: |
Відсутність мікробіологічної лабораторії або недостатня її оснащеність |
1. Вивчити можливість направлення зразків в лабораторію регіонального, обласного або національного рівня. |
Епідеміологічний нагляд без мікробіологічної лабораторії неможливий: |
2.5. Потенційні бар’єри при розробці та затвердженні заходів з моніторингу, оцінки і зворотного зв’язку
Потенційний бар’єр |
Потенційні рішення |
Приклади реалізації |
1 |
2 |
3 |
Відсутня підтримка моніторингу, оцінки і зворотного зв’язку |
1. Пояснити, що моніторинг, оцінка і зворотній зв’язок — ключовий елемент ММС. |
Мультидисциплінарний підхід: |
Оцінка займає занадто багато часу |
1. Почати із оцінок, що оцінюють один СОП та письмового збору даних. |
Кожен сам для себе є найкращим суддею: |
2.6. Потенційні бар’єри при розробці та затвердженні заходів щодо режиму роботи, штатного розпису і навантаження на ліжко
Потенційний бар’єр |
Потенційні рішення |
Приклади реалізації |
1 |
2 |
3 |
Недостатньо людських ресурсів, в тому числі для ПІІК |
1. Залучити медичних сестер клінічних структурних підрозділів, як тимчасовий захід. |
|
Наявна кількість ліжок не задовольняє потреби |
1. Малорозмірні ліжка в дитячих відділеннях. |
Креативні рішення для створення додаткового простору: |
2.7. Потенційні бар’єри при розробці та затвердженні заходів щодо приміщень, матеріалів та обладнання
Потенційний бар’єр |
Потенційні рішення |
Приклади реалізації |
1 |
2 |
3 |
Відсутність досвіду щодо затвердження та впровадження заходів щодо приміщень, матеріалів та обладнання |
Визначити можливість залучення фахівців регіонального або національного рівнів. |
Посилення потенціалу шляхом консолідації зусиль регіону: |
Відсутність програми управління відходами |
Використати прості та дрібномасштабні підходи до поліпшення якості, що ґрунтуються на ММС. |
Маленькі проекти для досягнення великих цілей: |
2.8. Потенційні бар’єри при розробці та затвердженні заходів з впровадження ММС в ПІІК
Потенційний бар’єр |
Потенційні рішення |
Приклади реалізації |
Відсутнє поняття про те, що таке ММС |
Роз’яснити критичність впровадження ММС в реалізації та підтримці ПІІК. |
Підвищити освіченість шляхом семінарів. |
Труднощі у «зміні культури» в рамках ММС |
Використовувати гігієну рук в якості прикладу того, що означає мультимодальна стратегія, і розробити опис кожного із п’яти компонентів ММС. |
Використати чемпіонів для розповсюдження знань: |
Додаток 7
до Порядку впровадження профілактики інфекцій
та інфекційного контролю в закладах охорони здоров’я,
які надають медичну допомогу в стаціонарних умовах
(пункту 15 розділу III)
Реалізація етапу оцінки впливу (крок 4)
Завдання і необхідні дії
Завдання |
Необхідні дії |
1 |
2 |
Відслідковування прогресу |
1. Переглянути результати базової оцінки (крок 2) і план дій (крок 3). |
Узгодження ролей і обов’язків |
1. Визначити працівників ВІК, які будуть проводити оцінку впливу із застосуванням протоколу системної самооцінки ПІІК в ЗОЗ. |
Час проведення |
Під час засідань, за участю керівників оцінюваних структурних підрозділів, визначити графіки проведення та дату закінчення оцінки впливу. |
Аналіз результатів |
1. Порівняти результати із базовою оцінкою і обговорити із фахівцями ВІК, де отримані дані вказують на усунення проблем і де вони все ще існують (по кожному основному компоненту окремо і в цілому). |
Представлення результатів і дотримання графіку оцінювання |
1. Організувати зустріч або серію зустрічей для представлення результатів повторної системної самооцінки з ПІІК керівникам ЗОЗ і відповідних клінічних структурних підрозділів (бажано із залученням сестер медичних), а також іншим зацікавленим сторонам (відділ контролю якості медичних послуг, спілки пацієнтів та інші громадські об’єднання тощо). |
Додаток 8
до Порядку впровадження профілактики інфекцій
та інфекційного контролю в закладах охорони здоров’я,
які надають медичну допомогу в стаціонарних умовах
(пункт 18 розділу III)
Реалізація етапу формування культури безпеки (крок 5)
1. Завдання та необхідні дії
Завдання |
Необхідні дії |
1 |
2 |
Спиратися на дані та досвід, що отримані на попередніх етапах |
Використати переглянутий на етапі кроку 4 план дій і результати системної самооцінки з ПІІК для розробки довгострокового (наприклад, п’ятирічного) плану, у якому обов’язково зазначити регулярний (щонайменше, щорічний) цикл оцінювання та перегляду, з метою забезпечення довгострокового стійкого впливу. |
Залучати та підтримувати лідерів думки у процесі формування культури безпеки |
1. Організовувати зустрічі із керівництвом ЗОЗ, задля забезпечення довгострокової підтримки ПІІК. |
Використовувати мультимодальну стратегію впровадження ПІІК |
Під час розгляду плану дій заохочувати обговорення за участю всіх зацікавлених сторін проблем, що стосуються: |
Повідомляти про успіхи у ПІІК та заохочувати кращих |
1. Визначити, яким чином, окрім зустрічей на рівні ЗОЗ, можна повідомити про успіхи у впровадженні ПІІК (наприклад, виступи на національних або міжнародних конференціях, публікації у фахових журналах). |
2. Потенційні бар’єри і рішення для їх подолання
Потенційний бар’єр |
Потенційні рішення |
Приклади реалізації |
1 |
2 |
3 |
Лідери думки і чемпіони не затримуються на довго в ЗОЗ |
1. Включити в довгостроковий план дій можливе періодичне оновлення або повторне впровадження ПІІК. |
Підхід вчитель готує вчителя: |
Втома від ПІІК або поява нових пріоритетів |
1. Продовжити співпрацю з іншими суміжними структурними підрозділами з метою включення питань ПІІК у інші програми/плани/заходи. |
|
Перерозподіл коштів — фінансові ресурси, які направлені на ПІІК, передають на інші програми |
1. Переглянути і оновити бюджет. |
ЗАТВЕРДЖЕНО
Наказ Міністерства охорони здоров’я України
03 серпня 2021 року № 1614
Зареєстровано
в Міністерстві юстиції України
11 жовтня 2021 р. за № 1321/36943
Інструкція з впровадження покращення гігієни рук в закладах охорони здоров’я та установах / закладах надання соціальних послуг / соціального захисту населення
I. Загальні положення
1. Ця Інструкція визначає порядок організації гігієни рук і спрямована на оптимізацію заходів щодо запобігання появи та поширення в закладах охорони здоров’я та серед фізичних осіб-підприємців, які зареєстровані в установленому законом порядку та одержали ліцензію на право провадження господарської діяльності з медичної практики, закладах громадського здоров’я (далі — ЗОЗ), установах / закладах надання соціальних послуг / соціального захисту населення (далі — ЗСЗ) інфекційних хвороб, пов’язаних з наданням медичної допомоги, та мікроорганізмів із антимікробною резистентністю.
Ця Інструкція не застосовується для фармацевтичних (аптечних) закладів, центрів медичної статистики та автопідприємств санітарного транспорту.
2. Ця Інструкція є обов’язковою для ЗОЗ і ЗСЗ незалежно від форм власності та їх відомчого підпорядкування, крім зазначених у абзаці другому пункту 1 цієї Інструкції.
3. Відповідальними за виконання цієї Інструкції у ЗОЗ, ЗСЗ є його керівник, у структурних підрозділах ЗОЗ, ЗСЗ — відділ з інфекційного контролю (далі — ВІК) та керівники структурних підрозділів.
4. У цій Інструкції терміни та умовні скорочення вживаються у такому значенні:
антисептик для рук — спиртовмісний дезінфекційний засіб (рідина, гель або піна), що застосовується для нанесення на шкіру рук з метою знищення мікроорганізмів;
гігієнічна обробка рук — обробка рук шляхом втирання антисептика для рук в шкіру рук;
диспенсер — пристрій для контрольованої видачі речовини або рідини заданою кількістю, об’ємом або вагою;
зацікавлена сторона — людина, посадова особа, група осіб, організація або її структурний підрозділ, що зацікавлені у певному рішенні щодо впровадження профілактики інфекцій та інфекційного контролю, включаючи тих, на кого буде прямо чи опосередковано чинитися вплив;
зворотній зв’язок — повідомлення у будь-якій формі, які людина (працівник) або організація, її структурний підрозділ посилає у відповідь на повідомлення іншої людини (працівника) або організації, її структурного підрозділу;
культура безпеки — продукт індивідуальних та групових цінностей, відносин, уявлень, компетенцій і моделей поведінки, які визначають прихильність, стиль та майстерність управління організацією в області охорони здоров’я та безпеки. Організації із позитивною культурою безпеки характеризуються комунікаціями, що базуються на взаємній довірі, спільному сприйнятті важливості безпеки, а також впевненістю у ефективності превентивних заходів. Впровадження профілактики інфекцій та інфекційного контролю є складовою культури безпеки ЗОЗ;
лідер думки — людина, що володіє здатністю впливати на думки і поведінку інших;
чемпіон — людина, що активно підтримує нововведення і чий вплив є критичною рушійною силою для успіху впровадження;
АМР — антимікробна резистентність;
ІПНМД — інфекційні хвороби, пов’язані із наданням медичної допомоги;
ММС — мультимодальна стратегія;
ПІІК — профілактика інфекцій та інфекційний контроль.
Інші терміни у цій Інструкції вживаються у значеннях, наведених в Законах України «Основи законодавства України про охорону здоров’я», «Про захист населення від інфекційних хвороб», «Про соціальні послуги», «Про охорону дитинства» та інших нормативно-правових актах у сфері охорони здоров’я і надання соціальних послуг.
5. ММС з покращення гігієни рук в ЗОЗ/ЗСЗ є частиною комплексного підходу для зниження розповсюдженості ІПНМД та АМР. Її впровадження відіграє ключове значення для досягнення безпеки пацієнтів.
6. ММС з покращення гігієни рук складається із наступних основних компонентів:
1) зміни в системі:
забезпечення наявності інфраструктури, що дозволяє працівникам дотримуватися гігієни рук;
доступ до централізованого водопостачання, мила і одноразових паперових рушників;
доступ до антисептику для рук в точці догляду;
2) навчання і підготовка — забезпечення регулярних навчань і практичної підготовки з правил і практик гігієни рук відповідно до додатку 1 до цієї Інструкції, СОП, розробленої відповідно до додатку 2 до цієї Інструкції;
3) нагадування на робочому місці — нагадування працівникам ЗОЗ/ЗСЗ про важливість гігієни рук, показання і процедури для її виконання;
4) моніторинг, оцінка і зворотній зв’язок — моніторинг дотримання рекомендованих практик та наявної інфраструктури, а також зворотній зв’язок, який полягає в розповсюдженні отриманих результатів та їх обговорення;
5) культура дотримання гігієни рук — створення середовища і сприйняття в колективі, які сприятимуть підвищенню обізнаності щодо проблем безпеки пацієнтів і гарантуватимуть постійне поліпшення або підтримання на високому рівні гігієни рук, у тому числі:
активну участь як на рівні ЗОЗ/ЗСЗ, так і на індивідуальному рівні працівника;
усвідомлення індивідуальної (працівника) та інституційної спроможності ЗОЗ/ЗСЗ до змін і покращення;
партнерство з пацієнтами, їх організаціями.
Культура дотримання гігієни рук є складовою культури безпеки ЗОЗ/ЗСЗ.
7. Діяльність із впровадження гігієни рук, оцінки і зворотного зв’язку мають періодично переглядатися (із урахуванням новітніх даних), повторюватися (при відсутності позитивних зрушень або при поверненні до відправної точки) та стати частиною заходів із покращення якості надання медичної допомоги/соціальних послуг з догляду. Покращення в сфері гігієни рук не може бути обмеженим у часі, тому моніторинг, оцінка і зворотній зв’язок, навчання і підготовка, нагадування про необхідність дотримання практик повинні впроваджуватися в ЗОЗ/ЗСЗ постійно.
8. Розробка та впровадження заходів з покращення гігієни рук у ЗОЗ/ЗСЗ здійснюється ВІК відповідно цієї Інструкції. Штатні працівники ВІК виконують функції координатора з гігієни рук, його заступника(-ів), інструктора(-ів)/тренера(-ів) та спеціаліста зі збору та аналізу даних/статистика. Функції спостерігача(-ів)/дослідника(-ів) можуть виконувати працівники інших структурних підрозділів ЗОЗ/ЗСЗ та залучатися за потреби. Профіль та основні завдання працівників, які виконують зазначені функції наведено у додатку 3 до цієї Інструкції. Кількість працівників для впровадження заходів з покращення гігієни рук у ЗОЗ/ЗСЗ визначається в залежності від розміру ЗОЗ/ЗСЗ та функціонального навантаження працівників.
Для фізичних осіб-підприємців, які зареєстровані в установленому законом порядку та одержали ліцензію на право провадження господарської діяльності з медичної практики (далі — ФОП), створення ВІК або визначення працівників для виконання функцій координатора з гігієни рук, його заступника, інструктора/тренера та спеціаліста зі збору та аналізу даних/статистика є не обов’язковим, може здійснюватися на добровільних засадах з урахуванням розміру організованої ними медичної практики. ФОП зобов’язані виконувати правила і практики гігієни рук відповідно до додатку 1 до цієї Інструкції.
ВІК створюється відповідно до Положення про відділ з інфекційного контролю закладу охорони здоров’я та установи / закладу надання соціальних послуг / соціального захисту населення, затвердженого наказом Міністерства охорони здоров’я України від 03 серпня 2021 року № 1614.
9. Координацію заходів з покращення гігієни рук у адміністративно-територіальних одиницях здійснює регіональний координатор з гігієни рук, який є координатором з гігієни рук закладу громадського здоров’я у відповідній адміністративно-територіальній одиниці.
II. Зміни в системі
1. Дотримання гігієни рук можливе лише в тому випадку, якщо ЗОЗ/ЗСЗ забезпечує необхідну інфраструктуру і постійну наявність витратних матеріалів для гігієни рук. Тому для надійного та постійного дотримання працівниками гігієни рук, керівництво ЗОЗ/ЗСЗ має забезпечити:
1) раковини для миття рук із доступом до проточної води в кожному приміщенні, де проводяться догляд за хворими, інструментальні дослідження та інвазивні процедури;
2) рідке мило;
3) одноразові паперові рушники;
4) антисептик для рук.
2. Антисептик для рук повинен відповідати Державним стандартам України, які затверджуються національним органом стандартизації, добре переноситися працівниками та підбиратися з урахуванням його вартості таким чином, щоб забезпечити достатню його кількість.
3. Диспенсери мають бути встановлені поблизу точок догляду, бути справними, надійними і заповненими милом/антисептиком для рук. Слід обов’язково дотримуватися рекомендацій щодо безпечного повторного використання дозатору, які зазначені в інструкції до виробу.
4. Кишенькові ємності з антисептиком для рук можуть використовуватися лише у випадках або у підрозділах, де існує потенційний ризик вживання антисептика для рук пацієнтами як алкогольного напою.
5. Для забезпечення зміни в системі у ЗОЗ/ЗСЗ проводяться наступні оцінки:
1) інфраструктури і ресурсів для гігієни рук у ЗОЗ/ЗСЗ відповідно до протоколу, наведеного у додатку 4 до цієї Інструкції;
2) потреби у антисептику для рук та витрат на нього відповідно до протоколу, наведеного у додатку 5 до цієї Інструкції;
3) використання засобів для гігієни рук у ЗОЗ/ЗСЗ відповідно до протоколу, наведеного у додатку 6 до цієї Інструкції;
4) переносимості і прийнятності антисептику для рук, що використовується або планується до використання у ЗОЗ/ЗСЗ відповідно до протоколу, наведеного у додатку 7 до цієї Інструкції.
Зазначені оцінки можуть проводитись:
на початку впровадження заходів із покращення гігієни рук;
для вдосконалення впроваджених заходів з гігієни рук;
після змін в інфраструктурі ЗОЗ/ЗСЗ (наприклад, після ремонту або переобладнання приміщень, добудови нового корпусу).
Оцінки проводяться із залученням спостерігачів/дослідників, які проводять збір даних відповідно до затверджених форм протоколів оцінок.
6. У випадку, коли ЗОЗ/ЗСЗ має серйозні недоліки в інфраструктурі для змін в системі (відсутні або наявні в недостатній кількості раковини для миття рук, відсутня проточна вода, відсутнє або наявне в недостатній кількості рідке мило та/або одноразові паперові рушники) необхідно провести оцінку наявної інфраструктури і ресурсів відповідно до протоколу, наведеного у додатку 4 до цієї Інструкції, та обговорення її результатів із керівником ЗОЗ/ЗСЗ, визначити необхідність дотримання рекомендацій щодо співвідношення раковини/кількість ліжок для пацієнтів 1 до 10 та постійного забезпечення проточною водою, рідким милом і одноразовими паперовими рушниками.
У разі недоступності у ЗОЗ/ЗСЗ антисептику для рук:
провести оцінку потреби у антисептику для рук та витрат на нього відповідно до протоколу, наведеного у додатку 5 до цієї Інструкції;
перевірити переносимість і прийнятність антисептиків для рук, використовуючи метод 1 протоколу оцінки переносимості і прийнятності антисептику для рук, що використовується або планується до використання у ЗОЗ/ЗСЗ, наведеного у додатку 7 до цієї Інструкції.
Для прийняття рішення щодо закупівлі антисептику для рук в ЗОЗ/ЗСЗ враховуються такі критерії як доступність на ринку, переносимість шкірою рук та вартість.
7. У випадку, коли ЗОЗ/ЗСЗ почав реалізовувати заходи з гігієни рук, але показники успіху відповідно до пункту 11 розділу V цієї Інструкції не були досягнуті необхідно:
1) визначити як засіб переноситься працівниками відповідно до додатку 7 до цієї Інструкції;
2) розглянути питання вибору іншого продукту;
3) використовуючи протокол оцінки інфраструктури і ресурсів (додаток 4 до цієї Інструкції), визначити як і в яких умовах використовуються засоби для гігієни рук (на постійній основі чи лише в окремих ситуаціях), чи розміщені засоби для гігієни рук в усіх точках догляду;
4) забезпечити наявність засобів для гігієни рук в усіх точках догляду (наприклад, диспенсери знаходяться біля кожного ліжка хворого, а не біля входу до палати; наявні дозатори різних видів — настінні, кишенькові, прикріплені до меблів; співвідношення раковина/ліжко для пацієнта більше або дорівнює 1:10);
5) сприяти забезпеченню достатнього річного бюджету для закупівлі засобів для гігієни рук, із розрахунку, що засоби для гігієни рук мають бути доступні в кожному підрозділі та цілодобово.
8. У випадку, коли в ЗОЗ/ЗСЗ досягли успіхів у впровадженні гігієни рук для підтримки зміни в системі необхідно:
1) сфокусувати основну увагу на продовженні і вдосконаленні досягнутого (формування культури гігієни рук);
2) проводити оцінки наявної інфраструктури і ресурсів, переносимості і прийнятності антисептиків для рук (додатки 4, 7 до цієї Інструкції) відповідно до затверджених планів-графіків (додаток 8, 9 до цієї Інструкції) з метою виявлення на постійній основі недоліків;
3) виділяти відповідний річний бюджет для забезпечення ресурсами для гігієни рук всіх підрозділів у будь-який час.
III. Навчання і підготовка
1. Для впровадження покращення гігієни рук всі працівники ЗОЗ/ЗСЗ мають пройти курс з навчання і підготовки щодо правил і практик гігієни рук (додаток 1 до цієї Інструкції), який розробляється ВІК (координатором з гігієни рук).
2. Навчання і підготовка повинні проводитись ВІК (координатором з гігієни рук, інструкторами/тренерами з гігієни рук, координатором з навчання і підготовки з ПІІК) регулярно (включно із обов’язковим навчанням для нових працівників), включати перевірку знань і практик, спонукати до поведінкових і культурних змін, а також гарантувати, що компетентність глибоко укорінилася і підтримується всіма працівниками ЗОЗ/ЗСЗ у відношенні гігієни рук.
3. Викладач (координатор навчання і підготовки з ПІІК, координатор з гігієни рук, тренер/інструктор) має користуватися чіткими формулюваннями, що закриті для особистої інтерпретації, з орієнтованим на працівника стандартизованим підходом.
4. За результатами навчання кожен працівник ЗОЗ/ЗСЗ повинен мати щонайменше базовий рівень знань із гігієни рук для формування безпечного середовища в ЗОЗ/ЗСЗ.
5. Навчання і підготовку мають пройти інструктори/тренери, спостерігачі або дослідники та працівники. Для їх навчання необхідно використовувати низхідний підхід, при якому координатор з гігієни рук разом із зацікавленими сторонами визначають осіб, що стануть інструкторами (тренерами) і спостерігачами.
6. Навчання і підготовка тренера має бути проведена координатором з гігієни рук (при наявності підготовки і досвіду) або спеціалізованим закладом (заклад освіти або тренінговий центр). Аналогічно, спостерігачі або дослідники повинні пройти курс навчання, однак, особлива увага при їхній підготовці має приділятися правильному використанню протоколів для оцінки (додатки 4, 5, 6, 7, 10, 11, 12 до цієї Інструкції).
7. Плани навчання і підготовки працівників з гігієни рук розробляються і затверджуються на етапі першого кроку відповідно до розділу VII цієї Інструкції та включають інформацію про кількість виділеного часу, конкретні клінічні/практичні умови, в яких вони будуть проводитися, та пріоритетні напрями (наприклад, профілактика катетер-асоційованих інфекцій кровотоку).
8. Базові навчальні програми для інструкторів, спостерігачів і працівників мають включати:
1) основи інфекційної безпеки пацієнтів;
2) визначення, вплив та розповсюдженість ІПНМД;
3) основні патерни передавання патогенів, що пов’язані із наданням медичної допомоги, із акцентуацією уваги на контактному (через руки) шляху інфікування;
4) профілактика ІПНМД і роль гігієни рук в ній;
5) правила і практики з гігієни рук, наведені у додатку 1 до цієї Інструкції;
6) додаткові заняття мають бути присвячені спостерігачам (проведення тренінгів з протоколів для оцінки).
9. ЗОЗ/ЗСЗ необхідно запровадити систему перевірки компетентності всіх працівників після проведеного навчання. Це може мати форму щорічного навчального курсу або практичного демонстративного семінару з гігієни рук із наступним тестуванням або перевіркою практичних навичок.
10. Результат проведеного оцінювання з гігієни рук також може бути використаний як:
1) підстава для допуску/не допуску до виконання своїх функціональних обов’язків нових медичних працівників (при працевлаштуванні, після випробувального терміну);
2) показник відповідності займаній посаді або компетентності працівника.
11. В ЗОЗ/ЗСЗ, де навчання і підготовка з гігієни рук проводиться недостатньо або не проводиться взагалі, потрібно розробити відповідний план дій, який буде включати:
1) визначення особи, відповідальної за розробку або доопрацювання навчальних програм;
2) визначення процедур та критеріїв підбору майбутніх інструкторів/тренерів та спостерігачів;
3) пріоритетні групи працівників, які мають пройти навчання і підготовку;
4) строки початку і закінчення навчання інструкторів, спостерігачів та працівників;
5) затвердження графіків навчання і підготовки;
6) виділений бюджет на проведення навчання і підготовки.
12. В ЗОЗ/ЗСЗ, де проводиться базова підготовка працівників з часом виникає необхідність ввести нові заходи для поступового формування культури дотримання гігієни рук. В цьому випадку в ЗОЗ/ЗСЗ можуть проводитись такі додаткові дії:
1) постійне (безперервне) навчання всіх працівників в ЗОЗ/ЗСЗ із щорічною перевіркою їх компетентності;
2) підготовка нових тренерів та спостерігачів;
3) проведення навчання і підготовки, спираючись на зворотній зв’язок (дані перевірок компетентності та дані проведених системних самооцінок з ПІІК (для ЗОЗ) відповідно до додатку 4 до Порядку впровадження профілактики інфекцій та інфекційного контролю в закладах охорони здоров’я, які надають медичну допомогу в стаціонарних умовах, затвердженого наказом Міністерства охорони здоров’я України від 03 серпня 2021 року № 1614;
4) перегляд та оновлення відповідно до нових даних навчальних програм (не менше одного разу на рік);
5) обмін досвідом із іншими ЗОЗ/ЗСЗ та публікація досягнень;
6) регулярний перегляд і оновлення планів дій із урахуванням зворотного зв’язку.
IV. Нагадування на робочому місці
1. Нагадування на робочому місці — найліпший спосіб звернути увагу працівників на важливість гігієни рук. Нагадування мають містити відповідні вказівки та процедури для їх виконання. Вони також є засобом інформування пацієнтів та їх родичів щодо якості догляду, яку вони повинні отримати від працівників ЗОЗ/ЗСЗ.
2. Інформаційні плакати є найпоширенішим типом нагадування. Інші типи нагадувань — кишенькові листівки, наклейки, які розміщені поряд із точками догляду, та позначки/малюнки, слогани щодо важливості гігієни рук (наприклад, «Помий руки — збережи життя»). Також рекомендовано використовувати мобільні технології, програмні продукти та комп’ютерні технології для спонукання до дотримання гігієни рук.
3. Розробка та розміщення інформаційних матеріалів повинні бути включені в плани дій ЗОЗ/ЗСЗ з покращення гігієни рук.
4. Інформаційні матеріали із зазначенням етапів та показань до проведення гігієни рук розміщуються у всіх підрозділах ЗОЗ/ЗСЗ та можуть стосуватися працівників, пацієнтів та інших відвідувачів ЗОЗ/ЗСЗ.
5. ЗОЗ/ЗСЗ, які починають впровадження гігієни рук і мають обмежені ресурси, забезпечують виконання наступних дій:
1) оцінка наявних ресурсів, що можуть бути використані для фінансування заходів з нагадування працівникам;
2) розробка макетів і визначення строків їх виробництва;
3) визначення наступних фінансових затрат та затвердження бюджету.
6. В ЗОЗ/ЗСЗ, де здійснюється впровадження покращення гігієни рук, забезпечується виконання наступних дій:
1) розгляд можливості адаптації інформаційних матеріалів до місцевого контексту ЗОЗ/ЗСЗ (наприклад, заміна фотографій або рисунків);
2) регулярні перевірки стану інформаційних матеріалів та їх заміну за необхідності;
3) розгляд можливості втілення ідей працівників ЗОЗ/ЗСЗ на інформаційних плакатах (наприклад, запросити дизайнера або художника);
4) використання інших видів нагадувань (наприклад, листівки або відеоролики).
V. Моніторинг, оцінка і зворотній зв’язок
1. Моніторинг і оцінка є необхідним компонентом впровадження покращення гігієни рук. Безперервний моніторинг дозволяє визначити зміни, які набуті в процесі впровадження заходів з гігієни рук, та їх ефективність.
2. Шляхом проведення системного оцінювання відповідно до протоколу системної самооцінки гігієни рук в ЗОЗ/ЗСЗ (додаток 12 до цієї Інструкції) визначається рівень гігієни рук в ЗОЗ/ЗСЗ та області, що заслуговують більш значних зусиль. Ця інформація використовується для корегування плану дій ЗОЗ/ЗСЗ з покращення гігієни рук.
3. В ЗОЗ/ЗСЗ необхідно проводити моніторинг наступних показників:
1) дотримання правил гігієни рук шляхом безпосереднього спостереження;
2) наявні інфраструктура і ресурси;
3) знання працівників щодо ІПНМД та гігієни рук;
4) сприйняття працівниками гігієни рук та проблеми ІПНМД;
5) використання засобів для гігієни рук.
4. Проведення початкової/базової оцінки важливе на кожному з етапів впровадження ММС покращення гігієни рук, але особливо у ЗОЗ/ЗСЗ, де системні заходи з гігієни рук реалізуються вперше. Така оцінка здійснюється для збору даних, які реально відображають ситуацію щодо поточного дотримання гігієни рук, знань, сприйняття та інфраструктури.
5. Після реалізації ЗОЗ/ЗСЗ плану дій (наприклад, річного) з метою відслідковування прогресу і підтвердження того, що впровадження ініціатив з покращення гігієни рук призвело до зниження розповсюдженості ІПНМД, проводиться повторна оцінка. Повторні оцінки забезпечать послідовність, порівняння результатів та вимірювання прогресу.
6. Збір та аналіз даних — важлива частина оцінки. У разі відсутності в ЗОЗ/ЗСЗ статистичного підрозділу, визначається працівник(-ки) для збору та аналізу даних відповідно до профілю у додатку 3 до цієї Інструкції.
7. Збір, аналіз даних та ведення звітності з впровадження компонентів ММС потребує забезпечення комп’ютерною технікою. Для збору даних можуть використовуватись паперові або електронні копії відповідних форм та електронні інструменти (програмне забезпечення).
8. Дані із анкет/опитувальників, які використовуються для проведення оцінки, вносяться до електронного інструменту (програмного забезпечення), який використовується ЗОЗ/ЗСЗ з метою збереження і аналізу даних. Після введення даних друковані або електронні копії зберігаються у координатора з гігієни рук протягом одного року.
9. Зворотній зв’язок після проведеного оцінювання є обов’язковим етапом і робить таке оцінювання значимим. Результати проведеного оцінювання мають отримати всі зацікавлені сторони (у вигляді письмового чи електронного звіту, презентації під час навчання, під час робочої зустрічі тощо). Існують також інші способи зворотного зв’язку, тому в кожному із ЗОЗ/ЗСЗ обирається найбільш прийнятний спосіб.
10. Після проведеної базової оцінки в ЗОЗ/ЗСЗ, де системні заходи з покращення гігієни рук проводяться вперше, отримані дані будуть вказувати на проблеми у практиці гігієни рук, що застосовується, прогалини в знаннях або на погане сприйняття працівниками проблеми. В таких випадках результати оцінювання презентуються працівникам і використовуються для підвищення їх обізнаності та переконання у необхідності змін. Наступне оцінювання, що буде проведене після реалізації плану дій з покращення гігієни рук, має продемонструвати покращення і підтримати мотивацію до використання впроваджених практик. Ці дані також є важливими для визначення проблемних областей, в яких необхідні подальші зміни.
11. Ключовими показниками успіху ЗОЗ/ЗСЗ у впровадженні покращення гігієни рук є:
1) підвищення показника дотримання правил гігієни рук;
2) покращення інфраструктури гігієни рук;
3) збільшення використання засобів для гігієни рук;
4) покращення сприйняття гігієни рук працівниками;
5) покращення знань з гігієни рук;
6) покращення рівня ПІІК (для ЗОЗ).
Оцінка показників здійснюється з використанням протоколів оцінки, наведених у додатках 4, 6, 11, 12 до цієї Інструкції та для ЗОЗ у додатку 4 до Порядку впровадження профілактики інфекцій та інфекційного контролю в закладах охорони здоров’я, які надають медичну допомогу в стаціонарних умовах, затвердженого наказом Міністерства охорони здоров’я України від 03 серпня 2021 року № 1614.
VI. Культура дотримання гігієни рук
1. Створення культури безпеки в ЗОЗ/ЗСЗ є пріоритетом для всіх дій, спрямованих на підтримку гігієни рук, незалежно від рівня прогресу в ЗОЗ/ЗСЗ із впровадження заходів з гігієни рук.
2. На початковому етапі створюється мотивація дотримання гігієни рук. Керівники ЗОЗ/ЗСЗ і лідери думки залучаються до процесу планування заходів з гігієни рук на найбільш ранній стадії та беруть участь у подальшому процесі впровадження та після реалізації відповідного плану дій.
3. Для безперервного прогресу одночасно або в подальшому оцінюються і покращуються інші області безпеки пацієнтів, а культура безпеки має глибоко укорінитися в інституціональних традиціях і підходах ЗОЗ/ЗСЗ. Це потребує постійного прогресу в розробці систем для виявлення небажаних явищ і оцінки якості, при цьому гігієна рук залишається ключовим показником.
4. Пацієнти залучаються до формування інституційного середовища безпеки ЗОЗ/ЗСЗ. Обізнаність і сприйняття необхідності гігієни рук пацієнтами є важливими аспектами, що враховуються при розробці плану дій ММС з покращення гігієни рук. Мотивація працівників пацієнтами до виконання СОП сприятиме прискоренню реалізації зазначеного плану дій. Дотримання правил гігієни рук сприяє формуванню довірчих відносин між пацієнтами і працівниками та робить перебування в ЗОЗ/ЗСЗ більш безпечним для пацієнтів і працівників.
5. У випадку, коли ЗОЗ/ЗСЗ починає впроваджувати покращення гігієни рук, необхідно:
1) визначити координатора з гігієни рук і, за необхідності, його команду;
2) координатору з гігієни рук:
підготувати ініціативи з покращення гігієни рук у ЗОЗ/ЗСЗ;
визначити зацікавлені сторони в ЗОЗ/ЗСЗ та заручитися їхньою підтримкою (наприклад, отримати фінансування і кадрові ресурси, підтримку в організації навчальних заходів);
разом із керівником підрозділу, в якому впроваджується покращення гігієни рук, визначити щонайменше одного працівника (для кожного підрозділу), які пройдуть навчання і підготовку та стануть інструкторами (тренерами) і спостерігачем(ами) (перевага надається працівникам, які вже пройшли навчання з основних засад ПІІК);
провести навчання і підготовку інструкторів і спостерігача(ів);
співпрацювати з громадськими об’єднаннями, що проводять діяльність у напрямку гігієни рук в ЗОЗ/ЗСЗ;
3) почати із розміщення інформаційних стендів або плакатів для підвищення обізнаності працівників та відвідувачів ЗОЗ/ЗСЗ.
6. ЗОЗ/ЗСЗ, які реалізували п’ять поспіль річних планів дій із впровадження гігієни рук, необхідно:
1) підготувати довгостроковий план дій із зазначенням ключових завдань, що дозволять підтримувати культуру безпеки в ЗОЗ/ЗСЗ (із врахуванням гігієни рук);
2) включити оцінювання гігієни рук до інструментів визначення якості надання медичної допомоги;
3) встановити рівень самооцінки з гігієни рук, яких планується досягти в наступні декілька років, із урахуванням місцевого контексту;
4) розробити та затвердити систему заохочень та винагород для якнайкращого дотримання практики гігієни рук;
5) в співпраці із громадськими об’єднаннями розробити та запровадити програму інформування та популяризації гігієни рук на рівні ЗОЗ/ЗСЗ і регіональному/національному рівнях, яка може включати в себе наступне:
опитування пацієнтів для визначення їхнього відношення до гігієни рук та думок щодо можливого їх залучення до популяризації практик гігієни рук;
ініціацію до пропаганди гігієни рук (наприклад, інформаційні стенди на вході у ЗОЗ/ЗСЗ);
навчання пацієнтів визначенню моментів, коли є необхідність працівнику провести гігієну рук.
VII. Етапи впровадження
1. Покроковий підхід допомагає розробити і спланувати покращення гігієни рук в хронологічному порядку та з раціональною послідовністю дій.
На початку ЗОЗ/ЗСЗ необхідно зосередитися на реалізації невеликих цілей із наступним поступовим розширенням. Мінімальні критерії, що необхідні для реалізації ММС з покращення гігієни рук, наведені в додатку 13 до цієї Інструкції.
2. Підготовчий етап (крок 1) забезпечує готовність ЗОЗ/ЗСЗ до початку впровадження покращення гігієни рук.
Цей крок включає:
1) отримання необхідних ресурсів (фінансових і кадрових), визначення та затвердження кандидатур координатора з гігієни рук та його помічників (інструкторів/тренерів і дослідників/спостерігачів, спеціаліста зі збору та аналізу даних), визначення індивідуальних завдань та очікуваних результатів;
2) планування із визначенням стратегії дій (примірний план дій з покращення гігієни рук в ЗОЗ/ЗСЗ наведено у додатку 14 до цієї Інструкції):
складання плану реалізації кожного або лише декількох із основних компонентів ММС із покращення гігієни рук, із врахуванням місцевого контексту;
прийняття рішення про масштаби і ступінь реалізації (зосередитися на реалізації програми на рівні одного або декількох підрозділів, чи на рівні всього ЗОЗ/ЗСЗ);
3) узгодження заходів і дій з наявними людськими та фінансовими ресурсами. У випадках нестачі фінансових ресурсів проводиться економічний аналіз з метою визначення найбільш ефективного та економічно обґрунтованого шляху реалізації заходів;
4) навчання і підготовка тренерів та спостерігачів для проведення заходів, які пов’язані з навчанням і підготовкою, моніторингом і оцінкою;
5) ознайомлення з усіма протоколами для проведення оцінювання та зворотного зв’язку, розробка і затвердження плану проведення опитувань та оцінювань.
3. Для виконання підготовчого етапу (крок 1) залучаються:
1) керівник ВІК, фахівці/спеціалісти ВІК (для ЗОЗ, що надають цілодобову стаціонарну допомогу);
2) координатор з гігієни рук та його заступник (за наявності);
3) інструктори/тренери з гігієни рук;
4) спостерігач(і)/дослідник(и) з гігієни рук;
5) спеціаліст зі збору та аналізу даних/статистик;
6) керівництво ЗОЗ/ЗСЗ (керівник і його заступник, заступник з медичних питань ЗОЗ/медичний директор);
7) керівники підрозділів та старші сестри медичні ЗОЗ, провідні спеціалісти;
8) структурний підрозділ із закупівель;
9) фармацевтичний/аптечний підрозділ (для ЗОЗ, що надають цілодобову стаціонарну допомогу).
4. Тривалість підготовчого етапу (крок 1) може складати близько двох місяців (може бути зменшена, якщо в ЗОЗ/ЗСЗ вже впроваджувались системні заходи з гігієни рук, або збільшена, наприклад, в разі необхідності проведення навчання для координатора з гігієни рук).
5. Показниками виконання підготовчого етапу (кроку 1) є:
1) визначений координатор з гігієни рук, інструктори/тренери та спостерігачі, спеціаліст зі збору та аналізу даних;
2) визначені зацікавлені сторони для реалізації заходів із гігієни рук;
3) проведено аналіз ризиків реалізації ММС;
4) проведено аналіз бюджету;
5) план дій узгоджений із всіма зацікавленими сторонами та затверджений керівництвом ЗОЗ/ЗСЗ;
6) інструктори/тренери і спостерігач(і)/дослідник(и) пройшли необхідні навчання і підготовку;
7) визначений постачальник засобів для гігієни рук, з ним укладений договір, в бюджеті ЗОЗ/ЗСЗ виділені кошти для виконання цього договору;
8) закуплені та наявні в достатній кількості витратні матеріали для гігієни рук, в тому числі антисептик для рук;
засоби для гігієни рук наявні у всіх точках догляду ЗОЗ/ЗСЗ.
6. На етапі базової оцінки (крок 2) проводиться оцінка практики гігієни рук в ЗОЗ/ЗСЗ, сприйняття працівниками необхідності гігієни рук, знань працівників та наявних інфраструктури і ресурсів.
Цей крок включає:
1) оцінки наявної інфраструктури і ресурсів, сприйняття керівництвом ЗОЗ/ЗСЗ і працівниками гігієни рук, дотримання правил гігієни рук працівниками, використання засобів для гігієни рук, переносимості і прийнятності антисептику для рук (додатки 4, 6, 7, 10, 11, до цієї Інструкції);
2) аналіз отриманих даних одразу після проведеного оцінювання;
3) оцінка результатів та перевірка їх достовірності;
4) формування звіту та його розповсюдження серед ключових зацікавлених сторін із впровадження гігієни рук;
5) планування та визначення дій, що будуть виконані на етапі реалізації, із врахуванням проведеного аналізу (наприклад, затвердження плану лекцій та практичних занять, визначення конкретних дій щодо покращення інфраструктури);
6) оцінка розповсюдженості ІПНМД за останні шість або дванадцять місяців в ЗОЗ/ЗСЗ в цілому або у окремо взятому підрозділі;
7) завершення навчання інструкторів/тренерів;
8) перегляд навчальних матеріалів і підготовка додаткових навчальних матеріалів із включенням даних звіту за результатами оцінювання;
9) підготовка інформаційних матеріалів (стенди, плакати, листівки тощо), які будуть використані на етапі реалізації;
10) завершення закупівель антисептиків для рук;
11) підготовка до змін в практиці надання медичної допомоги (наприклад, встановлення раковин, диспенсерів для рідкого мила і антисептику для рук, закритих диспенсерів для одноразових паперових рушників).
7. Для виконання етапу базової оцінки залучаються наступні фахівці:
1) координатор з гігієни рук та його заступники (при наявності);
2) інструктори/тренери з гігієни рук;
3) спостерігачі з гігієни рук;
4) фармацевт аптечного підрозділу (для ЗОЗ);
5) фахівці підрозділу закупівель ЗОЗ/ЗСЗ;
6) працівники підрозділу статистики/спеціаліст зі збору та аналізу даних;
7) епідеміолог ВІК (для ЗОЗ, що надають цілодобову стаціонарну допомогу).
8. Тривалість етапу базової оцінки (крок 2) може складати близько трьох місяців (може бути зменшена або подовжена в залежності від кількості підрозділів, в яких заплановане впровадження покращення гігієни рук). Примірний графік проведення базової оцінки наведено у додатку 8 до цієї Інструкції, вказані у ньому строки є орієнтовними і можуть бути скореговані в залежності від місцевого контексту.
9. Показниками виконання етапу базової оцінки (крок 2) є:
1) проведено базову оцінку інфраструктури і ресурсів;
2) проведено базову оцінку сприйняття гігієни рук серед керівництва та працівників ЗОЗ/ЗСЗ;
3) проведено базову оцінку використання засобів для гігієни рук;
4) проведено базову оцінку дотримання працівниками правил гігієни рук;
5) проведено базову оцінку знань працівників щодо гігієни рук;
6) отримані дані базових оцінок введені та проаналізовані, їх достовірність підтверджена;
7) забезпечена наявність антисептиків для рук в достатній кількості;
8) проведено оцінку переносимості і прийнятності антисептику для рук (метод 1 або 2);
9) інструктори/тренери з гігієни рук завершили навчання;
10) підготовлено інформаційні та навчальні матеріали з урахуванням результатів етапу базової оцінки (кроку 2).
10. Етап реалізації (крок 3) є ключовим етапом для досягнення покращення гігієни рук в ЗОЗ/ЗСЗ і складається із дій, які були заплановані на підготовчому етапі (крок 1) та відкориговані після етапу базової оцінки (крок 2).
Цей етап включає наступне:
1) проведення офіційного заходу із залученням всіх співробітників ЗОЗ/ЗСЗ, для роз’яснення необхідності впровадження покращення гігієни рук і демонстрації прихильності керівництва ЗОЗ/ЗСЗ;
2) забезпечення доступності антисептиків для рук в усіх точках догляду у всіх підрозділах, де впроваджується покращення гігієни рук;
3) проведення оцінки переносимості і прийнятності антисептику для рук (додаток 7 до цієї Інструкції), якщо не була проведена на етапі базової оцінки;
4) розміщення інформаційних плакатів, бюлетенів і стендів, роздача листівок, розповсюдження інших інформаційних матеріалів щодо правил гігієни рук та необхідності їх дотримання;
5) організація навчальних занять для всіх працівників, які працюють в підрозділах та беруть участь у впровадженні покращення гігієни рук (проведення практичних занять, в тому числі біля ліжка хворого, лекцій, семінарів, тренінгів тощо);
6) оцінка знань працівників щодо гігієни рук, якщо не була проведена на етапі базової оцінки;
7) поточне оцінювання наявної інфраструктури і ресурсів, використання засобів для гігієни рук, дотримання правил гігієни рук (додатки 4, 6, 11 до цієї Інструкції) та знань працівників;
8) організація регулярних зустрічей для моніторингу реалізації заходів, обговорення поточної ситуації та корекції плану дій при необхідності.
11. Для успішного виконання етапу реалізації (крок 3) здійснюється координація дій наступних фахівців:
1) координатор з гігієни рук та його заступники (при наявності);
2) інструктори/тренери з гігієни рук;
3) спеціаліст зі збору та аналізу даних;
4) керівництво ЗОЗ/ЗСЗ;
5) керівники та старші сестри медичні підрозділів;
6) фахівці ВІК (для ЗОЗ, що надають цілодобову стаціонарну допомогу);
7) керівник аптечного підрозділу (для ЗОЗ) і представник підрозділу закупівель;
8) представники громадських об’єднань (за згодою).
12. Тривалість етапу реалізації (крок 3) складає близько трьох місяців (може бути подовжена в залежності від кількості підрозділів, в яких заплановане впровадження покращення гігієни рук).
13. Показниками виконання етапу реалізації (кроку 3) є:
1) план дій, розроблений на етапі кроку 1 та скоригований на етапі кроку 2, використовується в процесі реалізації;
2) звіт (із обов’язковим зазначенням аналізу даних) за результатами базової оцінки направлений всім зацікавленим сторонам;
3) розміщені та розповсюджені інформаційні матеріали (плакати, стенди, бюлетені, листівки тощо);
4) розповсюджені навчальні матеріали (СОП, протоколи, відеоролики, статті тощо);
5) проведені навчання і підготовка;
6) проводяться щомісячні (в перший рік впровадження) або щоквартальні (в наступні роки) оцінки використання засобів для гігієни рук (додаток 6 до цієї Інструкції);
7) проведено оцінку переносимості і прийнятності антисептику для рук (додаток 7 до цієї Інструкції);
8) проводяться щомісячні (мінімум щорічні) оцінки дотримання працівниками правил гігієни рук (додаток 11 до цієї Інструкції);
9) проводяться регулярні ознайомчі зібрання з питань впровадження покращення гігієни рук із залученням всіх зацікавлених сторін.
14. На етапі оцінки впливу (крок 4) здійснюється моніторинг та аналіз прогресу і підтвердження того, що реалізація заходів призводить до покращення гігієни рук. Всі заходи, які були розпочаті на етапі реалізації (крок 3), продовжуються на етапі оцінки впливу (крок 4), особлива увага приділяється зворотному зв’язку, з метою продовження виконання плану дій та можливої його корекції.
Етап оцінки впливу включає наступне:
1) оцінка наявної інфраструктури і ресурсів, сприйняття керівництвом ЗОЗ/ЗСЗ і працівниками гігієни рук, дотримання правил гігієни рук працівниками, використання засобів для гігієни рук (додатки 4, 6, 10, 11 до цієї Інструкції);
2) аналіз отриманих даних одразу після проведених оцінок;
3) оцінювання результатів оцінок та перевірка їх достовірності;
4) проведення заходів, які направлені на покращення гігієни рук та розпочаті на етапі реалізації (крок 3), у відповідності до потреб ЗОЗ/ЗСЗ і затвердженого плану дій.
Оцінки, які були проведені на етапі базової оцінки (крок 2), повторюються на етапі оцінки впливу (крок 4) у визначені планом терміни (визначається термін, який є достатнім для реалізації запланованого заходу). Оскільки такий моніторинг проводиться одразу після реалізації заходів, він визначає лише безпосередній вплив. Для оцінки довгострокового впливу проводиться аналіз на основі оцінок, проведених протягом періоду не менше п’яти років.
15. Для виконання етапу оцінки впливу (крок 4) залучаються наступні фахівці:
1) координатор з гігієни рук та його заступники (при наявності);
2) спостерігачі/дослідники з гігієни рук;
3) спеціаліст зі збору та аналізу даних;
4) працівник підрозділу закупівель;
5) фахівці ВІК (для ЗОЗ, що надають цілодобову стаціонарну допомогу).
16. Тривалість етапу оцінки впливу складає близько двох місяців (може бути подовжена в залежності від кількості підрозділів, в яких відбувається впровадження покращення гігієни рук). У додатку 9 до цієї Інструкції наведено примірний план-графік проведення оцінки впливу впровадження покращення гігієни рук, вказані у ньому строки є орієнтовними і можуть корегуватися в залежності від місцевого контексту.
17. Показниками виконання етапу оцінки впливу (крок 4) є:
1) проведено оцінку наявної інфраструктури і ресурсів (додаток 4 до цієї Інструкції);
2) проведено оцінку сприйняття гігієни рук серед керівництва та працівників ЗОЗ/ЗСЗ (додаток 10 до цієї Інструкції);
3) оцінка використання засобів для гігієни рук проводиться щомісячно (на першому році впровадження) або щоквартально (у наступні роки) (додаток 6 до цієї Інструкції);
4) проведено оцінку дотримання працівниками правил гігієни рук (додаток 11 до цієї Інструкції);
5) проведено оцінку знань працівників щодо гігієни рук;
6) отримані дані оцінок введені та проаналізовані, їх достовірність підтверджена;
7) реалізація плану дій продовжується.
18. На етапі розробки довгострокового плану (крок 5) проводиться перегляд всіх проведених заходів з покращення гігієни рук, з метою розробки п’ятирічного плану дій для забезпечення подальшого прогресу і стійкого покращення гігієни рук. Довгостроковий план дій рекомендується розробляти не раніше, ніж через п’ять років від початку впровадження покращення гігієни рук. Розробка і наступна реалізація довгострокового плану дозволить забезпечити формування культури дотримання гігієни рук і, таким чином, культури безпеки в ЗОЗ/ЗСЗ.
19. Етап розробки довгострокового плану дій (крок 5) включає наступне:
1) аналіз результатів базової і наступних оцінок та оцінки впливу для досягнення ключових показників успіху, наведених в пункті 11 розділу V цієї Інструкції;
2) визначення областей, які потребують подальшого покращення;
3) підготовка звіту із детальним описом всього процесу впровадження, оцінкою впливу, зазначенням існуючих проблем та варіантів їх усунення;
4) визначення способу поширення результатів оцінки впливу (наприклад, направлення звіту в письмовій або електронній формі, організація зустрічі із запрошенням всіх зацікавлених сторін);
5) залучення керівництва ЗОЗ/ЗСЗ до розробки і реалізації довгострокового плану дій (заручення підтримкою для впровадження подальших заходів);
6) приведення у відповідність інфраструктури і ресурсів (в тому числі людських) до запланованих заходів із покращення гігієни рук;
7) підготовка, доопрацювання і затвердження довгострокового плану дій;
8) підготовка, доопрацювання і затвердження кошторису заходів;
9) зазначення в кошторисі заходів можливих непередбачуваних витрат із вказанням шляхів їх фінансування;
10) розробка та затвердження графіку проведення моніторингу, оцінки і зворотного зв’язку;
11) розробка системи оцінки даних з метою координації планів дій, що реалізуються відповідно до ММС ПІІК в ЗОЗ;
12) розробка та впровадження системи звітності у підрозділах, із зазначенням залучених співробітників, задач та протоколів моніторингу, графіку проведення оцінки та зворотного зв’язку;
13) створення або залучення зовнішньої моніторингової групи (громадські об’єднання, представники ВІК/координатор з гігієни рук іншого ЗОЗ/ЗСЗ тощо) для підтвердження достовірності даних оцінювання;
14) винайдення чемпіонів і лідерів думки та співпраця з ними;
15) розробка плану взаємодії із регіональними, національними та міжнародними організаціями, які займаються покращенням гігієни рук, з метою обміну досвідом і стимуляції розширення масштабів заходів, що реалізуються в ЗОЗ/ЗСЗ;
16) визначення способів комунікації та популяризації гігієни рук поза межами ЗОЗ/ЗСЗ (наприклад, засоби масової інформації).
20. Для розробки і реалізації довгострокового плану дій необхідна координація дій наступних фахівців:
1) координатор з гігієни рук та його заступники (при наявності);
2) інструктори/тренери з гігієни рук;
3) спостерігачі/дослідники з гігієни рук;
4) працівники підрозділу статистики/спеціаліст зі збору та аналізу даних;
5) керівники та старші сестри медичні підрозділів ЗОЗ /керівники підрозділів ЗСЗ;
6) керівництво ЗОЗ/ЗСЗ;
7) керівник, епідеміолог та спеціалісти ВІК (для ЗОЗ, що надають цілодобову стаціонарну допомогу);
8) представники громадських об’єднань (за згодою).
21. Довгостроковий план дій може включати наступні заходи:
1) щодо зміни в системі:
складання графіку оцінок наявної інфраструктури і ресурсів через регулярні, заздалегідь визначені періоди часу, надання отриманої за результатами оцінок інформації зацікавленим сторонам і внесення змін до плану дій при необхідності;
створення системи забезпечення постійної наявності і доступності засобів для гігієни рук, у тому числі антисептиків для рук, в усіх точках догляду ЗОЗ/ЗСЗ;
2) щодо навчання і підготовки:
розроблення плану дій для працівників з перевірки компетентності один одного після навчальних сесій (із обов’язковим зазначенням інструментів, які повинні використовуватися), впровадження, проведення періодичної оцінки правильності використання та ефективності такого плану дій;
створення системи пошуку нових інструкторів/тренерів та спостерігачів;
розроблення графіку регулярних зустрічей із працівниками ВІК та інструкторами/тренерами з гігієни рук задля перегляду та вдосконалення навчальних програм;
збір відгуків про способи подачі інформації, що використовуються, під час навчальних сесій для того щоб визначити найефективніші;
залучення зовнішніх консультантів задля проведення оцінки, вдосконалення та впровадження інноваційних методів до навчальної програми;
3) щодо нагадування на робочому місці:
збір пропозицій працівників ЗОЗ/ЗСЗ, громадських об’єднань щодо адаптації наявних та ідей для нових нагадувань на робочому місці і складання плану по їх розробці та виготовленню;
визначення працівників ЗОЗ/ЗСЗ, відповідальних за належний стан нагадувань на робочих місцях;
4) щодо моніторингу, оцінки і зворотного зв’язку:
підготовка плану щомісячного моніторингу наявної інфраструктури і ресурсів та дотримання правил гігієни рук працівниками в підрозділах ЗОЗ/ЗСЗ;
підготовка плану періодичної оцінки знань та сприйняття серед працівників щодо гігієни рук у відповідності до графіку проведення навчальних сесій;
регулярне звітування про результати проведених оцінок всім зацікавленим сторонам із обов’язковим зазначенням покращень, які були досягнуті;
проведення моніторингу розповсюдженості ІПНМД в ЗОЗ;
проведення щорічного аналізу динаміки показників розповсюдженості ІПНМД у тих підрозділах ЗОЗ, в яких впроваджено покращення гігієни рук;
створення системи безперервного обліку та звітності (щомісячне оцінювання) щодо використання засобів для гігієни рук, особливо антисептиків для рук, для розрахунку щорічних тенденцій;
5) щодо культури дотримання гігієни рук:
включення оцінки дотримання правил гігієни рук в список показників для визначення якості надання медичних послуг (наприклад, шляхом підготовки мотиваційного листа із довідковою інформацією щодо необхідності дотримання гігієни рук, планами заходів, результатами проведених оцінок і потенційних переваг наявності відповідних показників серед показників якості);
створення системи розробки, перегляду і затвердження щорічних планів дій ЗОЗ/ЗСЗ із врахуванням думки пацієнтів, їх громадських об’єднань, визначенням способів оприлюднення рекомендацій, пропозицій та затверджених планів;
затвердження графіку презентацій та/або відкритих нарад із участю громадських об’єднань, для їх сприяння формуванню культури безпеки в ЗОЗ/ЗСЗ;
створення системи мотивацій для працівників.
22. Тривалість етапу розробки довгострокового плану (крок 5) складає близько двох місяців (може бути подовжена в залежності від місцевого контексту).
23. Показниками виконання етапу розробки довгострокового плану (крок 5) є:
1) проведений аналіз оцінок та оцінки впливу;
2) затверджено графік проведення зустрічей із всіма зацікавленими сторонами для обговорення поточної ситуації щодо гігієни рук в ЗОЗ/ЗСЗ;
3) області, що потребують подальшого вдосконалення, визначені, а методи усунення проблем затверджені (в тому числі заплановано фінансування);
4) визначені та використовуються на постійній основі методи зворотного зв’язку із всіма зацікавленими сторонами;
5) розроблений та затверджений довгостроковий план дій (або плани дій, у разі впровадження в окремих підрозділах) із зазначенням графіку проведення оцінювання і наступного можливого перегляду;
6) кошторис запланованих заходів затверджений і в ньому зазначені шляхи фінансування в разі появи неочікуваних витрат;
7) дати проведення зустрічей в наступному році заплановані та доведені до відома всіх зацікавлених сторін.
24. Популяризація і моніторинг гігієни рук не повинні завершуватися після реалізації заходів відповідно до планів дій — після виконання плану дій на відповідний період має виконуватись план дій на наступний період.
25. Стратегія покращення гігієни рук не може залишатися незмінною, її потрібно оновлювати через певні проміжки часу або після отримання нових наукових (доказових) даних. При внесенні змін, відповідно до довгострокового плану дій, весь цикл заходів необхідно повторювати протягом мінімум п’яти років із використанням покрокового підходу відповідно до цього розділу.
Генеральний директор Директорату громадського здоров’я
та профілактики захворюваності
І. Руденко
Додаток 1
до Інструкції з впровадження покращення гігієни рук
в закладах охорони здоров’я та установах / закладах надання
соціальних послуг / соціального захисту населення
(пункт 2 розділу I, підпункт 2 пункту 6 розділу I,
пункт 8 розділу I, пункт 1 розділу III, підпункт 5
пункту 8 розділу III)
Правила і практики гігієни рук
I. Показання і способи гігієни рук
1. П’ять показань до проведення гігієнічної обробки рук.
Дотримуватися гігієнічної обробки рук необхідно за всіх зазначених на Схемі 1 показань, незалежно від того, використовуються рукавички чи ні (якщо використовуються рукавички, гігієнічна обробка рук проводиться виключно після їх зняття).
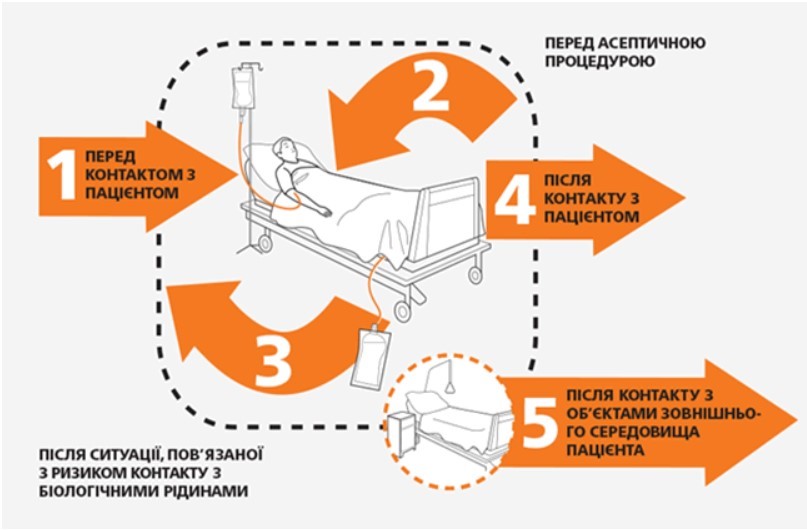
Схема 1. П’ять показань до проведення гігієнічної обробки рук
2. Руки стають факторами передавання в наступних випадках:
1) при догляді за одним пацієнтом у випадках переносу із однієї ділянки шкіри до іншої (ділянка А пацієнта — руки працівника — ділянка Б пацієнта);
2) при догляді за декількома пацієнтами — від одного пацієнта до іншого (пацієнт А — руки працівника — пацієнт Б);
3) при контакті із об’єктами навколишнього середовища, що забруднені мікроорганізмами (об’єкт навколишнього середовища — руки працівника — пацієнт або пацієнт — руки працівника А — об’єкт навколишнього середовища — руки працівника Б — пацієнт);
4) при контакті брудними (контамінованими мікроорганізмами) руками із медичним обладнанням (наприклад, інструментарієм) та лікарськими засобами (руки працівника — інструментарій — пацієнт).
3. Показання до практики з гігієнічної обробки рук:
1) до контакту із пацієнтом;
2) до асептичних процедур;
3) після ситуації, що пов’язана із ризиком контакту/контактом з біологічними рідинами;
4) після контакту із пацієнтом;
5) після контакту із об’єктами внутрішнього середовища ЗОЗ/ЗСЗ, що перебувають у безпосередній близькості із пацієнтом.
4. Необхідно дотримуватися наступних вимог:
1) до контакту із пацієнтом:
гігієнічна обробка рук призначена для захисту (запобігання інфікуванню/колонізації) пацієнта від потенційно небезпечних мікроорганізмів, які знаходяться на руках працівників;
після виконання практики гігієнічної обробки рук заборонено торкатися до будь-яких об’єктів внутрішнього середовища ЗОЗ/ЗСЗ;
якщо контакт із пацієнтом потребує одягання рукавичок, гігієнічна обробка рук проводиться до їх одягання (рукавички одягаються на повністю висохлі руки, після одягання рукавичок заборонено торкатися до будь-яких об’єктів внутрішнього середовища ЗОЗ/ЗСЗ).
Наступні ситуації є обов’язковими для виконання практики гігієнічної обробки рук до контакту із пацієнтом:
перед рукостисканням та перед тим, як доторкнутися до дитини;
перед тим, як допомогти пацієнту провести особисту гігієну, прийняти їжу, одягнутися, прийняти ванну тощо;
перед наданням допомоги неінвазивними видами лікування (наприклад, застосування кисневої маски, проведення масажу);
перед проведенням неінвазивного фізикального обстеження: вимірювання пульсу та артеріального тиску, аускультація органів грудної клітини, запис ЕКГ тощо;
2) до асептичних процедур:
гігієнічна обробка рук призначена для захисту від проникнення в організм пацієнта потенційно небезпечних мікроорганізмів, в тому числі через опосередкований контакт при забрудненні (контамінації мікроорганізмами) стерильних об’єктів внутрішнього середовища ЗОЗ/ЗСЗ (обладнання, інструментарію, матеріалів, лікарських засобів тощо);
практику з гігієнічної обробки рук необхідно виконувати безпосередньо перед контактом з біотопами, з якими пов’язаний ризик інфікування пацієнта (наприклад, слизові оболонки, пошкоджена шкіра, інвазивний медичний пристрій).
Наступні ситуації є обов’язковими для виконання практики гігієнічної обробки рук до асептичної процедури:
перед чищенням зубів пацієнта, закапуванням очних крапель, перед проведенням пальцьового вагінального або ректального обстежень, перед обстеженням порожнин рота, носа та вух із застосуванням або без інструментів, перед введенням супозиторію/маткового кільця, перед відсмоктуванням слизу;
перед перев’язуванням рани із застосуванням або без інструментів, перед нанесенням мазі на пухир, перед черезшкірною ін’єкцією/пункцією;
перед введенням інвазивного медичного пристрою (назальні канюлі, назогастральна та ендотрахеальна трубки, сечовий та внутрішньовенний катетери, дренажна трубка);
перед тим, як роз’єднати/відкрити контур інвазивного медичного пристрою (наприклад, з метою введення їжі або ліків, з метою дренування, відсмоктування або моніторингу);
перед приготуванням їжі, підготовкою лікарських засобів і стерильних матеріалів;
3) після ситуації, що пов’язана із ризиком контакту з біологічними рідинами:
гігієнічна обробка рук призначена для захисту працівників від колонізації або інфікування потенційно небезпечними мікроорганізмами пацієнта і попередження забруднення внутрішнього середовища ЗОЗ/ЗСЗ;
практика гігієнічної обробки рук виконується одразу після завершення процедури, що пов’язана із ризиком контакту із біологічними рідинами (наприклад, після спорожнення сечоприймача);
якщо контакт був при одягнених рукавичках, практику гігієни рук необхідно провести після їх зняття (рукавички слід викинути не торкаючись ними навколишніх об’єктів).
Наступні ситуації є обов’язковими для виконання практики гігієни рук після ситуації, що пов’язана із ризиком контакту з біологічними рідинами:
після контакту зі слизовими оболонками і пошкодженою шкірою;
після черезшкірної ін’єкції або пункції;
після введення інвазивного медичного пристрою (судинний доступ, катетер, трубка, дренаж тощо) та після того, як відбулося роз’єднання і відкриття контуру інвазивного пристрою;
після видалення інвазивного медичного пристрою;
після видалення будь-якого матеріалу, що забезпечував захист (серветки, перев’язочний матеріал, марля, жіночі прокладки тощо);
після роботи із лабораторним зразком, що містить органічну речовину, після змивання виділень і біологічних рідин, після очищення будь-яких забруднених поверхонь і матеріалів (забруднена постільна білизна, зубні протези, інструменти, сечоприймачі, підкладні судна тощо);
4) після контакту із пацієнтом:
гігієнічна обробка рук призначена для захисту працівників від колонізації або інфікування потенційно небезпечними мікроорганізмами пацієнта та попередження забруднення внутрішнього середовища ЗОЗ/ЗСЗ;
практика з гігієнічної обробки рук після контакту із пацієнтом проводиться безпосередньо в точці догляду;
до проведення гігієни рук заборонено торкатися до будь-яких об’єктів, включно із об’єктами, що знаходяться у безпосередній близькості до пацієнта;
якщо контакт потребував використання рукавичок, гігієнічну обробку рук необхідно проводити після їх зняття (рукавички слід викинути не торкаючись ними навколишніх об’єктів).
Наступні ситуації є обов’язковими для виконання практики гігієни рук після контакту з пацієнтом:
після рукостискання та після доторку до дитини;
після допомоги пацієнту (допомога в пересуванні, прийнятті ванни, одяганні, прийнятті їжі тощо);
після виконання неінвазивних видів лікування (застосування кисневої маски, проведення масажу тощо);
після заміни постільної білизни, коли пацієнт у ліжку;
після неінвазивного фізикального обстеження (після вимірювання пульсу та артеріального тиску, аускультації органів грудної клітини, запису ЕКГ тощо);
5) після контакту із об’єктами внутрішнього середовища ЗОЗ/ЗСЗ, що перебувають у безпосередній близькості до пацієнта:
гігієнічна обробка рук призначена для захисту працівників від колонізації або інфікування потенційно небезпечними мікроорганізмами, які можуть бути присутні на поверхнях або предметах в оточенні пацієнта і попередження забруднення внутрішнього середовища ЗОЗ/ЗСЗ;
практика гігієнічної обробки рук після контакту із об’єктами внутрішнього середовища ЗОЗ/ЗСЗ, що перебувають у безпосередній близькості до пацієнта проводиться у всіх випадках, якщо працівник доторкувався до об’єктів внутрішнього середовища ЗОЗ/ЗСЗ в оточенні пацієнта, навіть коли не мав місце безпосередній контакт із пацієнтом (наприклад, зміна постільної білизни).
Наступні ситуації є обов’язковими для виконання практики гігієнічної обробки рук після контакту із об’єктами внутрішнього середовища ЗОЗ/ЗСЗ, що перебувають у безпосередній близькості до пацієнта:
після видів діяльності, що включають фізичний контакт із предметами в безпосередній близькості до пацієнта (заміна постільної білизни у відсутності пацієнта, пересування візка, прибирання на приліжковій тумбі тощо);
після лікувальних процедур (наприклад, корекція швидкості перфузії) і перевірки сигнальних пристроїв;
після інших контактів із поверхнями або предметами (наприклад, доторкування у намаганні спертися на ліжко або приліжкову тумбу; необхідно намагатися уникати цих необов’язкових дій).
5. Способи гігієни рук в залежності від показань:
1) необхідно мити руки із милом та водою у випадках:
руки видимо забруднені;
перед вживанням їжі;
після приходу в ЗОЗ/ЗСЗ та по закінченню робочої зміни;
руки забруднені кров’ю або іншими біологічними рідинами;
після відвідування туалету;
якщо ви сумніваєтеся у їх чистоті;
у випадках високого ризику забруднення спороутворюючими мікроорганізмами (спалахи захворювань, що викликані C. difficile) та норовірусами;
у всіх випадках необхідності практики гігієни рук, але недоступності антисептику для рук;
2) необхідно провести гігієнічну обробку рук:
до і після контакту із пацієнтом;
до того як доторкнутися до інвазивного приладу для догляду за пацієнтом, в незалежності від того, використовуєте ви рукавички чи ні;
після потенційного контакту із біологічними рідинами або виділеннями;
після контакту із слизовими оболонками, непошкодженими ділянками шкіри або пов’язкою;
якщо при огляді одного пацієнта ви переходите від забрудненої (контамінованої мікроорганізмами) частини тіла до незабрудненої;
після контакту із предметами (включно із медичним обладнанням), що знаходяться у безпосередній близькості до пацієнта (в зоні пацієнта);
після зняття стерильних або нестерильних (оглядових) рукавичок;
після контакту із собою — доторкування до носа, прикритті роту при кашлі і чханні, контакті із медичним одягом;
після зняття засобів індивідуального захисту (захисний одяг, маски, респіратори тощо);
3) до роботи із медикаментами або перед приготуванням їжі необхідно провести гігієнічну обробку рук або вимити руки із звичайним/антибактеріальним милом і водою;
4) мило і антисептик для рук не повинні використовуватися одночасно.
6. При прямих контактах із пацієнтами заборонено мати нарощені або штучні нігті, покривати нігті будь-яким лаком.
7. Нігті мають бути короткими — кінчик не більше 0,5 см.
II. Техніка гігієни рук
1. Гігієнічна обробка рук:
1) налити 3 мл антисептику для рук і покрити ним всі поверхні рук;
2) розтирати руки до повного висихання;
3) техніка та етапи гігієнічної обробки рук наведені на Схемі 2 нижче.
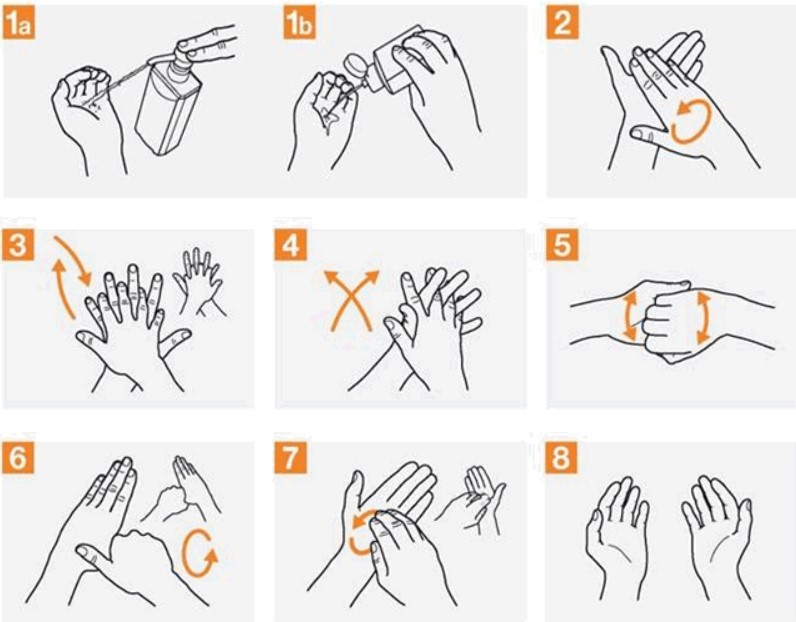
Схема 2. Гігієнічна обробка рук
2. Миття рук з милом та водою:
1) змочити руки водою та нанести необхідну кількість мила, аби покрити ним всі поверхні рук, але не менше 1 мл;
2) уникайте використання гарячої води, так як це може збільшити ризик розвитку дерматиту;
3) техніка та етапи миття рук з милом та водою наведені на Схемі 3 нижче;
4) ополосніть руки проточною водою і ретельно витріть одноразовим паперовим рушником;
5) використаним паперовим рушником закрийте кран.
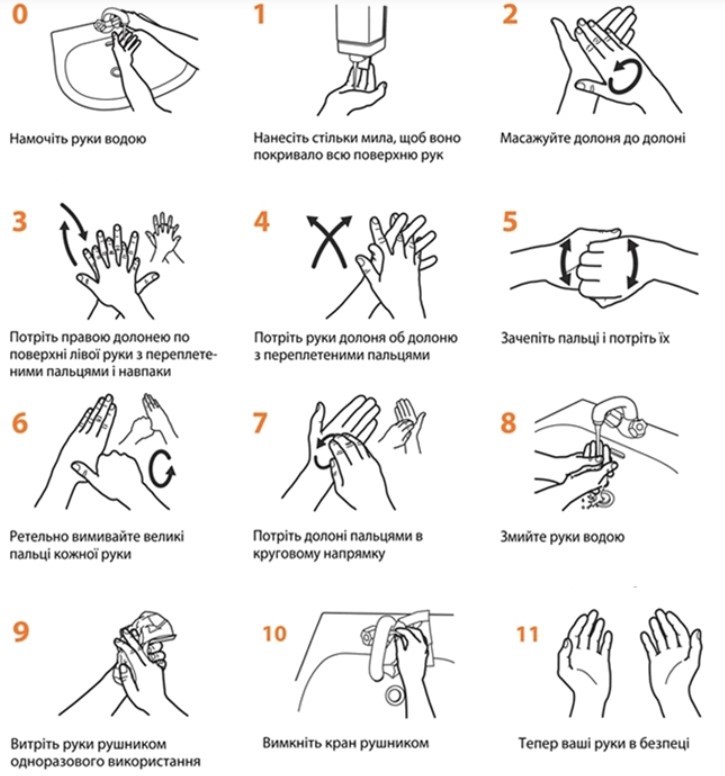
Схема 3. Миття рук з водою та милом
3. Хірургічна обробка рук:
1) загальні вимоги, яких необхідно дотримуватися для проведення якісної хірургічної обробки рук:
хірургічну обробку рук слід провести до одягання одноразової шапочки захисної від інфекційних агентів та медичної (хірургічної) маски, шляхом їх миття з милом і водою із залученням передпліччя та зап’ястків;
перед початком процедури слід зняти кільця, наручні годинники і браслети до того як приступити до гігієни рук та видалити бруд з-під нігтів, використовуючи нігтьочистку, під проточною водою;
штучні та нарощені нігті заборонені;
раковини необхідно спроектувати так, аби кількість бризків була мінімальною (струмінь води має бути направленим у стік);
використовувати щітки для миття рук не рекомендовано;
заборонено використовувати хірургічний скраб для рук;
до надягання стерильних рукавичок необхідно виконати хірургічну обробку рук із використанням антисептику для рук, що містить інгредієнти, які забезпечують довготривалий ефект (наприклад, хлоргексидин) відповідно до Схеми 4 нижче;
необхідно дотримуватися інструкцій виробника по часу експозиції при використанні антисептика;
наносити антисептик слід лише на сухі руки;
при використанні антисептику для рук необхідно використовувати достатню кількість засобу, аби руки та передпліччя під час хірургічної обробки залишалися вологими, але не менше 10 мл на одну обробку.
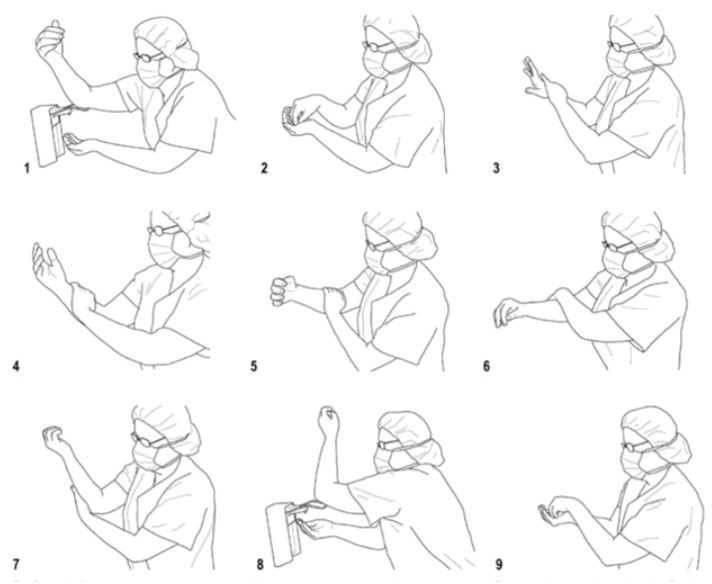
Схема 4. Хірургічна обробка рук
2) етапи хірургічної обробки рук (відповідно до рисунків Схеми 4, що наведені вище):
1 — налити 5 мл антисептику в долоню лівої руки, використовуючи лікоть правої руки для натискання на ручку диспенсера;
2 — вмочити пальці правої руки в антисептик і тримати їх 5 секунд;
3 — 7 — провести обробку шкіри передпліччя до ліктя (наносити антисептик слід круговими рухами охоплюючи всю поверхню шкіри; обробка проводиться до повного висихання антисептику — 10 — 15 секунд);
8 — налити 5 мл антисептику в долоню правої руки, використовуючи лікоть лівої руки для натискання на ручку диспенсера;
9 — вмочити пальці лівої руки в антисептик і тримати їх 5 секунд;
10 — провести обробку шкіри передпліччя до ліктя (наносити антисептик слід круговими рухами охоплюючи всю поверхню шкіри; обробка проводиться до повного висихання антисептику — 10 — 15 секунд);
11 — налити 3 — 5 мл антисептику в долоню, використовуючи лікоть іншої руки для натискання на ручку диспенсера;
12 — 16 — провести обробку рук дотримуючись стандартної процедури;
17 — після проведення обробки можуть бути одягнені стерильний хірургічний одяг і медичні рукавички.
III. Основні практики гігієнічної обробки рук в амбулаторно-поліклінічних ЗОЗ та ЗСЗ
1. Ключові аспекти, що необхідно враховувати для визначення необхідності проведення практики гігієни рук в амбулаторних умовах:
1) потенційний ризик передавання інфекційного агенту в залежності від процедури/маніпуляції;
2) потенційний ризик виникнення інфекційного захворювання для працівника і пацієнта;
3) відомий або підозрюваний статус колонізації мікроорганізмами;
4) можливість виконати практику гігієни рук в певній ситуації із врахуванням необхідної частоти її виконання.
2. Послідовність дій при проведенні щеплень:
1) пацієнт входить до кімнати і сідає на стілець, в той час як попередній пацієнт виходить;
2) працівник просить пацієнта назвати прізвище, власне ім'я та по батькові (за наявності) і адресу;
3) працівник вносить необхідні дані у відповідну документацію;
4) працівник просить пацієнта оголити передбачувану для проведення щеплення ділянку тіла;
5) працівник виконує гігієнічну обробку рук;
6) працівник готує все необхідне для щеплення - спиртові серветки, флакон з імунобіологічним лікарським засобом, шприц, голку та лейкопластир;
7) працівник протирає шкіру в місці ін'єкції спиртовою серветкою і викидає її в ємність для медичних відходів категорії А;
8) працівник бере попередньо підготований шприц із вакциною;
9) працівник проводить ін'єкцію, відповідно до рекомендацій виробника імунобіологічного лікарського засобу після висихання антисептика на шкірі пацієнта;
10) працівник викидає шприц з голкою або шприц-тюбик в контейнер для небезпечно гострих медичних відходів категорії В, який знаходиться на столі;
11) працівник накладає адгезивну пов'язку на місце ін'єкції (за необхідності);
12) працівник робить відмітку про виконану процедуру;
13) пацієнт встає і покидає кабінет (в той же час в кабінет входить наступний пацієнт);
14) працівник виконує гігієнічну обробку рук.
У випадках, коли процедура відбувається за вищенаведеним сценарієм, практика гігієнічної обробки рук, що має бути проведена після контакту із пацієнтом, проводиться одночасно із практикою гігієнічної обробки рук, яка має бути проведена перед контактом із пацієнтом.
В разі використання оглядових медичних рукавичок, після кожної ін'єкції їх необхідно зняти, викинути та провести гігієнічну обробку рук. Багаторазове використання медичних рукавичок (для проведення вакцинації двом і більше пацієнтам) заборонене. Обробка рук, одягнених в медичні рукавички, антисептиком для рук або іншим дезінфекційним засобом заборонена.
3. Послідовність дій під час здійснення забору крові в лабораторії:
1) пацієнт входить до кімнати і сідає на стілець (в той час як попередній пацієнт виходить);
2) працівник просить пацієнта назвати прізвище, власне ім'я та по батькові (за наявності), адресу і уточнює перелік необхідних аналізів згідно із направленням лікаря;
3) працівник вносить необхідні дані у відповідну документацію;
4) працівник вибирає та маркує пробірки для відбору зразків;
5) працівник просить пацієнта закатати рукав (за необхідності) аби звільнити передпліччя;
6) працівник готує все необхідне для проколу - одноразовий набір для забору крові, антисептик для рук, спиртові серветки, джгут, лейкопластир;
7) працівник накладає джгут;
8) працівник проводить гігієнічну обробку рук;
9) працівник надягає оглядові/нестерильні медичні рукавички;
10) працівник локалізує вену шляхом пальпації двома пальцями;
11) працівник обробляє місце майбутнього проколу спиртовою серветкою і викидає її у ємність для медичних відходів категорії А;
12) працівник проколює вену і забирає кров, після висихання антисептика на шкірі пацієнта;
13) працівник розпускає джгут;
14) працівник витягує голку та викидає її в контейнер для небезпечно гострих предметів медичних відходів категорії В і одночасно просить пацієнта натиснути на спиртову серветку в місці проколу;
15) працівник поміщає пробірки в стійку і викидає використаний матеріал, що залишився у ємності для медичних відходів відповідно до категорій;
16) працівник фіксує місце проколу лейкопластиром;
17) працівник знімає і викидає медичні рукавички;
18) працівник виконує гігієнічну обробку рук;
19) працівник оформлює необхідну документацію, в той час як виходить даний пацієнт і заходить наступний.
У випадках, коли процедура відбувається за вищенаведеним сценарієм, практика гігієнічної обробки рук, що має бути проведена перед контактом із пацієнтом, проводиться одночасно із практикою гігієнічної обробки рук, яка проводиться після контакту із пацієнтом.
4. Послідовність дій під час огляду лікарем загальної практики - сімейним лікарем:
1) пацієнт входить в кабінет і сідає на стілець чи кушетку;
2) пацієнт і лікар спілкуються один з одним, поки лікар переглядає записи щодо пацієнта;
3) лікар просить пацієнта лягти на кушетку;
4) лікар проводить гігієнічну обробку рук;
5) лікар виконує фізикальне обстеження;
6) після закінчення огляду лікар допомагає пацієнту встати;
7) лікар проводить гігієнічну обробку рук;
8) лікар сідає за стіл та проводить відповідні записи;
9) лікар пояснює пацієнту його стан та надає рекомендації;
10) даний пацієнт виходить, в той час до кімнати входить наступний.
В даній послідовності не враховані соціальні контакти, такі як рукостискання між пацієнтом і лікарем під час вітання та прощання. У випадку, якщо рукостискання відбуваються, після кожного з них необхідно додатково провести гігієнічну обробку рук.
Якщо під час огляду відбувається контакт із слизовими оболонками або шкірою, виникає необхідність асептичної або будь-якої іншої додаткової процедури, практику гігієни рук необхідно проводити за показаннями, які наведені у розділі I цього додатку.
5. Послідовність дій під час огляду новонародженого сестрою медичною (братом медичним) або лікарем:
1) мати / батько / законний представник дитини входять з нею до оглядової кімнати;
2) працівник запитує необхідну інформацію та записує її;
3) мати/батько/законний представник дитини роздягає її;
4) працівник виконує гігієнічну обробку рук;
5) працівник забирає дитину у матері / батька / законного представника та кладе її на стіл;
6) працівник оцінює фізичний розвиток дитини (здійснює вимірювання розмірів окружностей дитини та зважує її);
7) якщо у дитини під час зважування відбувся акт сечопускання, працівник одягає оглядові медичні рукавички, витирає випорожнення із використанням відповідних матеріалів і засобів, викидає рукавички у ємність для медичних відходів категорії В та проводить гігієнічну обробку рук;
8) працівник оглядає спину дитини, пальпує живіт, оглядає пупок і перевіряє неонатальні рефлекси;
9) працівник проводить аускультацію серця і легень;
10) працівник проводить гігієнічну обробку рук;
11) працівник оглядає очі дитини, злегка потягнувши повіки (дитина починає кричати);
12) працівник перевіряє зір шляхом водіння пальця перед очима (дитина продовжує кричати і плакати без сліз);
13) працівник оглядає ротову порожнину дитини під час плачу із використання медичного ліхтарика підтримуючи дитину за голову;
14) працівник перевіряє слух дитини, хлопаючи в долоні по бокам голови;
15) працівник перевіряє ніс та вуха дитини використовуючи отоскоп та викидає одноразову воронку у ємність для медичних відходів категорії В;
16) працівник пальпує шию дитини;
17) працівник проводить гігієнічну обробку рук;
18) мати / батько / законний представник дитини одягає її;
19) працівник записує дані і коротко спілкується із матір'ю/батьком/законним представником дитини;
20) мати / батько / законний представник із дитиною покидають оглядовий кабінет.
В даній послідовності не враховані соціальні контакти, такі як рукостискання між матір'ю / батьком / законним представником дитини і працівником під час вітання та прощання. У випадку, якщо рукостискання відбуваються, після кожного з них необхідно додатково провести гігієнічну обробку рук.
6. Послідовність дій при супроводі осіб, які потребують постійного догляду під час прийняття ванни:
1) працівник виконує гігієнічну обробку рук;
2) працівник готує рушник, одяг та інші необхідні предмети;
3) працівник одягає фартух захисний від інфекційних агентів (наприклад, целофановий) і допомагає пацієнту дійти або садить його в крісло колісне і супроводжує пацієнта до ванної кімнати;
4) в разі якщо крісло колісне індивідуальне (наприклад, допомога на дому), працівник не проводить практику гігієни рук; в інший випадках (наприклад, догляд в ЗСЗ) - перед повторним контактом із пацієнтом слід провести гігієнічну обробку рук;
5) працівник допомагає пацієнту роздягнутися, прийняти душ, витертися рушником, одягнутися, під час чищення зубів тощо;
6) поки пацієнт сидить на стільці або у кріслі колісному, працівник знімає фартух захисний від інфекційних агентів і змінює постільну білизну (в разі якщо крісло колісне не індивідуальне, після транспортування пацієнта до кімнати працівник проводить гігієнічну обробку рук);
7) працівник допомагає пацієнту лягти в ліжко;
8) працівник проводить гігієнічну обробку рук та прощається із пацієнтом.
7. Послідовність дій під час перев'язки хронічної трофічної виразки:
1) працівник виконує гігієнічну обробку рук;
2) працівник розкриває попередню пов'язку (знімає фіксувальний матеріал);
3) в разі проведення перев'язки на дому або в ЗСЗ, працівник проводить очищення і дезінфекцію приліжкового столика або тумби пацієнта і наступну практику гігієнічної обробки рук; працівник дістає стерильний запакований перев'язувальний матеріал та викладає його на приліжковий столик або тумбу;
4) працівник проводить гігієнічну обробку рук;
5) працівник готує стерильний перев'язочний набір і одягає оглядові медичні рукавички;
6) працівник знімає пов'язки і оглядає рану;
7) працівник викидає забруднені пов'язки у сміттєве відро (при догляді на дому або в ЗСЗ) або у ємність для медичних відходів категорії В (при догляді в амбулаторно-поліклінічному ЗОЗ);
8) працівник знімає та викидає оглядові медичні рукавички у сміттєве відро або у ємність для медичних відходів категорії В відповідно до підпункту 7 цього пункту;
9) працівник виконує гігієнічну обробку рук;
10) використовуючи відповідні інструменти, працівник декілька разів наносить антисептик, видаляє трохи фібрину ножицями (у разі необхідності) і знову наносить антисептик;
11) працівник викидає всі відходи у сміттєве відро або у ємність для медичних відходів категорії В відповідно до підпункту 7 пункту цього пункту, а інструменти складає;
12) використовуючи відповідні інструменти, працівник кладе мазь (у разі необхідності) на рану та накриває її марлевими серветками, фіксує клейкою пов'язкою;
13) після того як перев'язка завершена, працівник викидає всі відходи, які залишилися на столі у сміттєве відро або у ємність для медичних відходів категорії В відповідно до підпункту 7 цього пункту, інструментарій складає у пластиковий пакет і проводить дезінфекцію стола (якщо на поверхні стола наявні видимі залишки біологічних рідин, перед дезінфекцією слід провести очищення);
14) працівник проводить гігієнічну обробку рук;
15) працівник робить записи щодо стану рани та процедури;
16) працівник проводить гігієнічну обробку рук.
8. Послідовність дій під час проведення рентгенологічного обстеження:
1) пацієнт входить в кімнату, знімає та кладе свій одяг на стілець і підходить до рентген-лаборанта для отримання інструкцій;
2) рентген-лаборант проводить гігієнічну обробку рук;
3) рентген-лаборант допомагає пацієнту одягнути захисний свинцевий фартух і правильно розташуватися;
4) рентген-лаборант йде в апаратну кімнату і натискає кнопку з метою проведення знімку;
5) рентген-лаборант допомагає пацієнту зняти захисний свинцевий фартух та одягнутися (в разі необхідності);
6) рентген-лаборант виконує гігієнічну обробку рук;
7) рентген-лаборант записує необхідні дані.
9. Послідовність дій під час надання стоматологічної допомоги:
1) пацієнт входить в кімнату і сідає в стоматологічне крісло;
2) лікар-стоматолог одягає медичну (хірургічну) маску і захисні окуляри/щиток, налагоджує своє крісло та вмикає лампу;
3) лікар-стоматолог виконує гігієнічну обробку рук;
4) лікар-стоматолог одягає оглядові/нестерильні медичні рукавички;
5) лікар-стоматолог оглядає зуби пацієнта дзеркалом із лотка, що був підготований помічником (лоток, окрім дзеркала, містить всі матеріали і вироби, що необхідні для надання стоматологічної допомоги);
6) лікар-стоматолог проводить місцеву анестезію, знімає та викидає медичні рукавички в ємність для медичних відходів категорії В;
7) лікар-стоматолог виконує гігієнічну обробку рук;
8) лікар-стоматолог одягає оглядові медичні рукавички та виконує процедури;
9) по закінченню втручання, лікар-стоматолог знімає медичні рукавички, викидає їх у ємність для медичних відходів категорії В та виконує гігієнічну обробку рук;
10) помічник лікаря-стоматолога проводить гігієнічну обробку рук, одягає оглядові медичні рукавички, проводить очищення і дезінфекційну обробку стоматологічного крісла (включно із оточуючим середовищем, що потенційно було забруднене під час стоматологічної процедури);
11) помічник лікаря-стоматолога знімає і викидає медичні рукавички у ємність для медичних відходів категорії В та виконує гігієнічну обробку рук, готує лоток для проведення наступної процедури.
10. Вимірювання тиску та рівня глюкози крові у прикутого до ліжка пацієнта на дому або в будинку для людей похилого віку:
1) працівник виконує гігієнічну обробку рук та пояснює пацієнту ціль свого візиту;
2) працівник допомагає пацієнту зручно сісти, звільняє руку від одягу та вимірює артеріальний тиск;
3) працівник протирає палець пацієнта спиртовою серветкою та викидає її;
4) працівник одягає оглядові медичні рукавички;
5) працівник робить прокол пальця скарифікатором, після висихання антисептика на шкірі пацієнта;
6) працівник поміщає скарифікатор в ємність для небезпечно гострих предметів медичних відходів категорії В;
7) працівник вставляє тест-смужку в глюкометр та набирає необхідну кількість крові;
8) працівник прикладає спиртову серветку на місце проколу (до зупинки виділення крові в разі необхідності);
9) працівник знімає і викидає медичні рукавички в ємність для медичних відходів категорії В;
10) працівник виконує гігієнічну обробку рук;
11) працівник записує отримані результати.
11. Послідовність дій під час зміни підгузка у прикутого до ліжка пацієнта:
1) працівник виконує гігієнічну обробку рук та пояснює пацієнту свою ціль;
2) працівник одягає оглядові медичні рукавички;
3) працівник підкладає під пацієнта пелюшку;
4) працівник розкриває пацієнта, знімає і складує використаний підгузок і кладе його у пакет для підгузків або ємність для медичних відходів категорії В;
5) працівник очищає пацієнта, за допомогою мильної піни та паперових рушників, перед одяганням чистого підгузка;
6) працівник викидає використані паперові рушники у пакет для підгузків або ємність для відходів категорії В;
7) працівник знімає медичні рукавички, викидає їх у пакет для підгузків або ємність для медичних відходів категорії В та виконує гігієнічну обробку рук;
8) працівник укладає пацієнта у зручну позу, накриває його та проводить гігієнічну обробку рук.
IV. Використання медичних рукавичок
1. Використання медичних рукавичок не дає абсолютної гарантії захисту пацієнтів та працівників від збудників інфекції.
2. У медичній практиці використовуються три типи медичних рукавичок:
1) стерильні — використовуються при проведенні інвазивних втручань, що вимагають підтримки асептичних умов;
2) нестерильні/оглядові — забезпечують захист працівників при виконанні багатьох медичних маніпуляцій;
3) рукавички для проведення хіміотерапії.
3. Побутові (багаторазові, обмеженого використання) рукавички використовувати в ЗОЗ/ЗСЗ заборонено. Рукавички захисні від інфекційних агентів та хімічних речовин обмеженого використання дозволено використовувати при проведенні догляду за пацієнтами в надзвичайних ситуаціях/станах (наприклад, надання медичної допомоги в польових умовах).
4. Використання покритих тальком (талькованих) медичних рукавичок в ЗОЗ/ЗСЗ заборонено.
5. Показання до використання стерильних і оглядових медичних рукавичок наведено у Таблиці 1 нижче.
Таблиця 1. Показання до використання стерильних і оглядових медичних рукавичок*
Показано використання стерильних медичних рукавичок |
Використання нестерильних (оглядових) медичних рукавичок показано в наступних клінічних ситуаціях — ризик контакту з кров’ю та іншими біологічними рідинами, секретами, екскретами і предметами, що видимо ними забруднені |
Використання медичних рукавичок не показано (за виключенням контактних заходів захисту) — відсутність контакту з кров’ю або іншими біологічними рідинами, а також із об’єктами зовнішнього середовища, які контаміновані ними |
||
Прямий контакт з пацієнтом |
Непрямий контакт з пацієнтом |
Прямий контакт з пацієнтом |
Непрямий контакт з пацієнтом |
|
1 |
2 |
3 |
4 |
5 |
Будь-які хірургічні процедури |
Контакт з кров’ю чи іншими біологічними рідинами |
Спорожнення ємностей із блювотними масами |
Вимірювання артеріального тиску, температури і пульсу |
Використання телефону |
____________
* Медичні рукавички слід носити відповідно до стандартних і контактних заходів захисту. У Таблиці описано деякі клінічні ситуації, при яких необхідно використовувати рукавички, а також приклади, в яких наявні покази до використання стерильних і нестерильних (оглядових) медичних рукавичок. Гігієнічна обробка рук повинна бути виконана в тих випадках, коли це необхідно, в незалежності від наявності показів до використання рукавичок.
6. Правила одягання та знімання медичних рукавичок наведено на Схемах 5, 6, 7 нижче.
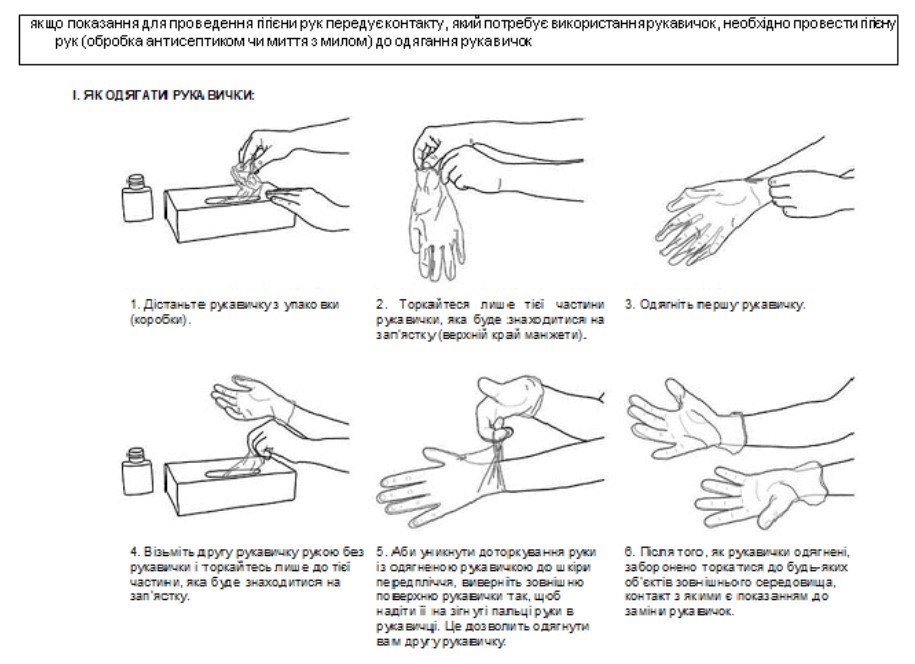
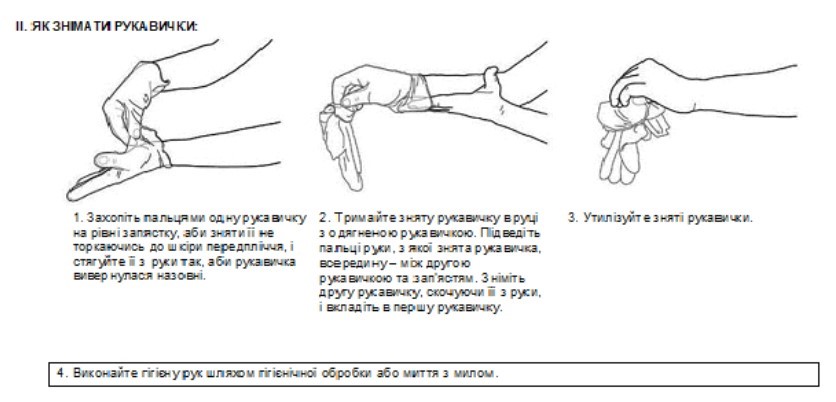
Схема 5. Одягання та знімання нестерильних (оглядових) медичних рукавичок
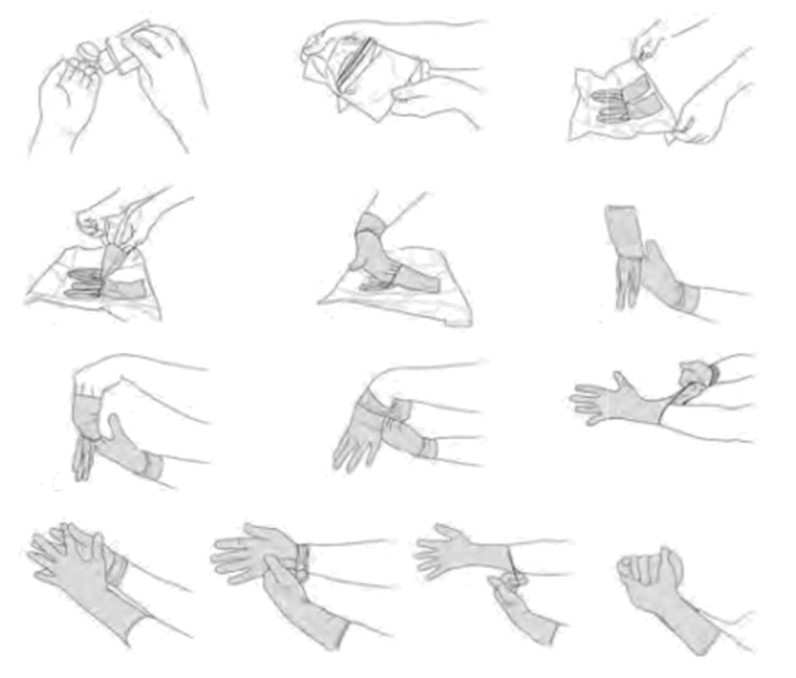
Схема 6. Одягання стерильних медичних рукавичок
Покрокова інструкція:
1) перед тим як перейти до одягання медичних рукавичок, слід обрати правильний їх розмір, в яких Вам буде зручно працювати. Необхідно зняти всі прикраси, годинники, якщо вони одягнені;
2) слід підготувати чисту робочу зону, шляхом очищення (за необхідності) і дезінфекції поверхні;
3) проведіть гігієнічну обробку рук;
4) перевірте упаковку на цілісність. Відкрийте першу (нестерильну) упаковку, зніміть її не торкаючись другої (стерильної);
5) покладіть медичні рукавички, запаковані в другу (стерильну) упаковку, на підготовану поверхню, не доторкуючись до неї. Відкрийте упаковку, тримаючи її з нижньої сторони;
6) використовуючи великий і вказівний пальці однієї руки, підніміть складений кінець манжети медичної рукавички;
7) надягніть медичну рукавичку на другу руку одним рухом, тримаючи складену манжету на рівні зап’ястя;
8) візьміть другу медичну рукавичку, просунувши пальці руки в медичній рукавичці під манжету;
9) одним рухом надіньте медичну рукавичку на другу руку, уникаючи контакту до будь-яких поверхонь, крім тих для роботи з якими одягаються медичні рукавички. В разі будь-якого контакту, внаслідок якого було порушено асептику, медичні рукавички слід замінити;
10) за необхідності, після одягання слід поправити медичні рукавички на пальцях та між пальцями, щоб медичні рукавички сиділи зручно;
11) розправити манжету першої одягненої медичної рукавички пальцями другої руки таким чином, аби уникнути контакту з будь-якими поверхнями окрім зовнішньої поверхні медичної рукавички. В разі будь-якого контакту, внаслідок якого було порушено асептику, медичні рукавички слід замінити;
12) руки в медичних рукавичках мають торкатися виключно стерильних об’єктів або ділянок тіла пацієнта, які попередньо продезінфіковані.
Одягання стерильних рукавичок для проведення хірургічних утручань проводиться в такій же послідовності, за виключенням:
1) перед одяганням медичних рукавичок проводиться хірургічна обробка рук;
2) одягання медичних рукавичок слідує після одягання стерильного хірургічного халату;
3) відкриття першої (нестерильної) упаковки проводиться помічником;
4) друга (стерильна) упаковка разом із медичними рукавичками перед одяганням має бути розміщена на стерильній поверхні, але не на тій на якій буде безпосередньо проводитися хірургічне втручання;
5) медичні рукавички повинні мати довгі манжети, аби повністю покривати манжети халату.
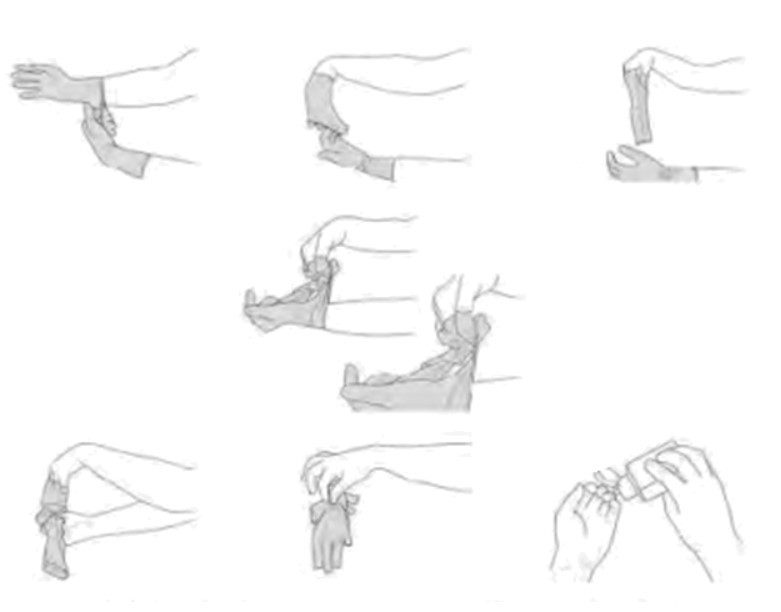
Схема 7. Знімання стерильних рукавичок
Покрокова інструкція:
1) знімати першу медичну рукавичку слід пальцями другої руки. Знімайте першу медичну рукавичку, вивертаючи її навиворіт, до другого суглобу пальців (не знімайте медичну рукавичку повністю);
2) зніміть повністю другу медичну рукавичку пальцями першої руки, вивертаючи її зовнішній край. Медичні рукавички слід знімати так, аби шкіра рук контактувала виключно з внутрішньою поверхнею медичної рукавички;
3) викиньте медичні рукавички;
4) проведіть гігієнічну обробку рук.
7. Одразу після використання медичні рукавички знімаються. Після використання медичні рукавички відносять до медичних відходів категорії В.
8. Правила використання медичних рукавичок:
1) використання медичних рукавичок не створює абсолютного захисту і вимагає виконання практики гігієнічної обробки рук, яка застосовується одразу після зняття медичних рукавичок;
2) медичні рукавички не припустимо використовувати повторно;
3) нестерильні медичні рукавички стерилізації не підлягають;
4) медичні рукавички необхідно змінювати одразу, у випадку пошкодження;
5) не допускається миття або обробка рук в медичних рукавичках;
6) не допускається пересування в медичних рукавичках поза точкою догляду;
7) перед надяганням медичних рукавичок не можна використовувати будь-які засоби, окрім антисептику для рук.
9. Помилки, які часто виникають при використанні медичних рукавичок:
1) неправильне зберігання медичних рукавичок (на сонці, при низьких температурах, потрапляння на рукавички хімічних речовин тощо);
2) натягування медичних рукавичок на руки, які зволожені антисептиком;
3) ігнорування необхідності проведення антисептичної обробки рук після зняття медичних рукавичок;
4) використання звичайних медичних рукавичок при роботі з цитостатиками (недостатній захист працівників);
5) недостатній догляд за шкірою рук;
6) відмова від медичних рукавичок.
10. Дезінфікувати медичні рукавички з метою їх повторного використання заборонено.
Додаток 2
до Інструкції з впровадження покращення гігієни рук
в закладах охорони здоров’я та установах / закладах надання
соціальних послуг / соціального захисту населення
(підпункт 2 пункту 6 розділу I)
Примірна стандартна операційна процедура : «Гігієна рук»*
«___» ____________ ____ р.
Посада |
Прізвище, ім’я та по батькові (за наявності) |
Підпис |
|
Розроблено |
|||
Підписано |
Керівник ВІК |
||
Затверджено |
Керівник ЗОЗ/ЗСЗ |
Алгоритм проведення гігієни рук медичного персоналу
№ п/п |
Умови і способи обробки рук |
Алгоритм |
Нормативний документ** |
1 |
2 |
3 |
4 |
1. |
Умови, при яких проводиться миття рук з милом і водою та гігієнічна обробка рук |
1. коротко підстрижені нігті; |
|
2. |
Способи гігієни рук |
1. миття рук з милом і водою для видалення бруду і транзиторної флори; |
|
3. |
Випадки в яких слід проводити гігієнічну обробку рук |
1. перед безпосереднім контактом із пацієнтом; |
|
4. |
Етапи гігієни рук |
1. етапи миття рук з милом і водою та гігієнічної обробки рук додаються***; |
|
6. |
Етапи хірургічної обробки рук |
1. етапи хірургічної обробки рук додаються***; |
Рекомендації ВООЗ |
____________
* шаблон, який використовується для розробки СОП в ЗОЗ/ЗСЗ.
** у колонці нормативний документ зазначаються нормативно-правові акти, рекомендації ВООЗ з питань гігієни рук, інші галузеві стандарти, які застосовує ЗОЗ/ЗСЗ. Нормативні документи додаються до СОП або визначається місце у ЗОЗ/ЗСЗ, де можна ознайомитись із такими документами;
*** слід додати візуальні схеми проведення практик гігієни рук.
Додаток 3
до Інструкції з впровадження покращення гігієни рук
в закладах охорони здоров’я та установах / закладах надання
соціальних послуг / соціального захисту населення
(пункт 8 розділу I, пункт 6 розділу V)
Профіль та основні завдання працівників для виконання ними функцій з впровадження покращення гігієни рук в ЗОЗ/ЗСЗ
Функція |
Профіль та професійні вимоги |
Основні завдання |
1 |
2 |
3 |
Координатор з гігієни рук та його заступник |
1. Має знання з профілактики інфекцій, інфекційного контролю та гігієни рук, що підтверджується відповідним документом (сертифікат або еквівалент). |
1. Відкрито і відповідно до правил дотримуватися гігієни рук. |
Інструктор/тренер |
1. Сестра медична або лікар із досвідом практичної медичної діяльності. |
1. Відкрито і відповідно до правил дотримуватися гігієни рук. |
Спостерігач/дослідник |
1. Сестра медична або лікар із досвідом практичної медичної діяльності. |
1. Відкрито і відповідно до правил дотримуватися гігієни рук. |
Спеціаліст зі збору та аналізу даних/статистик |
Знання в області епідеміології і статистичного аналізу. |
Збір, введення та аналіз даних оцінок з гігієни рук. |
Додаток 4
до Інструкції з впровадження покращення гігієни рук
в закладах охорони здоров’я та установах / закладах надання
соціальних послуг / соціального захисту населення
(підпункт 1 пункту 5 розділу II, пункт 6 розділу II,
підпункт 3 пункту 7 розділу II, підпункт 2 пункту 8 розділу II,
пункт 6 розділу III, пункт 11 розділу V, підпункт 1 пункту 6
розділу VII, підпункт 7 пункту 10 розділу VII, підпункт 1
пункту 14 розділу VII, підпункт 1 пункту 17 розділу VII)
Протокол оцінки інфраструктури і ресурсів для гігієни рук у ЗОЗ/ЗСЗ
I. Вступна частина
1. Виконання оцінки відповідно до цього Протоколу здійснюється для отримання даних про наявну інфраструктуру і ресурси для гігієни рук у ЗОЗ/ЗСЗ. 2. Збір інформації щодо інфраструктури і ресурсів для гігієни рук здійснюється для базової (початкової) оцінки та подальшого оцінювання в кожному з підрозділів ЗОЗ/ЗСЗ, де така оцінка має проводитися в контексті впровадження покращення з гігієни рук (кроки впровадження гігієни рук 1, 2 та 4, визначені у розділі VII Інструкції). 3. У разі відсутності доступу до раковин, проточної води, рідкого мила та антисептиків для рук проведення інших заходів з впровадження гігієни рук є неможливим. 4. Цей Протокол виконується відповідно до графіку, затвердженого керівництвом ЗОЗ/ЗСЗ, але не рідше ніж один раз на рік. 5. Цей Протокол виконується працівником, посада або функції якого входять до переліку, зазначеному у пункті 8 Опитувальника наведеного нижче, та пройшов інструктаж або відповідне навчання, яке проводиться ВІК. 6. Опитувальник та Таблиця для оцінки необхідної кількості обладнання і засобів для гігієни рук, які є частиною цього Протоколу, заповнюються під час перебування в підрозділі (в безпосередній близькості до точок догляду). 7. Дані, заповнені по кожному із підрозділів, сумуються для ЗОЗ/ЗСЗ в цілому згідно із Таблицею (пункт 3 цього Протоколу). 8. Результати оцінки, проведеної відповідно до цього Протоколу, використовуються для визначення пріоритетів для змін в системі і подальшого впровадження покращення з гігієни рук. 9. Короткий словник: антисептик для рук — спиртовмісний дезінфекційний засіб (рідина, гель або піна), що застосовується для нанесення на шкіру рук з метою знищення мікроорганізмів; гігієнічна обробка рук — обробка рук шляхом втирання антисептика для рук в шкіру рук; миття рук — миття рук з милом та водою; палата/бокс/кімната — найменша частина ЗОЗ/ЗСЗ, що використовується для надання допомоги окремому пацієнту, групі або категорії пацієнтів. |
II. Опитувальник
1. Дата: |
2. Назва ЗОЗ/ЗСЗ: |
||
3. Місто |
4. Регіон/Область: |
||
5. Підрозділ: |
6. Інше: |
Наявні обладнання та засоби для гігієни рук
7. Напрям діяльності: |__| терапевтичний/внутрішні хвороби |__| хірургічний |__| інтенсивна терапія |__| змішаний (надається різнопрофільна допомога в залежності від потреби) |__| невідкладна допомога/приймальне відділення |__| акушерство |__| педіатрія |__| реабілітація |__| хоспісна допомога |__| денний стаціонар |__| довготривалого перебування |__| інше (вписати): _____________________________________________________________________ 8. Посада/функція працівника, який заповнює Опитувальник та Таблицю: |__| координатор з гігієни рук |__| заступник координатора з гігієни рук |__| інший представник ВІК (зазначити посаду): ______________________ |__| старша сестра медична |__| ординатор |__| інші (зазначити): ____________________________________________________________________ 9. Кількість працівників в підрозділі (зазначити): |__| лікарі: _____ |__| сестри медичні/середні медичні працівники: _____ |__| молодші медичні працівники: _____ |__| інші працівники (зазначити посаду): 1) _____________: _____ 2) _____________: _____ 3) _____________: _____ 4) _____________: _____ 5) _____________: _____ 10. Проточна вода доступна: |__| завжди |__| часто |__| періодично |__| ніколи 11. Вода візуально є чистою: |__| так |__| ні |__| на момент проведення оцінювання проточна вода відсутня 12. Які види кранів доступні: |__| з ручним регулюванням |__| з ліктьовим регулюванням |__| з регулюванням ногами |__| автоматичні 13. Чи наявні одноразові паперові рушники біля кожної раковини? |__| так і існує доступний їх запас |__| так, але запас відсутній або знаходиться поза зоною доступності |__| ні, але наявний тримач |__| ні 14. Чи наявне мило біля кожної раковини? |__| так і існує доступний його запас |__| так, але запас відсутній або знаходиться поза зоною доступності |__| ні, але наявний диспенсер |__| ні 15. Чи доступний антисептик для рук? |__| так і існує доступний його запас |__| так, але запас відсутній або знаходиться поза зоною доступності |__| ні, але наявний диспенсер |__| ні 16. Якщо так, то які типи диспенсерів наявні (позначте всі типи, що наявні)? |__| кишеньковий |__| диспенсер, що прикріплений до процедурного/маніпуляційного столика/таці |__| диспенсер, що прикріплений до ліжка |__| настінний диспенсер |__| переносний диспенсер 17. Якщо наявні настінні диспенсери, чи розміщені вони в безпосередній доступності біля точок догляду? |__| так |__| так, але не поблизу всіх точок догляду |__| ні 18. Кожен працівник має доступ до кишенькових диспенсерів із антисептиком для рук? |__| так, завжди |__| так, часто |__| так, періодично |__| ні |__| на момент проведення оцінювання працівники відсутні 19. У підрозділі призначено відповідальну особу за наповнення/заміну диспенсерів? |__| так |__| ні 20. Чи замінюються одноразові кишенькові диспенсери після закінчення в них антисептиків для рук (оцінюється шляхом перевірки документації видачі/заміни)? |__| так |__| так, однак тривалість використання диспенсерів викликає сумніви (занадто довго використовуються) |__| так, однак інформація, що зазначена в документації сумнівна |__| документація не надана або відсутня 21. Інформаційні матеріали (наприклад, плакати), що ілюструють правила миття рук, наявні біля всіх раковин? |__| так |__| ні 22. Інформаційні матеріали (наприклад, плакати), що ілюструють правила гігієнічної обробки рук антисептиком, розміщені біля кожного диспенсеру та додатково в декількох інших місцях підрозділу? |__| так |__| так, але не біля кожного диспенсеру |__| так, але відсутні додаткові інформаційні матеріали |__| ні 23. Чи розміщені інформаційні матеріали (наприклад, плакати) в зоні відпочинку працівників? |__| Так |__| Ні 24. Чи наявні в підрозділі будь-які інші інформаційні матеріали щодо гігієни рук? |__| так |__| ні 25. Чи наявні нестерильні/оглядові медичні рукавички? |__| так |__| так, але в недостатній кількості |__| так, але відсутній доступний запас |__| ні 26. В підрозділі проводиться оцінка дотримання правил гігієни рук згідно із затвердженим графіком? |__| так |__| ні 27. Якщо так, то як часто? |__| не рідше одного разу на рік |__| не рідше одного разу на два роки |__| рідше одного разу на два роки |
III. Таблиця оцінки необхідних обладнання та засобів для гігієни рук
№ палати/ кімнати/ боксу |
Загальна кількість ліжок в палаті/ кімнаті/ боксі |
Кількість ліжок з диспенсером |
Кількість раковин в цій палаті/ кімнаті/ боксі |
Кількість раковин із доступом до проточної води |
Кількість раковин із доступом до мила |
Кількість раковин із доступом до одноразових паперових рушників |
Кількість раковин із доступом до проточної води, мила та одноразових паперових рушників |
Загальна кількість диспенсерів (стаціонарних) в цій палаті/ кімнаті/ боксі |
Кількість справних та наповнених диспенсерів |
Число працівників із якими зустрілися під час проведення оцінювання |
Число працівників у яких на час проведення оцінювання був наявний кишеньковий диспенсер |
|
Палати/кімнати/бокси для пацієнтів в цьому підрозділі |
||||||||||||
1 |
||||||||||||
2 |
||||||||||||
3 |
||||||||||||
4 |
||||||||||||
5 |
||||||||||||
6 |
||||||||||||
7 |
||||||||||||
8 |
||||||||||||
9 |
||||||||||||
10 |
||||||||||||
Всього |
||||||||||||
Процедурні кабінети |
||||||||||||
1 |
||||||||||||
2 |
||||||||||||
3 |
||||||||||||
4 |
||||||||||||
5 |
||||||||||||
Всього |
||||||||||||
Інші зони із точками догляду |
||||||||||||
1 |
||||||||||||
2 |
||||||||||||
3 |
||||||||||||
4 |
||||||||||||
5 |
||||||||||||
Всього |
||||||||||||
Загальна кількість |
||||||||||||
Додаток 5
до Інструкції з впровадження покращення гігієни рук
в закладах охорони здоров’я та установах / закладах надання
соціальних послуг / соціального захисту населення
(підпункт 2 пункту 5 розділу II, пункт 6
розділу II, пункт 6 розділу III)
Протокол оцінки потреби у антисептику для рук та витрат на нього
1. Відповідно до цього Протоколу здійснюється оцінка потреби ЗОЗ/ЗСЗ у антисептику для рук, витрат на нього.
2. Для проведення оцінки відповідно до цього Протоколу попередньо необхідно визначити:
1) місця у точках догляду, де повинні розташовуватися стаціонарні диспенсери (настінні, прикріплені до ліжок, приліжкових тумб або процедурних столиків (стаціонарних чи пересувних);
2) в яких підрозділах раціонально використовувати кишенькові антисептики для рук;
3) який антисептик для рук фінансово доступний для ЗОЗ/ЗСЗ, відповідає державним стандартам України, що затверджуються національним органом стандартизації, добре переноситься та сприймається працівниками.
3. Оцінка відповідно до цього Протоколу проводиться під час розробки плану дій з покращення гігієни рук, зміни виробника чи постачальника антисептику для рук, при проведенні системної самооцінки гігієни рук (додаток 12 до цієї Інструкції) або на етапі кроку 1 впровадження гігієни рук, визначеному у розділі VII цієї Інструкції.
4. Цей Протокол виконується координатором з гігієни рук або уповноваженим працівником, що працює у підрозділі (ординатор або старша сестра медична), після проходження інструктажу.
5. Цей Протокол включає Таблицю 1 та Таблицю 2, заповнення яких надає можливість оцінити ситуацію у ЗОЗ/ЗСЗ із антисептиками для рук та визначити першочергові і наступні затрати на антисептик для рук, його об’єми (наприклад, впровадження на рівні всього ЗОЗ/ЗСЗ або окремого підрозділу).
6. Результати оцінки відповідно до цього Протоколу використовуються керівництвом ЗОЗ/ЗСЗ, керівником ВІК, провізором або фармацевтом лікарняної аптеки, головною сестрою медичною.
Таблиця 1. Оцінка ресурсів для використання антисептиків для рук і першочергових витрат
Предмет оцінки |
Пояснення/приклади |
Результат/відповідь |
Кількість точок догляду, наявних в ЗОЗ/ЗСЗ/підрозділі/палаті |
Кількість ліжок та/або кількість процедурних столиків |
|
Кількість необхідних диспенсерів |
||
Кількість працівників, які мають бути забезпечені індивідуальними кишеньковими диспенсерами ємністю 100 мл для охоплення всіх можливих потреб в гігієнічній обробці рук |
Кількість працівників, які проводять догляд |
|
Сумарна вартість настінного диспенсеру та 500–1000 мл антисептику для рук.(грн. за одиницю) |
Обрати фінансово доступні для ЗОЗ/ЗСЗ |
|
Вартість кишенькового диспенсеру ємністю 100 мл (грн. за одиницю) |
Обрати фінансово доступні для ЗОЗ/ЗСЗ |
Примітка:
1. ця таблиця містить мінімальний примірний перелік предметів оцінки та може бути доповнена відповідно до потреб ЗОЗ/ЗСЗ;
2. у колонці «Пояснення/приклади» наведено примірні категорії та пояснення, які мають враховуватись для розрахунків;
3. у колонці «Результат/відповідь» наводяться результати розрахунків та пояснення для них.
Таблиця 2. Розрахунок місячної потреби антисептику для рук
Показник для розрахунку |
Пояснення/приклади |
Результат/відповідь |
Кількість працівників, які безпосередньо проводять догляд |
Не всі працівники (включно із лікарями і сестрами медичними) безпосередньо контактують із пацієнтами (наприклад, адміністрація ЗОЗ/ЗСЗ). Для визначення реального числа, прослідковується кількість працівників, які знаходяться в прямому контакті із пацієнтами в репрезентативній вибірці за певний період часу. Число таких працівників зазвичай складає 40–60% від загальної кількості працівників ЗОЗ/ЗСЗ. |
|
Кількість можливих процедур з гігієни рук за одну годину |
Слід зазначити максимально можливу кількість, яка може варіювати від 8 на годину для підрозділів ЗОЗ/ЗСЗ до 22 і більше для підрозділів інтенсивної терапії. |
|
Кількість годин в день, коли можливий контакт із пацієнтом |
Наприклад, 4–6 годин за 8-годинну зміну. |
|
Кількість робочих днів в місяць |
Приблизно 22–25 (в середньому 22). |
|
Кількість антисептику для рук, що необхідна для проведення однієї процедури гігієни рук |
3 мл |
|
Можливі втрати антисептику для рук. |
10% |
Примітка:1. у колонці «Пояснення/приклади» наводяться пояснення ЗОЗ/ЗСЗ для визначення значення показника для розрахунку;
2. у колонці «Результат/відповідь» наводяться результати розрахунків показників;
3. Розрахунок місячної потреби антисептику для рук здійснюється із використанням значень колонки «Результат/відповідь» за такою формулою:МП = КМП × ПР × Ч × РД × 0,003 + 10% МВ, деМП — місячна потреба антисептику для рук, в літрах;
КМП — кількість працівників;
ПР — кількість можливих процедур з гігієни рук за одну годину;
Ч — кількість годин в день, коли можливий контакт із пацієнтом;
РД — кількість робочих днів в місяць;
0,03 — кількість антисептику для рук, що необхідна для проведення однієї процедури, літри;
10% МВ — 10%, що закладаються на можливі втрати;4. отриманий результат розрахунків за формулою, наведеною у пункті 3 цієї Примітки, може не співпадати з реальними витратами антисептику для рук, особливо на початку реалізації заходів з покращення гігієни рук, оскільки не всі працівники дотримуються правильної практики гігієни рук;
5. на першому році впровадження покращення гігієни рук оцінювання витрат антисептику необхідно проводити щомісяця, а в подальшому — щоквартально. Такий підхід дозволяє не тільки коригувати витрати, а й, опосередковано, дає можливість отримати інформацію щодо реального дотримання практик гігієни рук.
Додаток 6
до Інструкції з впровадження покращення гігієни рук
в закладах охорони здоров’я та установах / закладах надання
соціальних послуг / соціального захисту населення
(підпункт 3 пункту 5 розділу II, пункт 6 розділу III, пункт 11
розділу V, підпункт 1 пункту 6 розділу VII, підпункт 7 пункту 10
розділу VII, підпункт 6 пункту 13 розділу VII, підпункт 1
пункту 14 розділу VII, підпункт 3 пункту 17 розділу VII)
Протокол оцінки використання засобів для гігієни рук у ЗОЗ/ЗСЗ
I. Вступна частина
1. Відповідно до цього Протоколу здійснюється оцінка використання засобів для гігієни рук (рідкого мила і антисептику для рук) у ЗОЗ/ЗСЗ з метою: 1) визначення використання засобів для гігієни рук на етапі базової оцінки (крок 2) відповідно до плану дій на перший рік впровадження покращення гігієни рук; 2) опосередкованого методу контролю гігієни рук; 3) моніторингу використання засобів для гігієни рук; 4) визначення потреби для планування та закупівлі засобів для гігієни рук, контролю рівня їх запасів в короткостроковій і в довгостроковій перспективах. 2. Оцінка відповідно до цього Протоколу проводиться у ЗОЗ/ЗСЗ вперше для базової оцінки та в подальшому один раз на місяць протягом першого року впровадження заходів з гігієни рук, починаючи з другого року впровадження — кожні 3— 4 місяці або в разі необхідності. Графік проведення оцінок може коригуватися у відповідності до графіку проведення закупок або поставок. 3. Оцінку відповідно до цього Протоколу проводить координатор з гігієни рук або уповноважений працівник, який працює у підрозділі (ординатор або старша сестра медична) після проходження інструктажу. 4. Виконання цього Протоколу передбачає заповнення форми для проведення оцінки, яка містить чотири пункти. Для збору даних можуть використовуватись форми замовлення або поставки відповідного засобу для гігієни рук згідно із практикою ЗОЗ/ЗСЗ, які отримані у тендерному комітеті (підрозділі закупівель) або в уповноваженої особи. Альтернативно дані можуть бути отримані у працівника ЗОЗ/ЗСЗ/підрозділу, який відповідальний за розподіл засобів для гігієни рук. 5. Заповнення Таблиць у пунктах 3 та 4 Форми для проведення оцінки використання засобів для гігієни рук у ЗОЗ/ЗСЗ здійснюється із врахуванням наступного: 1) таблиці використовуються для заповнення даних щомісячно протягом шести місяців. Якщо дані за один із місяців недоступні, вводяться сумарні дані, що відповідають більш тривалим періодам (наприклад, два або три місяці); 2) на кожні шість місяців заповнюється нова таблиця; 3) у розрахунку використання засобів для гігієни рук, проведеному відповідно до даних закупівельних або видаткових форм, враховується кількість засобів, які залишаються на складі. Для правильного визначення використаних засобів, від отриманої при підрахунках суми віднімаються залишки та перевіряється відповідність суми використаних засобів і їх залишків сумі, яка вказана в закупівельних або видаткових формах; 4) при використанні різних засобів для гігієни рук (наприклад, антисептики для рук із різним складом) необхідно заповнювати пункт 3 окремо для кожного з них. У випадках, коли один і той же засіб постачався в різних об’ємах (наприклад, на початку року фасувався по 100 мл в кишеньковій пляшечці, а потім — по 125 мл), Протокол заповнюється із вказанням кількості засобу в літрах та не враховується тара, в якій він постачався; 5) у таблицях враховуються будь-які зміни в кількості ліжок, працівників, пацієнтів або ліжкоднів. В разі залучення до використання засобів для гігієни рук нової палати, проведення капітального ремонту із перепрофілюванням або відкриття відділення — проводиться базова оцінка та подальший моніторинг. 6. В кінці шестимісячного періоду використання засобу необхідно сформувати звіти по кожному підрозділу і по ЗОЗ/ЗСЗ в цілому та направити всім зацікавленим сторонам. Результати оцінки, проведеної відповідно до цього Протоколу, використовуються ВІК/координатором з гігієни рук для оцінки впливу плану дій з покращення гігієни рук в цілому та направляються у структурний підрозділ, який проводить закупівлі, іншим зацікавленим сторонам. Тенденція до підвищення використання засобів для гігієни рук може свідчити про успіх програми з покращення гігієни рук. Статистично сталі результати або тенденції до зниження використання засобів для гігієни рук підлягають аналізу для коригування плану дій з метою покращення результатів. 7. Результати оцінки використовуються також для оцінки ефективності роботи ВІК/координатора з гігієни рук. 8. Короткий словник: відділ централізованих закупок — структурний підрозділ ЗОЗ/ЗСЗ або окрема структурна одиниця, що збирає потребу та здійснює закупки для ЗОЗ/ЗСЗ; антисептик для рук — спиртовмісний дезінфекційний засіб (рідина, гель або піна), що застосовується для нанесення на шкіру рук з метою знищення мікроорганізмів; палата/бокс/кімната — найменша частина ЗОЗ/ЗСЗ, що використовується для надання допомоги окремому пацієнту, групі або категорії пацієнтів. |
II. Форма для проведення оцінки використання засобів для гігієни рук у ЗОЗ/ЗСЗ
1. Загальна інформація щодо організації процесу закупівлі засобів для гігієни рук у ЗОЗ/ЗСЗ: 1) чи наявний відділ централізованих закупок? |__| так |__| ні 2) як часто збирається потреба в засобах для гігієни рук? |__| щомісяця |__| щоквартально |__| кожні півроку |__| нерегулярно |__| інше (вписати): ______________________ 3) опис процесу замовлення, закупки та розподілу засобу для гігієни рук в ЗОЗ/ЗСЗ/підрозділі із обов’язковим зазначенням часового інтервалу між замовленням, поставкою і початком розподілу та працівниками, які відповідальні за кожну задачу в процесі: __________________________________________________________________________________________ __________________________________________________________________________________________ __________________________________________________________________________________________ __________________________________________________________________________________________ __________________________________________________________________________________________ __________________________________________________________________________________________ __________________________________________________________________________________________ __________________________________________________________________________________________ __________________________________________________________________________________________ __________________________________________________________________________________________ 2. Інформація щодо місця проведення оцінки використання засобів для гігієни рук: 1) назва структурного підрозділу ЗОЗ/ЗСЗ: _______________________________________ 2) П. І. Б. координатора з гігієни рук: _______________________________________________ 3) період проведення (вказати чіткий шестимісячний інтервал): __________________ 4) вкажіть які та в якій кількості палати в ньому/ній наявні із зазначенням короткого опису (наприклад, розташування раковин і дозаторів, їхню кількість тощо): __________________________________________________________________________________________ __________________________________________________________________________________________ __________________________________________________________________________________________ __________________________________________________________________________________________ __________________________________________________________________________________________ __________________________________________________________________________________________ __________________________________________________________________________________________ __________________________________________________________________________________________ __________________________________________________________________________________________ __________________________________________________________________________________________ 3. Антисептик для рук: 1) тип продукту: |__| гель |__| рідина |__| піна |__| інше (вписати): __________________________________________________________________________________________ 2) назва та склад продукту: __________________________________________________________________________________________ |
|||||||||||
Кількість закупленого продукту |
Кількість розподіленого продукту |
Кількість використаного продукту |
Кількість ліжок в ЗОЗ/ЗСЗ/ |
Кількість працівників в ЗОЗ/ЗСЗ/ |
Кількість медичних працівників ЗОЗ/ЗСЗ/ підрозділі/ |
Кількість пацієнтів, які поступили в ЗОЗ/ЗСЗ/ |
Кількість ліжкоднів, що проведені пацієнтами |
||||
Використано в одиницях (наприклад, одноразових кишенькових диспенсерів) |
Використано в літрах |
Використано в одиницях (наприклад, одноразових кишенькових диспенсерів) |
Використано в літрах |
Використано в одиницях (наприклад, одноразових кишенькових диспенсерів) |
Використано в літрах |
||||||
Місяць 1 (зазначити дати): |
|||||||||||
Загальна кількість |
|||||||||||
Місяць 2 (зазначити дати): |
|||||||||||
Загальна кількість |
|||||||||||
Місяць 3 (зазначити дати): |
|||||||||||
Загальна кількість |
|||||||||||
Місяць 4 (зазначити дати): |
|||||||||||
Загальна кількість |
|||||||||||
Місяць 5 (зазначити дати): |
|||||||||||
Загальна кількість |
|||||||||||
Місяць 6 (зазначити дати): |
|||||||||||
Загальна кількість |
|||||||||||
4. Мило: 1) тип продукту: |__| рідке мило звичайне |__| рідке мило антибактеріальне |__| інше (вписати): _____________________________________________________________________________________________ _____________________________________________________________________________________________ 2) назва та склад продукту: _____________________________________________________________________________________________ _____________________________________________________________________________________________ |
|||||||||||
Кількість закупленого продукту |
Кількість розподіленого продукту |
Кількість використаного продукту |
Кількість ліжок в ЗОЗ/ЗСЗ/ |
Кількість працівників в ЗОЗ/ЗСЗ/ підрозділі/ службі |
Кількість медичних працівників ЗОЗ/ЗСЗ/ |
Кількість пацієнтів, які поступили в ЗОЗ/ЗСЗ/ |
Кількість ліжкоднів, що проведені пацієнтами |
||||
Використано в одиницях (наприклад, каністр) |
Використано в літрах |
Використано в одиницях (наприклад, каністр) |
Використано в літрах |
Використано в одиницях (наприклад, каністр) |
Використано в літрах |
||||||
Місяць 1 (зазначити дати): |
|||||||||||
Загальна кількість |
|||||||||||
Місяць 2 (зазначити дати): |
|||||||||||
Загальна кількість |
|||||||||||
Місяць 3 (зазначити дати): |
|||||||||||
Загальна кількість |
|||||||||||
Місяць 4 (зазначити дати): |
|||||||||||
Загальна кількість |
|||||||||||
Місяць 5 (зазначити дати): |
|||||||||||
Загальна кількість |
|||||||||||
Місяць 6 (зазначити дати): |
|||||||||||
Загальна кількість |
|||||||||||
Додаток 7
до Інструкції з впровадження покращення гігієни рук
в закладах охорони здоров’я та установах / закладах надання
соціальних послуг / соціального захисту населення
(підпункт 4 пункту 5 розділу II, пункт 6 розділу II, підпункт 1
пункту 7 розділу II, підпункт 2 пункту 8 розділу II, пункт 6
розділу III, підпункт 1 пункту 6 розділу VII, підпункт 3 пункту 10
розділу VII, підпункт 7 пункту 13 розділу VII)
Протокол оцінки переносимості і прийнятності антисептику для рук, що використовується або планується до використання у ЗОЗ/ЗСЗ
I. Вступна частина
1. Відповідно до цього Протоколу здійснюється оцінка переносимості шкірою рук і прийнятності антисептику для рук користувачем як найбільш важливих критеріїв при виборі ЗОЗ/ЗСЗ антисептику для рук, які впливають на довготривале його використання і успішне впровадження покращення гігієни рук.
2. Цей Протокол включає два методи оцінки:
1) метод 1 — для оцінки переносимості і прийнятності одного антисептику для рук;
2) метод 2 — для оцінки переносимості і прийнятності двох і більше антисептиків для рук.
Врахування думки і досвіду користувача, що передбачається в обох методах, сприятиме формуванню культури дотримання гігієни рук у ЗОЗ/ЗСЗ.
3. Складові компоненти методів оцінки наведено у таблиці:
Метод 1 |
Метод 2 |
Форма для планування зустрічей (метод 1) |
Форма для планування зустрічей (метод 2) |
Контрольна форма оцінки переносимості і прийнятності антисептику для рук (метод 1) |
Контрольна форма оцінки переносимості і прийнятності антисептику для рук (метод 2) |
Анкета для суб’єктивної оцінки стану шкіри рук, практики гігієни рук та використання антисептику для рук (Частини 1, 2) (видається учасникам оцінки) |
|
Анкета для об’єктивної оцінки стану шкіри рук (видається спостерігачу) |
|
II. Метод 1
1. Оцінка із використанням методу 1 проводиться у разі застосування нового для ЗОЗ/ЗСЗ антисептику для рук або якщо існує необхідність провести оцінку переносимості і прийнятності антисептику для рук при довготривалому його використанні.
2. Для виконання правильного оцінювання учасник повинен використовувати лише досліджуваний антисептик для рук не менше 5 робочих днів поспіль або один місяць звичайного використання.
3. Оцінка проводиться із залученням спостерігача та 40 працівників — учасників оцінки.
4. Оцінка включає в себе наступне:
1) щонайменше 40 учасників використовують не менше 30 мл засобу на день;
2) об’єктивну оцінку: спостерігач/дослідник використовує для оцінки стану шкіри працівника Анкету для об’єктивної оцінки стану шкіри рук;
3) суб’єктивну оцінку: працівники заповнюють Анкету для суб’єктивної оцінки стану шкіри рук, практики гігієни рук та використання антисептику для рук (Частини 1, 2), що призначена для оцінки всіх факторів ризику пошкодження шкіри (а не тільки тих, що пов’язані із використанням засобу), а також прийнятності продукту і переносимості шкірою;
4) проведення оцінювання перед початком використання, через 3 — 5 днів використання та через один місяць використання.
5. Оцінка із використанням методу 1 може бути сліпою (наприклад, роздавання кишенькових диспенсерів без жодних маркувань) або інформованою.
6. Оцінка складається із наступних етапів:
1) ідентифікація учасників, інструктаж та індивідуальне планування оцінювання;
2) використання антисептику для рук і оцінка;
3) введення і аналіз даних (формування звіту);
4) представлення звіту.
7. На етапі ідентифікації учасників, інструктажу та індивідуального планування оцінювання слід виконати наступне:
1) спостерігач/дослідник:
отримує дозвіл керівництва ЗОЗ/ЗСЗ на проведення оцінки та, за можливості, йому виділяється окреме робоче місце в підрозділі, в якому заплановано оцінювання, із тумбою/шафою/сейфом, що закриваються, для зберігання паперів та диспенсерів із антисептиком для рук;
отримує згоду керівників структурних підрозділів, в яких буде проводитися оцінка;
організовує та проводить інформаційні сесії для потенційних учасників серед працівників (висвітлення цілі, процедури і умов проведення, обмежень тощо);
визначає щонайменше 40 учасників та присвоює кожному з них ідентифікаційний номер (наприклад, учасник № 1 або працівник № 01). Номер, що був присвоєний учаснику дослідження, зазначається на Анкеті для суб’єктивної оцінки стану шкіри рук, практики гігієни рук та використання антисептику для рук (Частини 1, 2), кишенькових диспансерах і видається учаснику дослідження в перший день оцінювання. Номер учасника дослідження на Анкеті для об’єктивної оцінки стану шкіри рук, що заповнюється спостерігачем/дослідником, має співпадати з номером на Анкеті для суб’єктивної оцінки стану шкіри рук, практики гігієни рук та використання антисептику для рук (Частини 1, 2), яка заповнюється учасником;
визначає критерії переносимості шкірою і прийнятності продукту (до початку проведення оцінки). Визначені критерії не повідомляються учасникам оцінки;
планує та проводить особисті зустрічі із кожним учасником оцінювання, таким чином, щоб зустрічі проходили в робочий час, при цьому не заважали виконанню професійних обов’язків. Під час зустрічі складається план проведення оцінювання згідно із Формою для планування зустрічей (метод 1) (у двох екземплярах), ознайомлюється з ним учасник, спостерігач надає відповіді на запитання, що виникли у учасника оцінки. За результатом зустрічі спостерігач вносить відповідні дані в Контрольну форму оцінки переносимості і прийнятності антисептику для рук (метод 1);
видає учаснику оцінки один примірник Форми для планування зустрічей (метод 1) із зазначенням контактного номеру телефону спостерігача, примірник із зазначенням контактного номера учасника оцінки залишається у спостерігача;
визначає стан шкіри рук учасника оцінки до, під час та після першого нанесення антисептику для рук та заповнює Анкету для об’єктивної оцінки стану шкіри рук;
2) учасник оцінки отримує та заповнює Анкету для суб’єктивної оцінки стану шкіри рук, практики гігієни рук та використання антисептику для рук (Частини 1, 2);
3) спостерігач може застосувати для оцінки антисептику для рук наступні критерії:
А) критерії прийнятності:
у частині 2 Анкети для суб’єктивної оцінки стану шкіри рук, практики гігієни рук та використання антисептику для рук у розділі «Оцінка засобу гігієни для рук» — колір і аромат — і 50 % відповідей набрали 4 і більше балів;
у частині 2 Анкети для суб’єктивної оцінки стану шкіри рук, практики гігієни рук та використання антисептику для рук у розділі «Оцінка засобу гігієни для рук» — інше — і 75 % відповідей набрали 4 і більше балів;
Б) критерії переносимості шкірою рук:
у частині 2 Анкети для суб’єктивної оцінки стану шкіри рук, практики гігієни рук та використання антисептику для рук у розділі «Самооцінка стану шкіри на руках» — і 75 % відповідей набрали 4 і більше балів;
у Анкеті для об’єктивної оцінки стану шкіри рук — і 75 % відповідей набрали менше 2 балів.
8. Проведення етапу використання антисептику для рук і оцінки:
1) умови, які виконуються учасником оцінки:
для гігієнічної обробки рук протягом одного місяця використовувати тільки антисептик для рук, що оцінюється, за виключенням випадків, коли необхідно помити руки із водою та милом;
не використовувати засоби для захисту шкіри рук (креми, лосьйони, олії тощо) в перші 3 — 5 днів оцінювання;
використовувати не менше 30 мл засобу, що оцінюється, за робочий день;
заповнити Анкету для суб’єктивної оцінки стану шкіри рук, практики гігієни рук та використання антисептику для рук (частина 2) після перших 3 — 5 днів та одного місяця використання засобу, що оцінюється;
заповнити Анкету для суб’єктивної оцінки стану шкіри рук, практики гігієни рук та використання антисептику для рук (частина 1) після одного місяця використання засобу, що оцінюється;
зустрітися із спостерігачем перед початком оцінювання, через 3 — 5 днів та один місяць використання засобу з метою об’єктивної оцінки стану шкіри рук, повернення використаних і отримання заповнених диспенсерів, а також повернення заповнених частин 1, 2 Анкети для суб’єктивної оцінки стану шкіри рук, практики гігієни рук та використання антисептику для рук;
повернути всі диспенсери із засобом, що використовувалися протягом перших 3 — 5 днів оцінювання, в незалежності від того наскільки вони заповнені (пусті, заповнені частково або повні);
заздалегідь попередити спостерігача/дослідника про вихід із оцінювання;
2) спостерігач/дослідник оцінює і записує кількість використаного засобу, що оцінюється, за 3 — 5 днів та один місяць.
9. На етапі введення та аналізу даних спостерігач/дослідник класифікує документи (форми, анкети), перевіряє їх зміст, узгодженість і відповідність, після чого видаляє будь-яку інформацію, що може допомогти в ідентифікації учасника оцінки:
1) опрацьовані відповідно до пункту 9 документи передаються спостерігачем/досліднику спеціалісту зі збору та аналізу даних у підрозділ статистики або відповідальній особі в ВІК для формування аналізу даних та звіту. Звіт оформлюється в довільній формі із обов’язковим зазначенням наступного:
кількість учасників, які почали дослідження та завершили його;
кількість учасників, які вийшли або були виключені з дослідження з вказуванням причини;
узагальнені оцінки відповідно до критеріїв прийнятності та переносимості;
рекомендацію щодо (не-)використання засобу в ЗОЗ/ЗСЗ із зазначенням можливих ризиків, які були виявлені під час дослідження (наприклад, категоричне несприйняття працівниками одного з підрозділів);
2) у випадках, коли проведене оцінювання виявило негативний результат, розкривати будь-яку інформацію щодо виробника та назви продукту (антисептику для рук) категорично заборонено;
3) у випадках, коли результати оцінювання невизначені, оцінку можна повторити або продовжити, а також можна збільшити кількість учасників для підтвердження/анулювання результатів.
10. Керівник ВІК приймає рішення щодо формату та часу представлення результатів зацікавленим сторонам (керівництву ЗОЗ/ЗСЗ, керівникам підрозділів та працівникам).
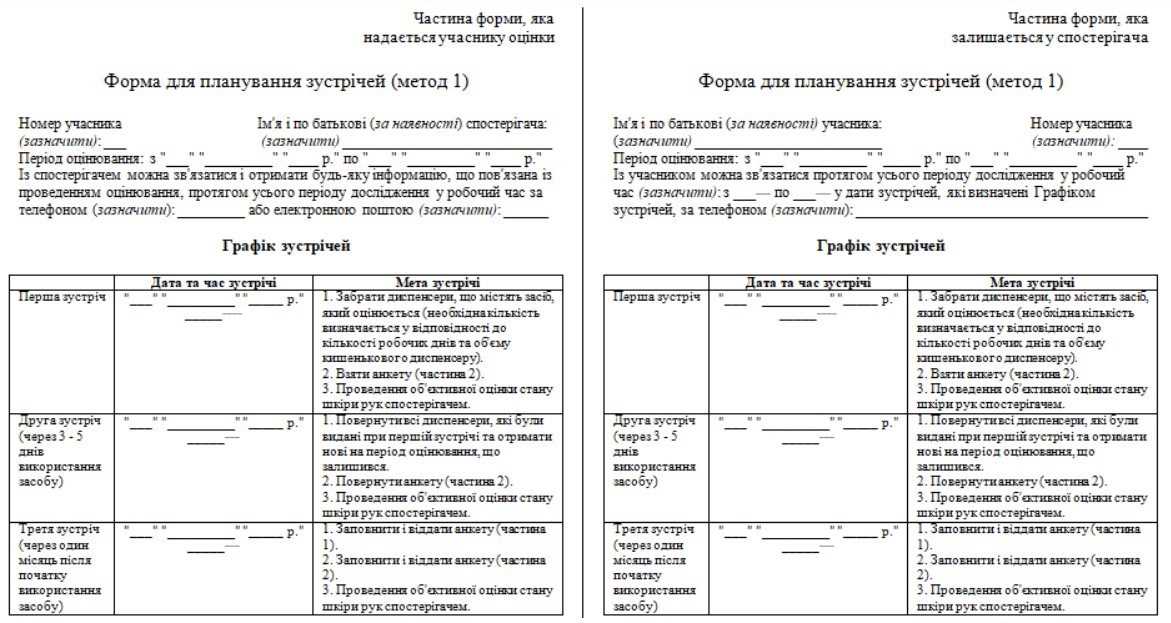
Контрольна форма оцінки переносимості і прийнятності антисептику для рук (метод 1)
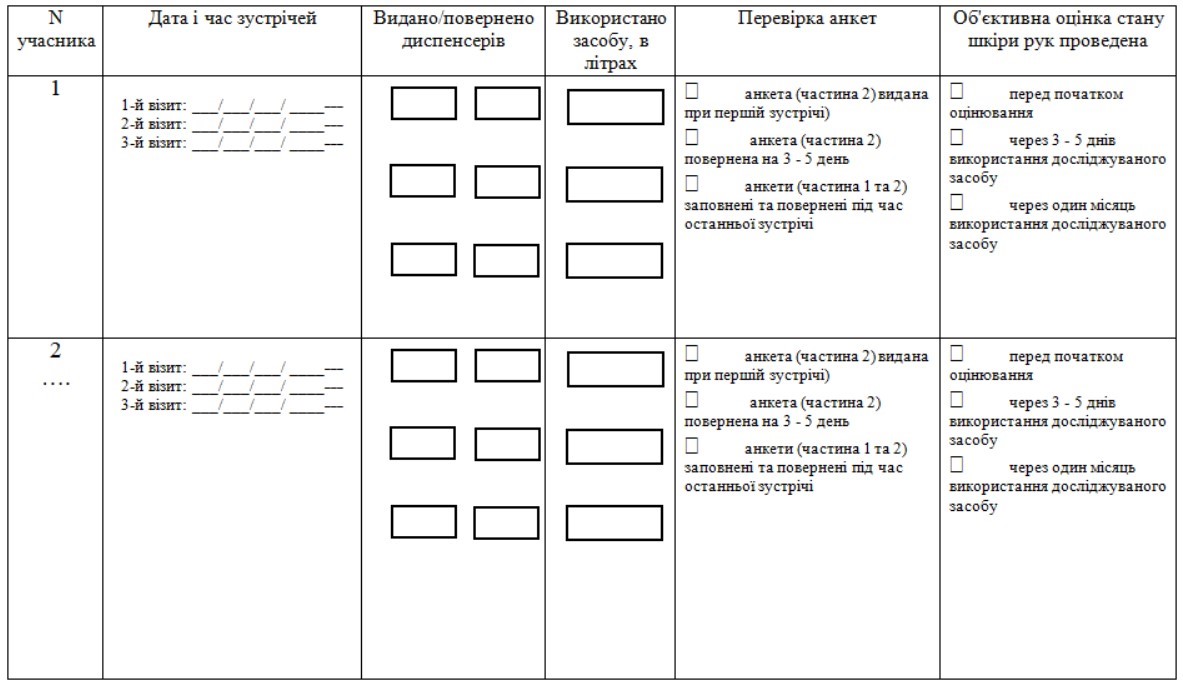
III. Метод 2
1. Оцінка із використанням методу 2 проводиться у ЗОЗ, які надають стаціонарну медичну допомогу та кількість медичних працівників яких складає більше 400, при наявності зацікавленості ЗОЗ в проведенні порівняння переносимості і прийнятності різних антисептиків для рук.
2. Для виконання правильного оцінювання потрібно використовувати кожен із оцінюваних антисептиків для рук не менше 5 робочих днів поспіль.
3. Оцінка проводиться із залученням головного дослідника, спостерігача/дослідника та 40 працівників — учасників оцінки.
Головним дослідником визначається працівник ВІК, який забезпечує організацію проведення оцінки та відповідає за делеговану йому фазу оцінки. Якщо оцінка проводиться у декількох підрозділах, організація оцінки має передбачати проведення оцінки для всіх учасників в одному з цих підрозділів або поетапне проведення оцінки (по завершенню оцінки в одному підрозділі, починається оцінка в іншому підрозділі).
4. Оцінка включає в себе наступне:
1) щонайменше 40 учасників використовують не менше як по 30 мл засобу на день;
2) рандомізоване дослідження: учасники визначаються випадково для проведення оцінювання; учасникам призначається номер, за яким визначається лише розподіл засобу (головний дослідник визначає якому номеру учасника видається диспенсер із відповідним номером). Номера призначаються учасникам в порядку їх зарахування. Ані учасники, ані спостерігачі/дослідники не повинні впливати на розподіл засобів;
3) подвійне сліпе дослідження: ані учасник, ані спостерігач/дослідник (включаючи підрозділ статистики, який проводить оцінку даних) не знають про склад та розподіл різних антисептиків для рук серед учасників;
4) перехресне оцінювання: кожен із учасників почергово оцінює кожен антисептик для рук;
5) об’єктивну оцінку: спостерігач/дослідник використовує для оцінки стану шкіри працівника Анкету для об’єктивної оцінки стану шкіри рук;
6) суб’єктивну оцінку: працівники заповнюють Анкету для суб’єктивної оцінки стану шкіри рук, практики гігієни рук та використання антисептику для рук (Частини 1, 2), що призначена для оцінки всіх факторів ризику пошкодження шкіри (а не тільки тих, що пов’язані із використанням засобу), а також прийнятності продукту і переносимості шкірою.
5. Оцінка складається із наступних етапів:
1) підготовка засобу (антисептику для рук) до оцінювання;
2) ідентифікація учасників, інструктаж та індивідуальне планування оцінювання;
3) використання антисептику для рук і оцінка;
4) введення і аналіз даних (формування звіту);
5) представлення звіту.
6. Підготовка засобу до оцінювання (проводиться фармацевтом або працівником аптеки):
1) (пере-)пакувати засіб в однакові і без будь-яких знаків розрізнення кишенькові диспенсери, вмістом 75, 100 або 125 мл;
2) пронумерувати кожен диспенсер та занести інформацію у відповідну розроблену форму, яка повинна залишатися конфіденційною (передається лише головному досліднику);
3) записати кількість продукту (в літрах) в кожному із диспенсерів (зазначити номер) та передати спостерігачеві/досліднику;
4) розмістити диспенсери по ящикам, у відповідності до груп учасників оцінки (кількість груп має відповідати кількості оцінюваних засобів), та своєчасно видавати їх у підрозділ, де працює учасник;
5) ані учасники, ані спостерігачі/дослідники, ані працівники відділу статистики не повинні знати склад та назву засобу і в який із диспенсерів він поміщений (подвійне сліпе дослідження).
7. На етапі ідентифікації учасників, інструктажу та індивідуального планування оцінювання виконується наступне:
1) спостерігач/дослідник:
отримує дозвіл керівництва ЗОЗ на проведення оцінки та, за можливості, йому виділяється окреме робоче місце в підрозділі, в якому заплановано оцінювання, із тумбою/шафою/сейфом, що закриваються, для зберігання паперів та диспенсерів із антисептиком для рук;
отримує згоду керівників структурних підрозділів, в яких буде проводитися оцінка;
організовує та проводить інформаційні сесії для потенційних учасників серед працівників (висвітлення цілі, процедури і умов проведення, обмежень тощо);
визначає щонайменше 40 учасників та присвоює кожному з них ідентифікаційний номер (наприклад, учасник № 1 або працівник № 01), розподіляє учасників на групи, використовуючи Контрольну форму оцінки переносимості і прийнятності антисептику для рук (метод 2). При цьому спостерігачу важливо знати кожного учасника особисто, однак не використовувати особисту інформацію при проведенні аналізу даних;
зазначає номер, що присвоєний учаснику, на анкетах (Анкета для суб’єктивної оцінки стану шкіри рук, практики гігієни рук та використання антисептику для рук (частини 1, 2), Анкета для об’єктивної оцінки стану шкіри рук), графіку зустрічей (Форма для планування зустрічей (метод 2) і на виданих диспенсерах;
планує та проводить особисті зустрічі із кожним учасником оцінювання, таким чином, щоб зустрічі проходили в робочий час, при цьому не заважали виконанню професійних обов’язків. Під час зустрічі складається план проведення оцінювання згідно із Формою для планування зустрічей (метод 2) (у двох екземплярах), ознайомлюється з ним учасник, спостерігач надає відповіді на запитання, що виникли у учасника оцінки. За результатом зустрічі спостерігач вносить відповідні дані в Контрольну форму оцінки переносимості і прийнятності антисептику для рук (метод 2);
видає учаснику оцінки один примірник Форми для планування зустрічей (метод 2) із зазначенням контактного номеру телефону спостерігача, примірник із зазначенням контактного номера учасника оцінки залишається у спостерігача;
визначає стан шкіри рук учасника оцінки до, під час та після першого нанесення антисептику для рук та заповнює Анкету для об’єктивної оцінки стану шкіри рук;
2) учасник оцінки отримує і заповнює частину 1 Анкети для суб’єктивної оцінки стану шкіри рук, практики гігієни рук та використання антисептику для рук в одному екземплярі та частину 2 цієї анкети у кількості екземплярів, що відповідає кількості антисептиків для рук, що оцінюються.
8. Проведення етапу використання антисептику для рук і оцінки:
1) умови, які виконуються учасником оцінки:
для гігієнічної обробки рук протягом п’яти днів використовувати тільки антисептик для рук, що оцінюється, за виключенням випадків, коли необхідно помити руки із водою та милом;
не використовувати засоби для захисту шкіри рук (креми, лосьйони, олії тощо);
заповнити Анкету для суб’єктивної оцінки стану шкіри рук, практики гігієни рук та використання антисептику для рук (частина 2) після перших 3 — 5 днів використання засобу, що оцінюється;
заповнити Анкету для суб’єктивної оцінки стану шкіри рук, практики гігієни рук та використання антисептику для рук (частина 1) після завершення кожного із етапів оцінювання (дослідження кожного із засобів);
зустрітися із спостерігачем перед початком та після завершення використання кожного із оцінюваних засобів з метою оцінки стану шкіри рук (Анкета для об’єктивної оцінки стану шкіри рук), повернення використаних і отримання заповнених диспенсерів, а також повернення заповнених анкет;
повернути всі диспенсери із засобом, в незалежності від того наскільки вони заповнені (пусті, заповнені частково або повні);
не змінювати свій графік роботи, після того як періоди для оцінки були заплановані, а в разі необхідності — завчасно повідомити спостерігача;
2) спостерігач та учасник мають враховувати, що кожен період оцінки має розділяти період змиття (проміжок часу між оцінюваннями засобів, протягом якого не використовуються антисептики для рук, що дозволяє нівелювати наслідки використання попереднього засобу), який складає щонайменше два дні;
3) спостерігач:
видає учасникам диспенсери без жодних етикеток та написів, що можуть ідентифікувати засіб, і містять лише номери, які визначаються головним дослідником, номери не повинні повторюватися. Крім того, особливу увагу слід звернути на те, що учасник не повинен перейматися тим, де і як отримати оцінюваний засіб (видача повинна проводитися не по закінченню засобу, а заздалегідь);
реєструє кількість виданого засобу для оцінки і порівнює із залишком;
проводить об’єктивну оцінку стану шкіри рук учасника та заповнює Анкету для об’єктивної оцінки стану шкіри рук до та після закінчення оцінки кожного із засобів (антисептиків для рук);
4) періоди оцінювання мають бути однаковими для кожного із засобів (наприклад, 5 робочих днів) та розділятися вихідними/святковими днями (період змиття, який повинен тривати не менше двох днів);
5) оцінка прийнятності та переносимості шкірою рук антисептиків для рук здійснюється шляхом порівняння підрахованих балів по кожному із критеріїв щодо кожного оцінюваного засобу:
А) критерії прийнятності засобу:
у розділі «Оцінка засобу гігієни для рук» частини 2 Анкети для суб’єктивної оцінки стану шкіри рук, практики гігієни рук та використання антисептику для рук — колір і аромат — підрахувати бали для порівняння по кожному засобу;
у розділі «Оцінка засобу гігієни для рук» частини 2 Анкети для суб’єктивної оцінки стану шкіри рук, практики гігієни рук та використання антисептику для рук — інші запитання — підрахувати бали для порівняння по кожному засобу;
Б) критерії переносимості шкірою рук:
у розділі «Самооцінка стану шкіри рук» частини 2 Анкети для суб’єктивної оцінки стану шкіри рук, практики гігієни рук та використання антисептику для рук — підрахувати бали для порівняння по кожному засобу;
у Анкетах для об’єктивної оцінки стану шкіри рук — підрахувати бали для порівняння по кожному засобу.
9. На етапі введення та аналізу даних спостерігач/дослідник класифікує документи (форми, анкети), перевіряє їх зміст, узгодженість і відповідність:
1) опрацьовані відповідно до пункту 9 документи передаються спостерігачем/дослідником спеціалісту зі збору та аналізу даних у підрозділ статистики або відповідальній особі в ВІК для формування аналізу даних та звіту. Звіт оформлюється в довільній формі із обов’язковим зазначенням наступного:
кількість учасників, які почали дослідження та завершили його;
кількість учасників, які вийшли або були виключені з дослідження з вказуванням причини;
узагальнені оцінки відповідно до критеріїв прийнятності та переносимості;
рекомендацію щодо (не-)використання засобу в ЗОЗ із зазначенням можливих ризиків, які були виявлені під час дослідження (наприклад, категоричне несприйняття працівниками одного з підрозділів);
2) після аналізу даних головний дослідник розкриває інформацію щодо складу, назви і виробника оцінюваних засобів (антисептиків для рук).
10. Керівник ВІК приймає рішення щодо формату та часу представлення результатів зацікавленим сторонам (керівництву ЗОЗ, керівникам підрозділів та працівникам).
IV. Анкета для суб’єктивної оцінки стану шкіри рук, практики гігієни рук та використання антисептику для рук*
Частина 1
Учасник № (зазначити): _____ |
Дата повернення анкети: «___» «____» «____ року» |
Оцінка факторів, що впливають на толерантність шкіри:
Вік (зазначити): _____ Стать: |__| чоловіча |__| жіноча Професійна група: |__| лікар |__| сестра медична |__| практикант (середні медичні працівники) |__| практикант (лікарський персонал) |__| допоміжний персонал (молодші медичні працівники, доглядальники(-ці) тощо) |__| інші (зазначити): ____________________________________________________________________ Шкіра: |__| бліда із веснянками |__| рожева із веснянками |__| світло-коричнева |__| коричнева |__| темно-коричнева |__| чорна Поточні кліматичні умови: |__| зима |__| весна |__| осінь |__| літо Чи проводите ви діяльність, що може призвести до пошкодження шкіри? |__| так |__| ні Чи користуєтеся ви засобами для догляду за шкірою рук (креми, лосьйони, олії тощо) поза оцінюванням? |__| більше 5 разів на день |__| до 5 разів на день |__| один раз на день |__| протягом певного сезону (вказати): ______________________ |__| періодично |__| ніколи Чи спостерігався у вас травматичний дерматит? |__| ніколи |__| іноді (вказати з чим пов’язаний): ______________________ |__| постійно Чи хворієте ви на атопічний дерматит? |__| так |__| ні Чи хворієте ви на алергічний риніт/кон’юнктивіт? |__| так |__| ні Чи хворієте ви на бронхіальну астму? |__| так |__| ні Чи є у вас непереносимість алкоголю? |__| так |__| ні |
Оцінка частоти практик гігієни рук:
Ви працюєте повний робочий день (8 годин)? |__| так |__| ні Якщо ви працюєте неповний робочий день, то вкажіть який із запропонованих варіантів підходить у вашому випадку найбільше? |__| менше 4 годин |__| 4 години |__| 5 годин |__| 6 годин |__| 7 годин Як довго ви використовуєте антисептик для рук на роботі? |__| вперше |__| менше одного року |__| більше одного року, але менше п’яти |__| більше п’яти років Як ви думаєте, чи зможете ви покращити власне дотримання практики гігієни рук? |__| так |__| ні |__| можливо Ви можете не використовувати антисептик для рук, тому що: |
|||||||
Забуваєте: |
завжди |
|__| |
|__| |
|__| |
|__| |
|__| |
ніколи |
Маєте недостатньо часу: |
завжди |
|__| |
|__| |
|__| |
|__| |
|__| |
ніколи |
Маєте пошкоджену шкіру: |
завжди |
|__| |
|__| |
|__| |
|__| |
|__| |
ніколи |
Частина 2
Учасник № (зазначити): _____ |
Дата повернення анкети: «___» «_____» «____ року» |
Кількість виданих диспенсерів (зазначити): _____ Кількість виданого засобу в літрах (зазначити): _________ Кількість повернених диспенсерів (зазначити): _________ Кількість використаного засобу (зазначити): ______ |
|
Оцінка частоти практик гігієни рук
Скільки робочих днів (8 годин) підряд ви використовували засіб? |__| 3 дні |__| 4 дні |__| 5 днів |__| 6 днів |__| 7 днів |__| більше 7 днів Як часто ви мали контакт із пацієнтом протягом робочого дня під час проведення дослідження (в середньому)? |__| менше одного |__| від одного до п’яти |__| від шести до десяти |__| від одинадцяти до п’ятнадцяти |__| більше п’ятнадцяти В скількох відсотках випадків, коли необхідно було виконати гігієнічну обробку рук, ви її виконували? |__| 0% |__| 10% |__| 20% |__| 30% |__| 40% |__| 50% |__| 60% |__| 70% |__| 80% |__| 90% |__| 100% Чи змінило це оцінювання ваше дотримання практики гігієни рук? |__| так |__| ні Скільки разів із останніх п’яти практик з гігієни рук ви використовували засоби для миття рук? |__| 0 |__| 1 |__| 2 |__| 3 |__| 4 |__| 5 Як часто, в середньому, ви практикуєте гігієну рук протягом робочого дня (за період проведення оцінювання)? |__| менше одного |__| від одного до п’яти |__| від шести до десяти |__| від одинадцяти до п’ятнадцяти |__| більше п’ятнадцяти |
Оцінка засобу гігієни для рук
Що ви думаєте про оцінюваний продукт**? |
|||||||
Колір: |
неприємний |
|__| |
|__| |
|__| |
|__| |
|__| |
приємний |
Запах: |
неприємний |
|__| |
|__| |
|__| |
|__| |
|__| |
приємний |
Текстура: |
дуже липка |
|__| |
|__| |
|__| |
|__| |
|__| |
зовсім не липка |
Подразнення: |
дуже подразнює |
|__| |
|__| |
|__| |
|__| |
|__| |
не подразнює |
Ефект висушування шкіри: |
сильний |
|__| |
|__| |
|__| |
|__| |
|__| |
відсутній |
Простота використання: |
складно |
|__| |
|__| |
|__| |
|__| |
|__| |
легко |
Швидкість висихання: |
швидко |
|__| |
|__| |
|__| |
|__| |
|__| |
повільно |
Застосування: |
приємне |
|__| |
|__| |
|__| |
|__| |
|__| |
неприємне |
Загальна оцінка: |
незадовільно |
|__| |
|__| |
|__| |
|__| |
|__| |
відмінно |
Чи є відмінності між оцінюваним засобом та засобом, що використовуються у вашому ЗОЗ? |
|||||||
суттєві |
|__| |
|__| |
|__| |
|__| |
|__| |
відсутні |
|
Який засіб вам подобається більше? |__| що вже використовується (0 балів) |__| що оцінюється (5 балів) |__| не надаю перевагу жодному (0 балів) |
|||||||
Як ви вважаєте, оцінюваний засіб може підвищити частоту дотримання практики гігієни рук в ЗОЗ**? |
|||||||
беззаперечно так |
|__| |
|__| |
|__| |
|__| |
|__| |
категорично ні |
|
Оцінка стану шкіри рук
Самооцінка стану шкіри рук** (після використання оцінюваного засобу): Зовнішній вигляд (почервоніння, висип, плямистість тощо): |
|||||||
нездорова |
|__| |
|__| |
|__| |
|__| |
|__| |
нормальна |
|
Садна і тріщини: |
велика кількість |
|__| |
|__| |
|__| |
|__| |
|__| |
відсутні |
Сухість: |
виражена |
|__| |
|__| |
|__| |
|__| |
|__| |
відсутня |
Неприємні відчуття (свербіж, печіння, болісність): |
|||||||
виражені |
|__| |
|__| |
|__| |
|__| |
|__| |
відсутні |
|
Як би ви оцінили цілісність шкіри рук? |
|||||||
незадовільна |
|__| |
|__| |
|__| |
|__| |
|__| |
відмінна |
|
________ Частина 2 цієї анкети заповнюється по методу 1 — через 3–5 днів та через один місяць використання антисептику для рук, по методу 2 — через 3–5 днів використання антисептику для рук. |__| ** зліва на право відповідає оцінці від 1 до 5 балів. Розподіл балів, що наведений у Протоколі, не надається учаснику. |
V. Анкета для об’єктивної оцінки стану шкіри рук
Учасник № (зазначити): ____ Дата першої оцінки : «___» «__________» «_____ року» Дата другої оцінки : «___» «__________» «_____ року» Дата третьої оцінки : «___» «__________» «_____ року» |
Шкала оцінки стану шкіри рук спостерігачем
До початку оцінювання |
Через 3 — 5 днів використання |
Через один місяць використання |
|||||||||||||
Почервоніння |
0 |
1 |
2 |
3 |
4 |
0 |
1 |
2 |
3 |
4 |
0 |
1 |
2 |
3 |
4 |
0 — відсутність почервоніння; 1 — легке почервоніння або плямистість; 2 — помірне почервоніння, що рівномірно розподілене; 3 — значне почервоніння; 4 — значне почервоніння із набряком |
|||||||||||||||
Лущення |
0 |
1 |
2 |
3 |
0 |
1 |
2 |
3 |
0 |
1 |
2 |
3 |
|||
0 — лущення відсутнє; 1 — слабко виражене і не розповсюджене; 2 — помірно виражене; 3 — виражене. |
|||||||||||||||
Тріщини |
0 |
1 |
2 |
3 |
0 |
1 |
2 |
3 |
0 |
1 |
2 |
3 |
|||
0 — відсутні; 1 — одиничні неглибокі; 2 — глибокі одиничні або множинні неглибокі; 3 — великі тріщини із кровотечою або просочуванням. |
|||||||||||||||
Шкала візуального оцінювання стану шкіри рук
Жодних видимих змін кольору, лущення або пошкоджень |
0 |
0 |
0 |
Незначне почервоніння, що нерівномірно розподілене |
1 |
1 |
1 |
Шкіра суха та/або наявне почервоніння |
2 |
2 |
2 |
Дуже суха шкіра із блідим відтінком груба на дотик таабо із наявним почервонінням, але без тріщин |
3 |
3 |
3 |
Потріскана поверхня шкіри, але без кровотечі/просочування |
4 |
4 |
4 |
Велика кількість тріщин на поверхні шкіри із кровотечою/ просочуванням |
5 |
5 |
5 |
Примітка: 1. ця анкета заповнюється спостерігачем по методу 1 — тричі: до початку використання засобу, через 3–5 днів та один місяць після початку використання засобу, по методу 2 — до оцінювання та через 3–5 днів; 2. у шкалі оцінки стану шкіри рук спостерігачем необхідно відзначити лише один із запропонованих варіантів відповідей. |
|||
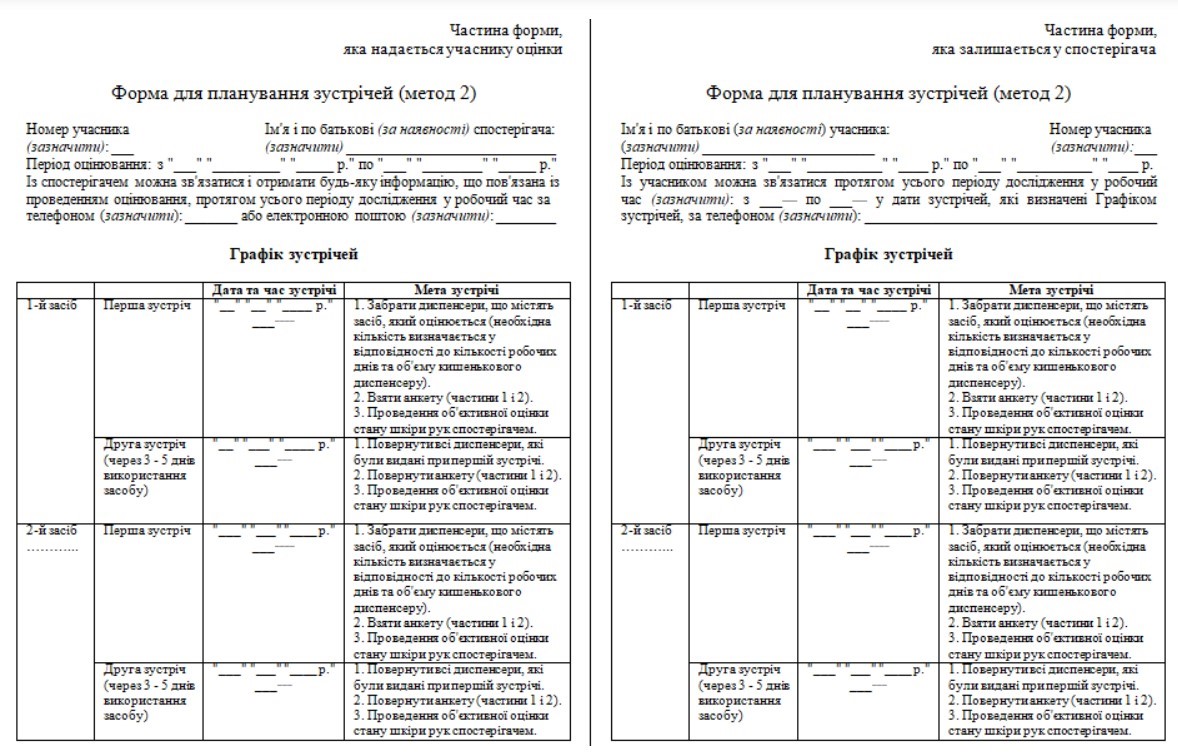
Контрольна форма оцінки переносимості і прийнятності антисептику для рук (метод 2)
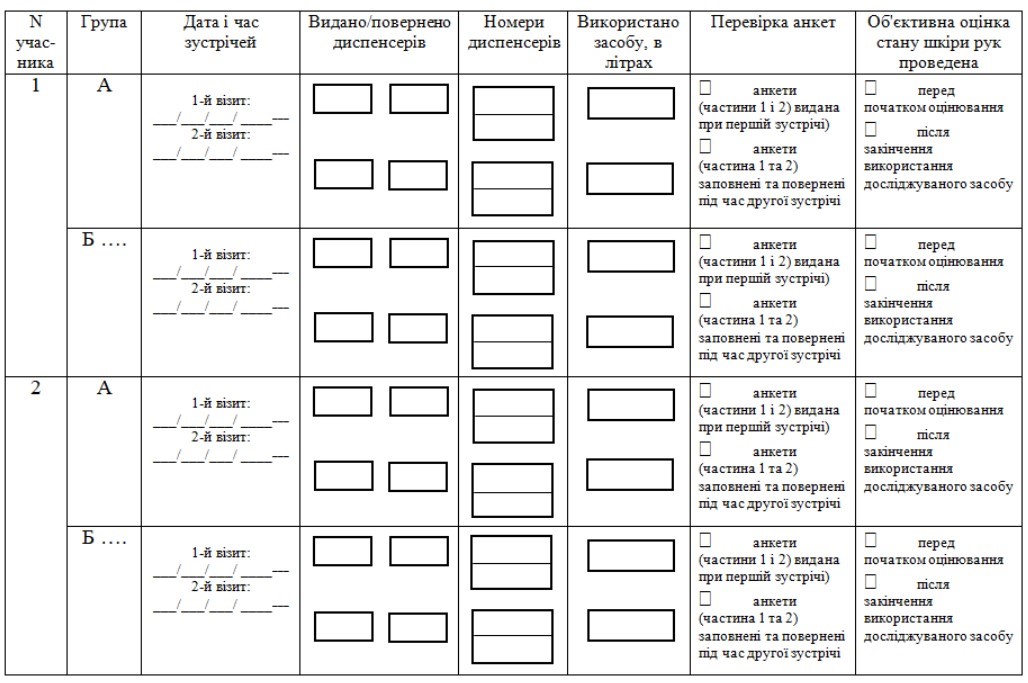
Примітка: структура цієї форми визначає випадковий розподіл (два рядки на кожного учасника), що відповідає оцінюванню двох засобів. При необхідності додається така кількість рядків, яка відповідає кількості засобів щодо яких проводиться оцінка.
Додаток 8
до Інструкції з впровадження покращення гігієни рук
в закладах охорони здоров’я та установах / закладах надання
соціальних послуг / соціального захисту населення
(підпункт 2 пункту 8 розділу II, пункт 8 розділу VII)
Примірний план-графік проведення базової оцінки для впровадження покращення гігієни рук у ЗОЗ/ЗСЗ
Вид оцінки |
Строки проведення |
||||
Оцінка інфраструктури і ресурсів |
перший — другий тижні |
||||
Оцінка сприйняття гігієни рук керівництвом ЗОЗ/ЗСЗ |
третій тиждень |
||||
Оцінка сприйняття гігієни рук працівниками |
четвертий — п’ятий тижні |
||||
Оцінка дотримання правил гігієни рук працівниками |
шостий — восьмий тижні |
||||
Оцінка використання засобів для гігієни рук |
в кінці кроку 2, надалі щомісяця протягом першого року впровадження та щоквартально в подальшому |
||||
Оцінка знань працівників щодо гігієни рук |
за тиждень або безпосередньо перед початком навчання |
||||
Оцінка переносимості і прийнятності антисептику для рук |
третій — восьмий тижні |
||||
Додаток 9
до Інструкції з впровадження покращення гігієни рук
в закладах охорони здоров’я та установах / закладах надання
соціальних послуг / соціального захисту населення
(підпункт 2 пункту 8 розділу II, пункт 16 розділу VII)
Примірний план-графік проведення оцінки впливу впровадження покращення гігієни рук у ЗОЗ/ЗСЗ
Вид оцінки |
Строки проведення |
||||
Оцінка інфраструктури і ресурсів |
перший — другий тижні |
||||
Оцінка сприйняття гігієни рук керівництвом ЗОЗ/ЗСЗ |
третій тиждень |
||||
Оцінка сприйняття гігієни рук працівниками та оцінка переносимості і прийнятності антисептику для рук, що використовується або планується до використання у ЗОЗ/ЗСЗ |
четвертий — восьмий тижні |
||||
Оцінка дотримання правил гігієни рук працівниками |
шостий — восьмий тижні |
||||
Оцінка використання засобів для гігієни рук |
щомісяця протягом першого року впровадження та щоквартально в подальшому |
||||
Оцінка знань працівників щодо гігієни рук |
за тиждень або безпосередньо перед початком навчання |
||||
Додаток 10
до Інструкції з впровадження покращення гігієни рук
в закладах охорони здоров’я та установах / закладах надання
соціальних послуг / соціального захисту населення
(пункт 6 розділу III, пункт 11 розділу V, підпункт 1 пункту 6 розділу VII,
підпункт 1 пункту 14 розділу VII, підпункт 2 пункту 17 розділу VII)
Протокол для оцінки сприйняття працівниками та керівництвом ЗОЗ/ЗСЗ необхідності попередження ІПНМД, важливості гігієни рук
I. Вступна частина
1. Цей Протокол використовується для визначення сприйняття працівниками та керівництвом ЗОЗ/ЗСЗ необхідності попередження ІПНМД, важливості гігієни рук як профілактичного заходу і ефективності всіх компонентів ММС. Сприйняття працівниками та керівництвом ЗОЗ/ЗСЗ необхідності попередження ІПНМД, важливості гігієни рук безпосередньо впливає на:
1) їх готовність прийняти зміни в системі;
2) створення культури безпеки та гігієни рук у ЗОЗ/ЗСЗ;
3) виділення ресурсів для реалізації плану дій з покращення гігієни рук.
2. Оцінка відповідно до цього Протоколу проводиться серед керівництва ЗОЗ/ЗСЗ та у всіх підрозділах, де впроваджується план дій з покращення гігієни рук, з метою:
1) базової оцінки сприйняття гігієни рук, до початку реалізації заходів з покращення гігієни рук;
2) наступної оцінки (щонайбільше через один рік) для визначення впливу плану дій з покращення гігієни рук;
3) регулярної оцінки після впровадження заходів з покращення гігієни рук (не рідше одного разу на рік) для моніторингу стійкості покращення та винайдення областей, що потребують додаткового втручання.
3. Цей Протокол включає такі анкети:
1) Анкета базової оцінки сприйняття працівниками ЗОЗ/ЗСЗ необхідності попередження ІПНМД, важливості гігієни рук;
2) Анкета оцінки сприйняття працівниками ЗОЗ/ЗСЗ необхідності попередження ІПНМД, важливості гігієни рук;
3) Анкета оцінки сприйняття керівництвом ЗОЗ/ЗСЗ необхідності попередження ІПНМД, важливості гігієни рук.
4. Цей Протокол виконується спостерігачем/дослідником.
5. Анкетування відповідно до цього Протоколу проводиться анонімно та рандомно. У випадках, коли рандомізація неможлива:
1) якщо задіяно всього декілька підрозділів, анкети роздаються всім працівникам протягом одного тижня та збираються заповненими через 4 — 5 днів;
2) якщо в оцінці беруть участь декілька підрозділів або ЗОЗ/ЗСЗ цілком, анкети роздаються всім працівникам, що присутні на роботі, в один конкретний день (вранці) і збираються заповненими в кінці робочого дня.
Анкетування керівництва ЗОЗ/ЗСЗ також проводиться анонімно — анкети роздаються керівним працівникам та збираються заповненими через 4 — 5 днів.
Анкета базової оцінки сприйняття працівниками ЗОЗ/ЗСЗ необхідності попередження ІПНМД, важливості гігієни рук
Ідентифікаційний номер*: __________
________ Так як Ви щоденно знаходитеся в безпосередньому контакті із пацієнтами, нам цікава Ваша думка щодо інфекційних хвороб, пов’язаних із наданням медичної допомоги та гігієни рук. Заповнення анкети займе у Вас не більше 10 хвилин. На кожне запитання є лише одна правильна відповідь. Будь-ласка уважно прочитайте запитання і лише тоді відповідайте. Короткий словник: антисептик для рук — спиртовмісний дезінфекційний засіб (рідина, гель або піна), що застосовується для нанесення на шкіру рук з метою знищення мікроорганізмів; гігієнічна обробка рук — обробка рук шляхом втирання антисептика для рук в шкіру рук; миття рук — миття рук милом та водою. |
|||
Дата: |
Назва ЗОЗ/ЗСЗ: |
||
Місто: |
Регіон/Область: |
||
Прізвище, ім’я та по батькові (за наявності)**: |
Інше: |
||
________ 1. Стать: |__| чоловіча |__| жіноча 2. Вік: _____ років. 3. Професійна група: |__| лікар |__| сестра медична |__| практикант (середні медичні працівники) |__| практикант (лікарський персонал) |__| допоміжний персонал (молодші медичні працівники, доглядальники (-ці) тощо) |__| інші (зазначити): ____________________________________________________________________ 4. Напрям діяльності: |__| терапевтичний/внутрішні хвороби |__| хірургічний |__| інтенсивна терапія |__| змішаний (надається різнопрофільна допомога в залежності від потреби) |__| невідкладна допомога/приймальне відділення |__| акушерство |__| педіатрія |__| реабілітація |__| хоспісна допомога |__| денний стаціонар |__| довготривалого перебування |__| інше (вписати): _____________________________________________________________________ 5. Чи проходили Ви навчання із гігієни рук за останні три роки? |__| так |__| ні 6. Чи використовуєте Ви на регулярній основі антисептик з метою проведення гігієнічної обробки рук? |__| так |__| ні 7. У якого відсотка пацієнтів, на Вашу думку, виникнуть інфекційні хвороби, пов’язані із наданням медичної допомоги, у Вашому ЗОЗ/ЗСЗ (від 0 до 100 %)? |__| ______ % |__| важко відповісти 8. Наскільки виражено, на Вашу думку, впливають інфекційні хвороби, пов’язані із наданням медичної допомоги, на результат лікування пацієнтів? |__| не впливають |__| впливають незначно |__| впливають суттєво |__| можуть стати причиною неефективного лікування |__| важко відповісти 9. Наскільки ефективна, на Вашу думку, гігієна рук для профілактики інфекційних хвороб, пов’язаних із наданням медичної допомоги? |__| не ефективна |__| впливає незначно |__| впливає суттєво |__| важко відповісти 10. Чи є пріоритетом гігієна рук у Вашому ЗОЗ/ЗСЗ? |__| не є пріоритетом |__| низька пріоритетність |__| середня пріоритетність |__| висока пріоритетність |__| важко відповісти 11. В якому відсотку випадків, що потребують виконання практики гігієни рук, в середньому, на Вашу думку, працівники дійсно її виконують (враховується миття рук милом і водою та обробка антисептиком)? |__| ______ % |__| важко відповісти 12. Наскільки ефективними будуть, на Вашу думку, наступні заходи, які направлені на постійне покращення дотримання практик гігієни рук, у Вашому ЗОЗ/ЗСЗ (у кожному із пунктів зазначте лише одну відповідь)? |
||||||
1) Керівництво ЗОЗ/ЗСЗ відкрито підтримує заходи із покращення гігієни рук: |
||||||
без будь-якого ефекту |
|__| |
|__| |
|__| |
|__| |
|__| |
надзвичайний ефект |
2) В ЗОЗ/ЗСЗ будуть встановлені диспенсери із антисептиком для рук в кожній точці догляду: |
||||||
без будь-якого ефекту |
|__| |
|__| |
|__| |
|__| |
|__| |
надзвичайний ефект |
3) Інформаційні плакати/стенди встановлені поряд із точками догляду з метою постійного нагадування: |
||||||
без будь-якого ефекту |
|__| |
|__| |
|__| |
|__| |
|__| |
надзвичайний ефект |
4) Кожен працівник проходить щорічне навчання із гігієни рук: |
||||||
без будь-якого ефекту |
|__| |
|__| |
|__| |
|__| |
|__| |
надзвичайний ефект |
5) В ЗОЗ/ЗСЗ розроблені, затверджені та розповсюджені серед всіх працівників прості та зрозумілі стандартні операційні процедури щодо практик гігієни рук: |
||||||
без будь-якого ефекту |
|__| |
|__| |
|__| |
|__| |
|__| |
надзвичайний ефект |
6) Працівники регулярно отримують зворотній зв’язок від координатора з гігієни рук щодо результатів впровадження: |
||||||
без будь-якого ефекту |
|__| |
|__| |
|__| |
|__| |
|__| |
надзвичайний ефект |
7) Ви — приклад для наслідування в дотриманні практик гігієни рук: |
||||||
без будь-якого ефекту |
|__| |
|__| |
|__| |
|__| |
|__| |
надзвичайний ефект |
8) Пацієнтам запропоновано нагадувати працівникам щодо необхідності виконати практику гігієни рук: |
||||||
без будь-якого ефекту |
|__| |
|__| |
|__| |
|__| |
|__| |
надзвичайний ефект |
13. Чи підтримує керівник Вашого підрозділу дотримання оптимальних практик гігієни рук? |
||||||
не підтримує |
|__| |
|__| |
|__| |
|__| |
|__| |
повністю підтримує |
14. Чи підтримують Ваші колеги дотримання оптимальних практик гігієни рук? |
||||||
не підтримують |
|__| |
|__| |
|__| |
|__| |
|__| |
повністю підтримують |
15. Як Ви оцінюєте зусилля, що докладаються у Вашому ЗОЗ/ЗСЗ задля підтримки оптимальної повсякденної практики гігієни рук? |
||||||
незадовільні |
|__| |
|__| |
|__| |
|__| |
|__| |
відмінні |
16. В якому відсотку випадків, що потребують використання практик гігієни рук, в середньому Ви їх дотримуєтесь (миття або обробка антисептиком)? |__| _____ % |__| не дотримуюсь взагалі |__| важко відповісти |
||||||
Дякуємо за Ваші відповіді!
Анкета оцінки сприйняття працівниками ЗОЗ/ЗСЗ необхідності попередження ІПНМД, важливості гігієни рук
Ідентифікаційний номер*: _______________
________ Так як Ви щоденно знаходитеся в безпосередньому контакті із пацієнтами, нам цікава Ваша думка щодо інфекційних хвороб, пов’язаних із наданням медичної допомоги та гігієни рук. Заповнення анкети займе у Вас не більше 10 хвилин. На кожне запитання є лише одна правильна відповідь. Будь-ласка уважно прочитайте запитання і лише тоді відповідайте. Ви вже проходили базове оцінювання щодо цього питання. Ця анкета відрізняється деякими додатковими запитаннями, що дадуть нам змогу отримати Вашу думку щодо стратегій та інструментів, які наразі використовуються для просування гігієни рук у ЗОЗ/ЗСЗ. Короткий словник: антисептик для рук — спиртовмісний дезінфекційний засіб (рідина, гель або піна), що застосовується для нанесення на шкіру рук з метою знищення мікроорганізмів; гігієнічна обробка рук — обробка рук шляхом втирання антисептика для рук в шкіру рук; миття рук — миття рук з милом та водою. |
Дата: |
Назва ЗОЗ/ЗСЗ: |
||
Місто: |
Регіон/Область: |
||
Прізвище, ім’я та по батькові (за наявності)**: |
Інше: |
________ 1. Стать: |__| чоловіча |__| жіноча 2. Вік: _____ років 3. Професійна група: |__| лікар |__| сестра медична |__| практикант (середні медичні працівники) |__| практикант (лікарський персонал) |__| допоміжний персонал (молодші медичні працівники, доглядальники (-ці) тощо) |__| інші (зазначити): ____________________________________________________________________ 4. Напрям діяльності: |__| терапевтичний/внутрішні хвороби |__| хірургічний |__| інтенсивна терапія |__| змішаний (надається різнопрофільна допомога в залежності від потреби) |__| невідкладна допомога/приймальне відділення |__| акушерство |__| педіатрія |__| реабілітація |__| хоспісна допомога |__| денний стаціонар |__| довготривалого перебування |__| інше (вписати): _____________________________________________________________________ 5. Чи проходили Ви навчання із гігієни рук за останні три роки? |__| так |__| ні 6. Чи використовуєте Ви на регулярній основі антисептик з метою проведення гігієнічної обробки рук? |__| так |__| ні 7. У якого відсотка пацієнтів, на Вашу думку, виникнуть інфекційні хвороби, пов’язані із наданням медичної допомоги, у Вашому ЗОЗ/ЗСЗ (від 0 до 100 %)? |__| ______ % |__| важко відповісти 8. Наскільки виражено, на Вашу думку, впливають інфекційні хвороби, пов’язані з наданням медичної допомоги, на результат лікування пацієнтів? |__| не впливають |__| впливають незначно |__| впливають суттєво |__| можуть стати причиною неефективного лікування |__| важко відповісти 9. Наскільки ефективна, на Вашу думку, гігієна рук для профілактики інфекційних хвороб, пов’язаних із наданням медичної допомоги? |__| не ефективна |__| впливає незначно |__| впливає суттєво |__| важко відповісти 10. Чи є пріоритетом гігієна рук у Вашому ЗОЗ/ЗСЗ? |__| не є пріоритетом |__| низька пріоритетність |__| середня пріоритетність |__| висока пріоритетність |__| важко відповісти 11. В якому відсотку випадків, що потребують виконання практики гігієни рук, в середньому, на Вашу думку, працівники дійсно її виконують (враховується миття рук милом і водою та обробка антисептиком для рук)? |__| ______ % |__| важко відповісти 12. Наскільки ефективними будуть, на Вашу думку, наступні заходи, які направлені на постійне покращення дотримання практик гігієни рук, у Вашому ЗОЗ/ЗСЗ (у кожному із пунктів зазначте лише одну відповідь)? |
||||||
1) Керівництво ЗОЗ/ЗСЗ відкрито підтримує заходи із покращення гігієни рук: |
||||||
без будь-якого ефекту |
|__| |
|__| |
|__| |
|__| |
|__| |
надзвичайний ефект |
2) В ЗОЗ/ЗСЗ будуть встановлені диспенсери із антисептиком для рук в кожній точці догляду: |
||||||
без будь-якого ефекту |
|__| |
|__| |
|__| |
|__| |
|__| |
надзвичайний ефект |
3) Інформаційні плакати/стенди встановлені поряд із точками догляду з метою постійного нагадування: |
||||||
без будь-якого ефекту |
|__| |
|__| |
|__| |
|__| |
|__| |
надзвичайний ефект |
4) Кожен працівник проходить щорічне навчання із гігієни рук: |
||||||
без будь-якого ефекту |
|__| |
|__| |
|__| |
|__| |
|__| |
надзвичайний ефект |
5) В ЗОЗ/ЗСЗ розроблені, затверджені та розповсюджені серед всіх працівників прості та зрозумілі стандартні операційні процедури щодо практик гігієни рук: |
||||||
без будь-якого ефекту |
|__| |
|__| |
|__| |
|__| |
|__| |
надзвичайний ефект |
6) Працівники регулярно отримують зворотній зв’язок від координатора з гігієни рук щодо результатів впровадження: |
||||||
без будь-якого ефекту |
|__| |
|__| |
|__| |
|__| |
|__| |
надзвичайний ефект |
7) Ви — приклад для наслідування в дотриманні практик гігієни рук: |
||||||
без будь-якого ефекту |
|__| |
|__| |
|__| |
|__| |
|__| |
надзвичайний ефект |
8) Пацієнтам запропоновано нагадувати працівникам щодо необхідності виконати практику гігієни рук: |
||||||
без будь-якого ефекту |
|__| |
|__| |
|__| |
|__| |
|__| |
надзвичайний ефект |
13. Чи підтримує керівник Вашого підрозділу дотримання оптимальних практик гігієни рук? |
||||||
не підтримує |
|__| |
|__| |
|__| |
|__| |
|__| |
повністю підтримує |
14. Чи підтримують Ваші колеги дотримання оптимальних практик гігієни рук? |
||||||
не підтримують |
|__| |
|__| |
|__| |
|__| |
|__| |
повністю підтримують |
15. Як Ви оцінюєте зусилля, що докладаються у Вашому ЗОЗ/ЗСЗ задля підтримки оптимальної повсякденної практики гігієни рук? |
||||||
незадовільні |
|__| |
|__| |
|__| |
|__| |
|__| |
відмінні |
16. В якому відсотку випадків, що потребують використання практик гігієни рук, в середньому Ви їх дотримуєтесь (миття або обробка антисептиком для рук)? |__| _____ % |__| не дотримуюсь взагалі |__| важко відповісти |
||||||
17. Чи спростило використання антисептиків для рук дотримання правил гігієни рук? |
||||||
взагалі ні |
|__| |
|__| |
|__| |
|__| |
|__| |
значно спростило |
18. Чи добре Ви переносите антисептик для рук, що використовується у Вашому ЗОЗ/ЗСЗ? |
||||||
взагалі не переношу |
|__| |
|__| |
|__| |
|__| |
|__| |
відмінно переношу |
19. Чи допомогли Вам і Вашим колегам знання щодо результатів оцінювання в подальшому дотримуватися оптимальних практик гігієни рук? |
||||||
взагалі не допомогло |
|__| |
|__| |
|__| |
|__| |
|__| |
спонукало до дії |
20. Наскільки факт періодичних повторних оцінок щодо дотримання практик гігієни рук спонукав Вас до дії? |
||||||
не звертав(-ла) увагу |
|__| |
|__| |
|__| |
|__| |
|__| |
спонукало до дії |
21. Чи були навчальні і підготовчі заходи, в яких Ви брали участь, корисними для Вас в сенсі спонукання до подальшої підтримки оптимальних практик гігієни рук? |
||||||
взагалі ні |
|__| |
|__| |
|__| |
|__| |
|__| |
спонукало до дії |
22. Чи вважаєте Ви, що керівництво Вашого ЗОЗ/ЗСЗ підтримує заходи з покращення гігієни рук? |
||||||
взагалі ні |
|__| |
|__| |
|__| |
|__| |
|__| |
повністю підтримує |
23. Чи допомогло Вам покращення культури безпеки (у випадку, якщо в результаті впровадження покращення гігієни рук, культура безпеки дійсно покращилася) покращити власну практику гігієни рук? |
||||||
взагалі ні |
|__| |
|__| |
|__| |
|__| |
|__| |
цілковито так |
24. Чи стали Ви краще розуміти свою роль в боротьбі із інфекційними хворобами, пов’язаними із наданням медичної допомоги після впровадження в ЗОЗ/ЗСЗ покращення гігієни рук? |
||||||
взагалі ні |
|__| |
|__| |
|__| |
|__| |
|__| |
цілковито так |
Дякуємо за Ваші відповіді!
Анкета оцінки сприйняття керівництвом ЗОЗ/ЗСЗ необхідності попередження ІПНМД, важливості гігієни рук
Ідентифікаційний номер*: __________________
________ Так як Ви займаєте керівну посаду у ЗОЗ/ЗСЗ, нам цікава Ваша думка щодо інфекційних хвороб, пов’язаних із наданням медичної допомоги і гігієни рук. Заповнення анкети займе у Вас не більше 10 хвилин. На кожне запитання є лише одна правильна відповідь. Будь-ласка уважно прочитайте запитання і лише тоді відповідайте. Короткий словник: антисептик для рук — спиртовмісний дезінфекційний засіб (рідина, гель або піна), що застосовується для нанесення на шкіру рук з метою знищення мікроорганізмів; гігієнічна обробка рук — обробка рук шляхом втирання антисептика для рук в шкіру рук; миття рук — миття рук з милом та водою. |
Дата: |
Назва ЗОЗ/ЗСЗ: |
||
Місто: |
Регіон/Область: |
||
Прізвище, ім’я та по батькові (за наявності)**: |
Інше: |
________ 1. Стать: |__| чоловіча |__| жіноча 2. Час, протягом якого Ви займаєте дану посаду: _______ років. 3. Час, протягом якого Ви працюєте в цьому ЗОЗ/ЗСЗ: _______ років. 4. Посада: |__| керівник |__| медичний директор/заступник керівника |__| головна сестра медична |__| інша посада (зазначити): _____________________________________________________________ 5. Чи наявний у Вас попередній досвід впровадження покращення гігієни рук? |__| так |__| ні 6. Чи використовується у Вашому ЗОЗ/ЗСЗ антисептик для рук, що закуповується централізовано ЗОЗ/ЗСЗ? |__| так |__| ні 7. У якого відсотка пацієнтів, на Вашу думку, виникнуть інфекційні хвороби, пов’язані із наданням медичної допомоги, у підпорядкованому Вам ЗОЗ/ЗСЗ (від 0 до 100 %)? |__| ______ % |__| важко відповісти 8. Наскільки виражено, на Вашу думку, впливають інфекційні хвороби, пов’язані із наданням медичної допомоги, на результат лікування пацієнтів? |__| не впливають |__| впливають незначно |__| впливають суттєво |__| можуть стати причиною неефективного лікування |__| важко відповісти 9. Як в цілому, на Вашу думку, впливають інфекційні хвороби, пов’язані із наданням медичної допомоги, на фінансові витрати підпорядкованого Вам ЗОЗ/ЗСЗ? |__| не впливають |__| впливають незначно |__| впливають суттєво |__| важко відповісти 10. Наскільки ефективна, на Вашу думку, гігієна рук для профілактики інфекційних хвороб, пов’язаних із наданням медичної допомоги? |__| не ефективна |__| впливає незначно |__| впливає суттєво |__| важко відповісти 11. Чи є пріоритетом гігієна рук під час Вашого перебування на керівній посаді? |__| не є пріоритетом |__| низька пріоритетність |__| середня пріоритетність |__| висока пріоритетність |__| важко відповісти 12. В якому відсотку випадків, що потребують виконання практики гігієни рук, в середньому, на Вашу думку, працівники підпорядкованого Вам ЗОЗ/ЗСЗ дійсно її виконують (враховується миття рук милом і водою та обробка антисептиком для рук)? |__| ______ % |__| важко відповісти |
||||||
13. Чи є лікарі та старші сестри медичні прикладами для наслідування щодо підтримки впровадження практик гігієни рук у підпорядкованому Вам ЗОЗ/ЗСЗ? |
||||||
взагалі не дотримуються |
|__| |
|__| |
|__| |
|__| |
|__| |
всі є прикладами для наслідування |
14. Чи всі пацієнти у підпорядкованому Вам ЗОЗ/ЗСЗ проінформовані щодо необхідності дотримання практик гігієни рук під час надання медичної допомоги? |__| так |__| ні |__| важко відповісти |
||||||
15. Як би Ви оцінили зусилля, що прикладаються Вашими підлеглими для дотримання практик гієни рук при наданні медичної допомоги? |
||||||
жодних зусиль |
|__| |
|__| |
|__| |
|__| |
|__| |
роблять все можливе |
16. Як працівники, у підпорядкованому Вам ЗОЗ/ЗСЗ, сприймають заклик щодо дотримання практик гігієни рук при наданні медичної допомоги? |
||||||
відсторонено |
|__| |
|__| |
|__| |
|__| |
|__| |
із розумінням |
17. Наскільки ефективними будуть, на Вашу думку, наступні заходи, які направлені на постійне покращення дотримання практик гігієни рук, у підпорядкованому Вам ЗОЗ/ЗСЗ (у кожному із пунктів зазначте лише одну відповідь)? 1) Керівництво ЗОЗ/ЗСЗ відкрито підтримує заходи з покращення гігієни рук: |
||||||
без будь-якого ефекту |
|__| |
|__| |
|__| |
|__| |
|__| |
надзвичайний ефект |
2) В ЗОЗ/ЗСЗ будуть встановлені диспенсери із антисептиком для рук в кожній точці догляду: |
||||||
без будь-якого ефекту |
|__| |
|__| |
|__| |
|__| |
|__| |
надзвичайний ефект |
3) Інформаційні плакати/стенди встановлені поряд із точками догляду з метою постійного нагадування: |
||||||
без будь-якого ефекту |
|__| |
|__| |
|__| |
|__| |
|__| |
надзвичайний ефект |
4) Кожен працівник проходить щорічне навчання із гігієни рук: |
||||||
без будь-якого ефекту |
|__| |
|__| |
|__| |
|__| |
|__| |
надзвичайний ефект |
5) В ЗОЗ/ЗСЗ розроблені, затверджені та розповсюджені серед всіх працівників прості та зрозумілі стандартні операційні процедури щодо практик гігієни рук: |
||||||
без будь-якого ефекту |
|__| |
|__| |
|__| |
|__| |
|__| |
надзвичайний ефект |
6) Працівники регулярно отримують зворотній зв’язок від координатора з гігієни рук щодо результатів впровадження: |
||||||
без будь-якого ефекту |
|__| |
|__| |
|__| |
|__| |
|__| |
надзвичайний ефект |
7) Лікарі та старші медичні сестри — приклади для наслідування в дотриманні практик гігієни рук: |
||||||
без будь-якого ефекту |
|__| |
|__| |
|__| |
|__| |
|__| |
надзвичайний ефект |
8) Пацієнтам запропоновано нагадувати працівникам щодо необхідності виконати практику гігієни рук: |
||||||
без будь-якого ефекту |
|__| |
|__| |
|__| |
|__| |
|__| |
надзвичайний ефект |
Дякуємо за Ваші відповіді!
Додаток 11
до Інструкції з впровадження покращення гігієни рук
в закладах охорони здоров’я та установах / закладах надання
соціальних послуг / соціального захисту населення
(пункт 6 розділу III, пункт 11 розділу V, підпункт 1
пункту 6 розділу VII, підпункт 7 пункту 10 розділу VII,
підпункт 8 пункту 13 розділу VII, підпункт 1 пункту 14
розділу VII, підпункт 4 пункту 17 розділу VII)
Протокол оцінки дотримання правил гігієни рук у ЗОЗ/ЗСЗ
I. Вступна частина
1. Цей Протокол використовується для оцінки дотримання правил гігієни рук у підрозділах ЗОЗ/ЗСЗ, де впроваджується покращення гігієни рук:
1) базової оцінки дотримання правил гігієни рук до початку реалізації заходів з покращення гігієни рук;
2) наступної оцінки (не пізніше ніж через один рік) для визначення оцінки впливу реалізації заходів з покращення гігієни рук;
3) оцінки після реалізації дій (не рідше одного разу на рік) для моніторингу стійкості покращення та винайдення областей, що потребують додаткового втручання.
Для отримання порівнюваних результатів оцінок слід використовувати однакові показники.
2. Оцінка відповідно до цього Протоколу проводиться шляхом збору даних щодо дотримання працівниками правил гігієни рук під час виконання ними рутинних процедур та дозволяє отримати найбільш об’єктивну інформацію. В кожному із оцінюваних підрозділів збираються дані щодо 150 — 200 випадків, коли потрібно проводити гігієну рук.
3. Цей Протокол включає такі форми для оцінки дотримання правил гігієни рук:
1) форма для запису результатів спостереження;
2) форма для розрахунку рівня дотримання правил гігієни рук за результатами спостереження;
3) форма для розрахунку відповідності показанням для гігієни рук за результатами спостереження.
Пояснення щодо заповнення зазначених форм наведені у інструкціях щодо їх заповнення.
4. Форми заповнюються спостерігачем/дослідником. Дані, що були визначені для спостереження і те, що було виявлено під час оцінювання, слід записувати олівцем, для того щоб одразу вносити корективи якщо в них виникла потреба. Під час проведення відкритих (працівників повідомлено щодо проведення оцінювання) і прямих (оцінювання проводиться безпосередньо під час проведення догляду) оцінок спостерігач/дослідник представляється працівнику, роз’яснює свою задачу і пропонує встановити безпосередній неформальний зворотній зв’язок.
II. Форма для запису результатів спостереження
Сторінка № ___ |
||
Заклад: _______________________________ |
Період №: _________________ |
Сеанс роботи №: ______________ |
Служба: _____________________________ |
Дата: ___/___/__ |
Спостерігач: _____________________ |
Відділення: ___________________________ |
Час початку сеансу: ________ |
Час завершення сеансу: _______ |
Палата: ______________________________ |
Тривалість сеансу (в хвилинах): _______ |
Проф. група |
Проф. група |
Проф. група |
Проф. група |
||||
Код |
Код |
Код |
Код |
||||
№ |
№ |
№ |
№ |
Випадок |
Показання |
Заходи по гр |
Випадок |
Показання |
Заходи по гр |
Випадок |
Показання |
Заходи по гр |
Випадок |
Показання |
Заходи по гр |
1 |
|_| дкп |
° АР |
1 |
|_| дкп |
° АР |
1 |
|_| дкп |
° АР |
1 |
|_| дкп |
° АР |
Випадок |
Показання |
Заходи по гр |
Випадок |
Показання |
Заходи по гр |
Випадок |
Показання |
Заходи по гр |
Випадок |
Показання |
Заходи по гр |
2 |
|_| дкп |
° АР |
2 |
|_| дкп |
° АР |
2 |
|_| дкп |
° АР |
2 |
|_| дкп |
° АР |
Випадок |
Показання |
Заходи по гр |
Випадок |
Показання |
Заходи по гр |
Випадок |
Показання |
Заходи по гр |
Випадок |
Показання |
Заходи по гр |
3 |
|_| дкп |
° АР |
3 |
|_| дкп |
° АР |
3 |
|_| дкп |
° АР |
3 |
|_| дкп |
° АР |
Випадок |
Показання |
Заходи по гр |
Випадок |
Показання |
Заходи по гр |
Випадок |
Показання |
Заходи по гр |
Випадок |
Показання |
Заходи по гр |
4 |
|_| дкп |
° АР |
4 |
|_| дкп |
° АР |
4 |
|_| дкп |
° АР |
4 |
|_| дкп |
° АР |
III. Інструкція щодо заповнення форми для запису результатів спостереження
1. Графи «Заклад», «Період», «Служба», «Дата», «Спостерігач», «Відділення», «Час початку сеансу» та «Палата» заповнюються до початку збору даних.
2. Сторінка № — зазначається лише в разі використання для одного сеансу більше однієї форми.
3. У графі «Заклад» зазначається назва закладу охорони здоров’я, закладу надання соціальних послуг або закладу соціально захисту.
4. У графі «Служба» зазначається назва відповідної служби, де проводиться спостереження — наприклад, терапевтична/внутрішні хвороби, хірургічна, інтенсивна терапія, змішана (надається різнопрофільна допомога в залежності від потреби), невідкладна допомога/приймальне відділення, акушерська, педіатрична, реабілітаційна, хоспісна тощо.
5. У графі «Відділення» зазначається назва відділення закладу, де проводиться спостереження.
6. У графі «Палата» зазначається номер або інший ідентифікатор палати, в якій проводиться спостереження.
7. У графі «Період» зазначається «1» — для базової оцінки, «2» — для оцінки, що проводиться через один місяць після впровадження заходів з гігієни рук, «3» — для наступних оцінок.
8. У графі «Тривалість сеансу» зазначається різниця між часом початку сеансу і його завершенням в хвилинах. Сеанс роботи має продовжуватися не більше 20 хвилин (±10 хвилин в залежності від діяльності, за якою ведеться спостереження). Час завершення і тривалість сеансу роботи зазначаються в кінці періоду спостереження.
9. У графі «Сеанс роботи N» зазначається порядковий номер сеансу, який визначається під час введення даних для аналізу. Кожне окреме заповнення форми для запису результатів спостереження дотримання правил гігієни рук є окремим сеансом. Заборонено відносити до одного сеансу результати спостережень, що розділені у часі (наприклад, не слід відносити до одного сеансу результати спостережень, що зібрані в одному відділенні у різні дні тижня або різні періоди доби). Також заборонено розділяти на окремі сеанси результати спостережень за різними групами працівників, якщо вони збиралися одночасно (наприклад, якщо результати отримані при спостереженні за сестрою медичною, лікарем-реаніматологом-анестезіологом, лікарем-гастроентерологом і прибиральницею, в один період часу в одному приміщенні, їх слід віднести до одного сеансу).
10. У графах «Професійна група» та «Код» зазначаються номери, які відповідають номеру професійної групи 1–4 та номеру посади працівника у таблиці, що наведена нижче. Класифікація за професійною групою для цілей цієї оцінки сформована відповідно до прогнозованої кількості проведених практик гігієни рук за робочу зміну.
У кожній колонці форми, під графами «Професійна група» можуть відмічатись випадки, показання і заходи з гігієни рук декількох працівників, посади яких відносяться до однієї професійної групи, за час одного сеансу роботи (наприклад, колонка перша відповідає професійній групі 1). Альтернативним варіантом заповнення може бути зазначення у одній колонці під графою «Професійна група» спостережень щодо випадків, показань і заходів з гігієни рук щодо одного працівника, тоді кожна колонка призначається лише для одного працівника і зазначається лише його професійна група та код (наприклад, перша — четверта колонки відповідають професійній групі 2).
Класифікація за професійною групою
Професійна група 1 |
Професійна |
Професійна |
Професійна група 4 |
1 |
2 |
3 |
4 |
Код 1.1 |
Код 2.1 |
Код 3.1 |
Код 4.1 |
Код 1.2 |
Код 3.2 |
Код 4.2 |
|
Код 1.3 |
Код 3.3 |
Код 4.3 |
|
Код 3.4 |
Код 4.4 |
||
Код 3.5 |
|||
Код 3.6 |
|||
Код 3.7 |
11. У графі «N» зазначається кількість працівників, які відносяться до однієї професійної групи (мають однаковий код) та потрапили у поле зору спостерігача/дослідника в моменти, що потребують виконання практики гігієни рук. Спостерігач/дослідник може вести спостереження не більше ніж за трьома працівниками одночасно, якщо гігієна рук проводиться часто.
12. Графа «Випадок» не заповнюється, означає ситуацію при якій є щонайменше одне показання для проведення практики гігієни рук. Відносно випадку заповнюються графи «Показання» та «Захід по гр». Кожен випадок для проведення гігієни рук вказується в одному рядку таблиці в кожному стовпчику; кожен рядок не пов’язаний із рядками в інших стовпчиках.
13. У графі «Показання» будь-якою позначкою (хрестик, галочка або «+») відмічаються показання для проведення гігієни рук (може бути відмічено декілька показань).
Скорочення, які застосовуються у графі «Показання»:
дкп — до контакту із пацієнтом;
дап — до асептичної процедури;
пбр — після ситуації, що пов’язана із ризиком контакту із біологічними рідинами;
пкп — після контакту із пацієнтом;
пзс — після контакту із об’єктами зовнішнього середовища, що перебувають у безпосередній близькості із пацієнтом.
14. У графі «Захід по гр» будь-якою позначкою (хрестик, галочка або «+») відмічається проведення заходу (АР, МР) працівником або не проведення заходу — навпроти «відсутні». Позначка навпроти «рукавички» проставляється, якщо захід із гігієни рук не виконано в той момент, коли на руках працівника були одягнені рукавички (наприклад, до наступного контакту із пацієнтом працівник не зняв рукавички та продовжив надавати медичну допомогу).
Скорочення, які застосовуються у графі «Захід по гр»:
гр — гігієна рук;
АР — гігієнічна обробка рук;
МР — миття рук з милом та водою.
IV. Форма для розрахунку рівня дотримання правил гігієни рук за результатами спостереження
|
|||||||||||||||||||
Професійна група: ___ |
Професійна група: ___ |
Професійна група: ___ |
Професійна група: ___ |
Всього за сеанс роботи: |
|||||||||||||||
Сеанс № |
Випадок (n) |
МР (n) |
АР (n) |
Випадок (n) |
МР (n) |
АР (n) |
Випадок (n) |
МР (n) |
АР (n) |
Випадок (n) |
МР (n) |
АР (n) |
Випадок (n) |
МР (n) |
АР (n) |
||||
1 |
|||||||||||||||||||
2 |
|||||||||||||||||||
3 |
|||||||||||||||||||
4 |
|||||||||||||||||||
5 |
|||||||||||||||||||
6 |
|||||||||||||||||||
7 |
|||||||||||||||||||
8 |
|||||||||||||||||||
9 |
|||||||||||||||||||
10 |
|||||||||||||||||||
11 |
|||||||||||||||||||
12 |
|||||||||||||||||||
13 |
|||||||||||||||||||
14 |
|||||||||||||||||||
15 |
|||||||||||||||||||
Всього |
|||||||||||||||||||
Розрахунок |
|||||||||||||||||||
Дотримання, % |
|||||||||||||||||||
V. Інструкція щодо заповнення форми для розрахунку рівня дотримання правил гігієни рук за результатами спостереження
1. Для заповнення форми використовуються дані форми для запису результатів спостереження.
2. Номер сеансу роботи, випадки (кількість) і дані заходів з гігієни рук щодо цих випадків під час відповідного сеансу роботи, вказуються в одному і тому ж рядку.
3. Розрахунок результатів по професійній групі та по сеансу роботи (по вертикалі):
1) сумувати заповнені у стовпчиках «Випадок» випадки дотримання правил гігієни рук, щодо яких було проведено спостереження, та записати суму у рядку «Всього» стовпчика «Випадок»;
2) сумувати проведені заходи з гігієни рук заповнені у стовпчиках «МР» (миття рук з милом) та «АР» (гігієнічної обробки рук) та записати суму у рядку «Всього» відповідних стовпчиків «МР» та «АР»;
3) сумувати дані щодо випадків та заходів з гігієни рук щодо кожного сеансу та записати у відповідних стовпчиках колонки «Всього за сеанс роботи»;
4) розрахувати відсоток дотримання правил гігієни рук за формулою:
заходи — це сума АР та МР, зазначених у відповідних стовпчиках рядка «Всього»;
випадки — це сума випадків, зазначена у рядку «Всього» у стовпчику «Випадок».
4. Результати розрахунку дотримання правил гігієни рук по колонці «Всього за сеанс роботи» дорівнюють середньому показнику дотримання гігієни рук по всіх професійних групах.
VI. Форма для розрахунку відповідності показанням для гігієни рук за результатами спостереження
|
|||||||||||||||||||
Перед контактом із пацієнтом, (n) |
До асептичної процедури, (n) |
Після ситуації, що пов’язана із ризиком контакту із біологічними рідинами, (n) |
Після контакту із пацієнтом, (n) |
Після контакту із об’єктами зовнішнього середовища, що перебувають у безпосередній близькості із пацієнтом, (n) |
|||||||||||||||
Сеанс № |
Випадки (n) |
МР (n) |
АР (n) |
Випадки (n) |
МР (n) |
АР (n) |
Випадки (n) |
МР (n) |
АР (n) |
Випадки (n) |
МР (n) |
АР (n) |
Випадки (n) |
МР (n) |
АР (n) |
||||
1 |
|||||||||||||||||||
2 |
|||||||||||||||||||
3 |
|||||||||||||||||||
4 |
|||||||||||||||||||
5 |
|||||||||||||||||||
6 |
|||||||||||||||||||
7 |
|||||||||||||||||||
8 |
|||||||||||||||||||
9 |
|||||||||||||||||||
10 |
|||||||||||||||||||
11 |
|||||||||||||||||||
12 |
|||||||||||||||||||
13 |
|||||||||||||||||||
14 |
|||||||||||||||||||
15 |
|||||||||||||||||||
Всього |
|||||||||||||||||||
Розрахунок |
|||||||||||||||||||
Відповідність показанням, % |
|||||||||||||||||||
VII. Інструкція щодо заповнення форми для розрахунку відповідності показанням для гігієни рук за результатами спостереження
1. Для заповнення форми використовуються дані форми для запису результатів спостереження.
2. Якщо декілька показань для гігієни рук виникають в рамках одного випадку, кожне із показань має розглядатися окремо, так само як і відповідний захід із дотримання гігієни рук.
3. Номер сеансу роботи і дані спостереження щодо випадків та заходів з гігієни рук під час відповідного сеансу роботи вказуються в одному і тому ж рядку.
4. Розрахунок результатів по показанням для гігієни рук (по вертикалі):
1) сумувати заповнену у стовпчиках «Випадки» кількість випадків виконання показання гігієни рук та записати суму у рядку «Всього» кожного стовпчика «Випадки»;
2) сумувати проведені заходи з гігієни рук заповнені у стовпчиках «МР» (миття рук з милом) та «АР» (гігієнічної обробки рук) та записати суму у рядку «Всього» відповідних стовпчиків «МР» та «АР»;
3) розрахувати відсоток відповідності показанням для гігієни рук за формулою:
заходи — це сума АР та МР, зазначених у відповідних стовпчиках рядка «Всього»;
випадки — це сума випадків, зазначена у рядку «Всього» у стовпчику «Випадки».
Додаток 12
до Інструкції з впровадження покращення гігієни рук
в закладах охорони здоров’я та установах / закладах надання
соціальних послуг / соціального захисту населення
(пункт 6 розділу III, пункт 2 розділу V, пункт 11 розділу V)
Протокол системної самооцінки гігієни рук в ЗОЗ/ЗСЗ
I. Вступна частина
1. Системна самооцінка гігієни рук в ЗОЗ/ЗСЗ проводиться відповідно до цього Протоколу з метою оцінки реалізації в ЗОЗ/ЗСЗ ММС з покращення гігієни рук.
2. Цей Протокол включає:
1) опитувальник щодо реалізації основних компонентів ММС відповідно до розділів «Зміни в системі», «Навчання і підготовка», «Моніторинг, аудит і зворотній зв'язок», «Нагадування на робочому місці», «Культура дотримання гігієни рук»;
2) таблицю результатів оцінки;
3) таблицю інтерпретації результатів оцінки — визначення рівня гігієни рук у ЗОЗ/ЗСЗ.
3. Оцінка здійснюється по кожному з питань у відповідному розділі та у підсумку по кожному з розділів по кількості балів, зазначених у колонці «Оцінка (балів)». Загальна сума балів по всіх розділах порівнюється із значеннями загальної суми балів для визначення рівня гігієни рук. Визначений рівень гігієни рук використовується для проведення відповідних заходів для покращення гігієни рук в ЗОЗ/ЗСЗ.
II. Опитувальник щодо реалізації основних компонентів ММС
Зміни в системі |
|||
№ |
Питання |
Відповідь (виберіть лише одну відповідь) |
Оцінка (балів) |
1 |
2 |
3 |
4 |
1. |
Наскільки легко у ЗОЗ/ЗСЗ знайти антисептик для рук? |
Не використовується |
0 |
Доступний(і), але його/їх ефективність (відповідність державним стандартам України) і переносимість не були визначені |
0 |
||
Доступний(і), але лише в деяких структурних підрозділах та/або наявний не завжди |
5 |
||
Завжди доступний(і) у всіх структурних підрозділах, визначені його/їх ефективність і переносимість |
10 |
||
Завжди доступний(і) у всіх структурних підрозділах і у більшості точок догляду, визначені його/їх ефективність і переносимість |
30 |
||
Завжди доступний(і) у всіх структурних підрозділах і всіх точках догляду, визначені його/їх ефективність і переносимість |
50 |
||
2. |
Співвідношення раковина/ліжко становить |
Менше ніж 1:10 |
0 |
і 1:10 у більшості структурних підрозділів |
5 |
||
і 1:10 у всіх структурних підрозділах та (тільки для ЗОЗ) 1:1 в ізоляторах і у ВАРІТ |
10 |
||
3. |
Чи наявна постійно чиста і безпечна вода (централізоване водопостачання)? |
Ні |
0 |
Так |
10 |
||
4. |
Чи наявне мило біля кожної раковини? |
Ні |
0 |
Так |
10 |
||
5. |
Чи наявні одноразові паперові рушники біля кожної раковини? |
Ні |
0 |
Так |
10 |
||
6. |
Чи наявні кошти виділені виключно на закупівлю витратних засобів для гігієни рук? |
Ні |
0 |
Так |
10 |
||
7. |
Додаткове запитання. Відповідати слід лише в тому випадку, якщо за перші шість запитань сума балів становить менше 100! |
Ні |
0 |
Так |
5 |
||
Сума балів оцінки по розділу «Зміни в системі» |
|||
Навчання і підготовка |
|||
№ |
Питання |
Відповідь (виберіть лише одну відповідь) |
Оцінка (балів) |
1. |
Як часто працівники проходять навчання з гігієни рук? |
Ніколи |
0 |
Одноразово (наприклад, при влаштуванні на роботу) |
5 |
||
Регулярне навчання для всіх працівників щонайменше один раз на рік |
10 |
||
Обов’язкове навчання перед влаштуванням на роботу та наступне регулярне щонайменше один раз на рік |
20 |
||
2. |
Чи проводиться перевірка знань після кожного курсу навчання? |
Ні |
0 |
Так |
20 |
||
3. |
Чи наявні у вільному доступі у ЗОЗ/ЗСЗ наступні документи? |
||
3.1 Правила і практики гігієни рук відповідно до Інструкції впровадження покращення гігієни рук в ЗОЗ та ЗСЗ |
Ні |
0 |
|
Так |
15 |
||
3.2 Гігієни рук: довідкове керівництво ВООЗ |
Ні |
0 |
|
Так |
5 |
||
4. |
Чи наявний у ЗОЗ/ЗСЗ спеціаліст (із відповідним сертифікатом або його еквівалентом), що проводить навчання з гігієни рук? |
Ні |
0 |
Так |
15 |
||
5 |
Чи наявні у ЗОЗ/ЗСЗ спостерігачі з гігієни рук? |
Ні |
0 |
Так |
15 |
||
6 |
Чи наявні виділені кошти на проведення навчання у ЗОЗ/ЗСЗ? |
Ні |
0 |
Так |
10 |
||
Сума балів оцінки по розділу «Навчання і підготовка» |
|||
Моніторинг, оцінка і зворотній зв’язок |
|||
№ |
Питання |
Відповідь |
Оцінка (балів) |
1 |
Чи проводяться регулярні оцінки (щонайменше щорічно) наявних інфраструктури і ресурсів для гігієни рук? |
Ні |
0 |
Так |
10 |
||
2 |
Чи проводиться після кожного навчання перевірка знань працівників щодо |
||
2.1. Показань до практики гігієни рук |
Ні |
0 |
|
Так |
5 |
||
2.2. Техніки проведення гігієни рук |
Ні |
0 |
|
Так |
5 |
||
3 |
Чи здійснюється регулярний моніторинг кількості використаних засобів для гігієни рук (щонайменше один раз на 3 місяці)? |
Ні |
0 |
Так |
5 |
||
4 |
Чи здійснюється регулярний моніторинг кількості використаного мила (щонайменше один раз на 3 місяці)? |
Ні |
0 |
Так |
5 |
||
5 |
Кількість використаного антисептику для рук становить щонайменше 20 літрів на 1000 ліжкоднів? |
Ні (або не визначається) |
0 |
Так |
5 |
||
6 |
Прямий моніторинг за дотриманням гігієни рук (заповнюється, якщо спостерігач пройшов відповідне навчання) |
||
6.1. Як часто проводиться оцінювання у ЗОЗ/ЗСЗ відповідно до Протоколу оцінки дотримання правил гігієни рук? |
Не проводиться |
0 |
|
Нерегулярно |
5 |
||
Щорічно |
10 |
||
Кожні 3 місяці або частіше |
15 |
||
6.2. Який загальний рівень дотримання правил гігієни рук у ЗОЗ/ЗСЗ? |
< 30% |
0 |
|
31–40% |
5 |
||
41–50% |
10 |
||
51–60% |
15 |
||
61–70% |
20 |
||
71–80% |
25 |
||
> 81% |
30 |
||
7 |
Чи забезпечується зворотній зв’язок з працівниками після кожної навчальної сесії? |
Ні |
0 |
Так |
5 |
||
8 |
Чи забезпечується системний зворотній зв’язок (щонайменше один раз на півроку) із врахуванням даних оцінювання щодо гігієни рук (споживання, дотримання правил, оцінка знань тощо)? |
||
8.1 Для працівників |
Ні |
0 |
|
Так |
7,5 |
||
8.2 Для адміністрації ЗОЗ/ЗСЗ |
Ні |
0 |
|
Так |
7,5 |
||
Сума балів оцінки по розділу «Моніторинг, оцінка і зворотній зв’язок» |
|||
Нагадування на робочому місці |
|||
№ |
Питання |
Відповідь (виберіть лише одну відповідь) |
Оцінка (балів) |
1 |
Чи наявні у ЗОЗ/ЗСЗ наступні нагадування на робочому місці? |
||
1.1. Показання для проведення практики гігієни рук |
Відсутні |
0 |
|
Наявні в деяких структурних підрозділах |
15 |
||
Наявні в більшості структурних підрозділах |
20 |
||
Наявні у всіх структурних підрозділах |
25 |
||
1.2. Пояснення щодо правильного використання диспенсерів |
Відсутні |
0 |
|
Наявні в деяких структурних підрозділах |
5 |
||
Наявні в більшості структурних підрозділах |
10 |
||
Наявні у всіх структурних підрозділах |
15 |
||
1.3. Техніка проведення обробки рук |
Відсутні |
0 |
|
Наявні в деяких структурних підрозділах |
5 |
||
Наявні в більшості структурних підрозділах |
7,5 |
||
Наявні у всіх структурних підрозділах |
10 |
||
2 |
Як часто проходить систематична перевірка наявності пошкоджених нагадувань та їх заміна в разі необхідності? |
Не проводиться |
0 |
Щорічно |
10 |
||
Кожні 2–3 місяці |
15 |
||
3 |
Чи проводиться виготовлення і розміщення власних (відмінних від вищенаведених) нагадувань з метою популяризації гігієни рук у ЗОЗ/ЗСЗ? |
Ні |
0 |
Так |
10 |
||
4 |
Чи наявні будь-які нагадування щодо гігієни рук у палатах/кімнатах? |
Ні |
0 |
Так |
10 |
||
5 |
Чи наявні інші нагадування на робочому місці у ЗОЗ/ЗСЗ (наліпки, значки, стенди тощо)? |
Ні |
0 |
Так |
15 |
||
Сума балів оцінки по розділу «Нагадування на робочому місці» |
|||
Культура дотримання гігієни рук |
|||
№ |
Питання |
Відповідь |
Оцінка (балів) |
1 |
Команда (щонайменше — координатор з гігієни рук, інструктор та спостерігач, спеціаліст зі збору та аналізу даних), яка займається реалізацією заходів з покращення гігієни рук у ЗОЗ/ЗСЗ: |
||
1.1 Створена |
Ні |
0 |
|
Так |
5 |
||
1.2 Зустрічається регулярно (щонайменше один раз на місяць) |
Ні |
0 |
|
Так |
5 |
||
1.3 У команди наявний виділений час для активної популяризації гігієни рук (наприклад, затверджений керівником ЗОЗ/ЗСЗ план із виділеним часом) |
Ні |
0 |
|
Так |
5 |
||
2 |
Чи мають наступні представники адміністрації ЗОЗ/ЗСЗ зобов’язання (оформлене в письмовій формі) підтримувати впровадження покращення гігієни рук? |
||
2.1 Керівник ЗОЗ/ЗСЗ |
Ні |
0 |
|
Так |
10 |
||
2.2 Медичний директор/заступник керівника ЗОЗ/ЗСЗ |
Ні |
0 |
|
Так |
5 |
||
2.3 Головна сестра медична/керівник ЗСЗ |
Ні |
0 |
|
Так |
5 |
||
3 |
Чи затверджений довгостроковий план покращення гігієни рук у ЗОЗ/ЗСЗ (щонайменше п’ятирічний)? |
Ні |
0 |
Так |
10 |
||
4 |
Чи існує у ЗОЗ/ЗСЗ система винайдення чемпіонів та потенційних координаторів з гігієни рук? |
||
Система винайдення чемпіонів (працівник, що цілковито виступає за дотримання стандартів безпеки, в тому числі гігієни рук, і популяризує їх у своєму структурному підрозділі і ЗОЗ/ЗСЗ в цілому) |
Ні |
0 |
|
Так |
5 |
||
Система винайдення потенційних координаторів з гігієни рук (працівник, який служить прикладом для наслідування (відсоток дотримання правил гігієни рук більше 80 %), здатен переконувати працівників у необхідності дотримання практик і правил гігієни рук та має хист до викладацької діяльності) |
Ні |
0 |
|
Так |
5 |
||
5 |
Участь пацієнтів у заходах з покращення гігієни рук |
||
5.1 Пацієнти інформовані щодо необхідності дотримання правил і практик гігієни рук (наприклад, видаються листівки) |
Ні |
0 |
|
Так |
5 |
||
5.2 Реалізовується програма залучення пацієнтів до покращення гігієни рук (наприклад, проводиться навчання щодо показань та техніки проведення гігієни рук) |
Ні |
0 |
|
Так |
10 |
||
6 |
Чи використовуються у ЗОЗ/ЗСЗ заходи щодо підтримки постійного покращення гігієни рук, такі як: |
||
6.1 Онлайн або дистанційне навчання |
Ні |
0 |
|
Так |
5 |
||
6.2 Цілі та задачі для покращення гігієни рук встановлюються щорічно |
Ні |
0 |
|
Так |
5 |
||
6.3 Обмін між ЗОЗ/ЗСЗ досвідом із впровадження інноваційних заходів/рішень |
Ні |
0 |
|
Так |
5 |
||
6.4 Проведення масових заходів із висвітленням необхідності подальшої підтримки покращення гігієни рук та/або випуск внутрішнього інформаційного бюлетеня |
Ні |
0 |
|
Так |
5 |
||
6.5 Система персональної відповідальності (наприклад, відмінні показники в дотриманні практик гігієни рук заохочуються премією або при виборі працівника для підвищення враховується вищезгадані показники) |
Ні |
0 |
|
Так |
5 |
||
6.6 Система наставництва (кожному новому працівнику виділяється наставник, що бере на себе відповідальність за ознайомлення його(її) із заходами з гігієни рук в ЗОЗ/ЗСЗ) |
Ні |
0 |
|
Так |
5 |
||
Сума балів оцінки по розділу «Культура дотримання гігієни рук» |
|||
III. Таблиця результатів оцінки
№ |
Розділ |
Оцінка (балів) |
1 |
Зміни в системі |
|
2 |
Навчання і підготовка |
|
3 |
Моніторинг, аудит і зворотній зв’язок |
|
4 |
Нагадування на робочому місці |
|
5 |
Культура дотримання гігієни рук |
|
Загальна сума балів оцінки |
||
IV. Таблиця інтерпретації результатів оцінки
Загальна сума балів оцінки |
Рівень гігієни рук |
0–125 |
Незадовільний |
126–250 |
Базовий |
251–375 |
Середній |
376–500 |
Достатній |
Додаток 13
до Інструкції з впровадження покращення гігієни рук в закладах охорони здоров’я та установах / закладах надання соціальних послуг / соціального захисту населення
(пункт 1 розділу VII)
Мінімальні критерії, що необхідні для реалізації мультимодальної стратегії з покращення гігієни рук у ЗОЗ/ЗСЗ
Компонент ММС |
Мінімальні критерії для реалізації |
Зміни в системі |
1. Диспенсери розташовані в точках догляду в кожному підрозділі або видані працівникам (кишенькові диспенсери). |
Навчання і підготовка |
Всі працівники підрозділів отримують курс навчання з гігієни рук. Навчальна програма оновлюється відповідно до нових науково обґрунтованих даних. |
Нагадування на робочому місці |
Інформаційні плакати щодо показань та практик проведення гігієни рук розміщені у відповідних зонах ЗОЗ/ЗСЗ (наприклад, процедурному кабінеті, кімнаті відпочинку для працівників, вестибюлі тощо). |
Моніторинг, оцінка і зворотній зв’язок |
Проводяться базова та подальші оцінки із використанням щонайменше протоколів оцінки наявної інфраструктури і ресурсів, оцінки дотримання правил гігієни рук та оцінки використання засобів для гігієни рук (додатки 4, 6, 11 до цієї Інструкції). |
Культура дотримання гігієни рук |
Керівництво ЗОЗ/ЗСЗ всебічно підтримує заходи з гігієни рук в довгостроковій перспективі (в бюджеті щорічно передбачаються кошти на план дій з покращення гігієни рук, проведені оцінювання керівництва з гігієни рук вказують на зростання обізнаності та прихильності, на постійній основі здійснюється заохочення працівників або підрозділів тощо). |
Додаток 14
до Інструкції з впровадження покращення гігієни рук
в закладах охорони здоров’я та установах / закладах надання
соціальних послуг / соціального захисту населення
(підпункт 2 пункту 2 розділу VII)
Примірний план дій ЗОЗ/ЗСЗ з покращення гігієни рук
Дія/захід |
Відповідальна особа |
Період впровадження (початок і закінчення) |
Бюджет (грн.) |
Індикатор виконання |
Досягнений результат (із коротким описом та датою завершення) |
1 |
2 |
3 |
4 |
5 |
6 |
Підготовчий етап |
|||||
Визначити координатора з гігієни рук |
Керівник ЗСЗ/ВІК |
Визначено координатора з гігієни рук. |
|||
Визначити помічників координатора з гігієни рук (при необхідності) |
Координатор з гігієни рук |
Визначені помічники координатора з гігієни рук. |
|||
Дослідити будь-які попередні ініціативи з впровадження покращення гігієни рук |
Координатор з гігієни рук |
1 місяць |
Проведено аналіз попередніх ініціатив з впровадження покращення гігієни рук, оформлено звіт довільної форми. |
||
Погодити масштаби та обсяг дій |
Керівництво ЗОЗ/ЗСЗ, керівник ВІК, координатор з гігієни рук |
1 місяць |
Проведена зустріч, на якій погоджено наступні кроки впровадження гігієни рук. |
||
Провести оцінку робочого навантаження персоналу з урахуванням необхідності виконання гігієни рук. |
Координатор з гігієни рук, відділ кадрів |
1 місяць |
Терапевтичні і хірургічні відділення укомплектовані сестрами медичними на зміну із розрахунку одна медична сестра на 20 ліжок, відділення інтенсивної терапії — одна сестра медична на два ліжка. |
||
При наявності в ЗОЗ/ЗСЗ затверджених клінічних протоколів, СОП, табелів матеріально-технічного оснащення включити в них практику гігієни рук |
Медичний директор або заступник керівника ЗСЗ, керівник ВІК, координатор з гігієни рук |
1–3 місяці |
Переглянуті і відкориговані наявні протоколи, СОП, табелі матеріально-технічного оснащення. |
||
Зміни в системі |
|||||
Вивчити дані щодо дотримання практики гігієни рук |
Координатор з гігієни рук |
1 місяць |
Проведено оцінку дотримання правил гігієни рук. Звіт надано для ознайомлення зацікавленим сторонам. |
||
Проаналізувати ЗОЗ/ЗСЗ з огляду на можливість впровадження покращення гігієни рук |
Керівник ВІК, координатор з гігієни рук |
1 місяць |
Визначені ризики неефективного впровадження та механізми їх нівелювання. |
||
Провести оцінку інфраструктури і ресурсів |
Координатор з гігієни рук і його помічники |
1–3 місяці |
Проведено оцінку інфраструктури і ресурсів. Звіт надано для ознайомлення зацікавленим сторонам. |
||
Провести оцінку використання засобів для гігієни рук |
Координатор з гігієни рук і його помічники |
1–3 місяці |
Проведено оцінку використання засобів для гігієни рук. Звіт надано для ознайомлення зацікавленим сторонам. |
||
Обговорити та затвердити заходи з покращення інфраструктури |
Керівництво ЗОЗ/ЗСЗ, керівник ВІК, координатор з гігієни рук |
За результатами оцінки |
Проведено зустріч, за результатами якої затверджено річний План дій щодо впровадження гігієни рук в ЗОЗ/ЗСЗ. |
||
Організувати закупівлю антисептиків для рук: |
Керівництво ЗОЗ/ЗСЗ, керівник фінансового підрозділу ЗОЗ/ЗСЗ, головна медична сестра ЗОЗ, фармацевт, керівник ВІК, координатор з гігієни рук |
1–3 місяці |
Визначена кількість диспенсерів, яку заплановано закупити, виділено фінансування, укладено договір на постачання. |
||
Провести оцінку дотримання правил та сприйняття гігієни рук серед працівників, використовуючи відповідні Протоколи |
Координатор з гігієни рук і його помічники |
1–3 місяці |
Проведено оцінку дотримання правил гігієни рук працівниками. Звіт надано для ознайомлення зацікавленим сторонам. |
||
Скласти та затвердити фінансовий план витрат для вирішення задач забезпечення проточною водою, раковинами і одноразовими паперовими рушниками |
Координатор з гігієни рук, заступник керівника ЗОЗ/ЗСЗ з технічних питань, керівник фінансового підрозділу ЗОЗ/ЗСЗ |
1 місяць |
Затверджено мінімум річний план із виділеним фінансуванням для усунення проблем з централізованим водопостачанням, встановленням раковин та забезпечення підрозділів одноразовими паперовими рушниками. |
||
Навчання і підготовка |
|||||
Встановити вимоги до обсягів навчання і підготовки працівників з урахуванням їх функціональних обов’язків |
Керівництво ЗОЗ/ЗСЗ, керівник ВІК, координатор з гігієни рук |
1 місяць |
Визначені навчальні групи відповідно до функціональних обов’язків (наприклад, хірурги, операційні сестри медичні, сестри медичні постові, водії, прибиральниці). |
||
Розробити, адаптувати або переглянути вже існуючий тренінг |
Координатор з гігієни рук |
1–3 місяці |
Підготовані матеріали для проведення тренінгів. |
||
Визначити працівників, що плануються на роль тренерів (щонайменше одного на підрозділ) |
Керівник ВІК, координатор з гігієни рук, відділ кадрів |
1 місяць |
Визначені тренери в підрозділах ЗОЗ/ЗСЗ. Відповідні зміни внесені в посадові обов’язки. |
||
Визначити працівників, що плануються на роль спостерігачів (щонайменше одного на ЗОЗ) |
Керівник ВІК/координатор з гігієни рук, відділ кадрів |
1 місяць |
Визначені спостерігачі. Відповідні зміни внесені в посадові обов’язки. |
||
Провести навчання тренерів |
ВІК/координатор з гігієни рук або заклад освіти, відділ кадрів |
1–3 місяці |
Проведено навчання тренерів. Звіт щодо проведеного навчання надано для ознайомлення зацікавленим сторонам. |
||
Провести навчання спостерігачів (тренери і спостерігачі можуть пройти однакову базову підготовку, але спостерігачі мають пройти спеціалізований курс) |
ВІК або заклад освіти, відділ кадрів |
1–3 місяці |
Проведено базове навчання спостерігачів. Звіт щодо проведеного навчання надано для ознайомлення зацікавленим сторонам. |
||
Розробити і затвердити план навчання і підготовки, із обов’язковим зазначенням графіку проведення оцінювання працівників |
Координатор з гігієни рук і його команда |
1 місяць |
Керівником ЗОЗ/ЗСЗ затверджено план навчання і підготовки працівників. |
||
Розробити і затвердити графік проведення навчання працівників |
Координатор з гігієни рук і його команда |
1 місяць |
Керівником ЗОЗ/ЗСЗ затверджено графік навчання працівників. |
||
Розробити і затвердити систему звітності щодо проведених тренінгів, включаючи план дій щодо працівників, які відсутні з різних причин |
Керівник ВІК/координатор з гігієни рук та інструктори |
1 місяць |
Керівником ЗОЗ/ЗСЗ затверджено форму звіту щодо проведених тренінгів. |
||
Витрати на програму навчання і підготовки затвердити у річному бюджеті |
Керівник ЗОЗ/ЗСЗ, керівник ВІК, координатор з гігієни рук |
1 місяць |
Керівником ЗОЗ/ЗСЗ затверджено бюджет програми навчання і підготовки з гігієни рук. |
||
Розробити та впровадити систему оновлення програм навчання і підготовки з гігієни рук. |
ВІК/координатор з гігієни рук, відділ кадрів |
1–3 місяці |
В посадових обов’язках координатора з гігієни рук окремим пунктом визначено щорічне оновлення програм навчання і підготовки з гігієни рук з урахуванням новітніх даних. |
||
Розробити та впровадити систему щорічної перевірки компетентності інструкторів |
Керівник ВІК, координатор з гігієни рук |
1–3 місяці |
Керівником ЗОЗ/ЗСЗ затверджено алгоритм щорічної перевірки компетентності інструкторів, що включає перевірку теоретичних знань і практичних навичок. |
||
Запланувати виготовлення додаткових навчальних матеріалів у довгостроковій перспективі (наприклад, матеріали для дистанційного навчання, створити групу в соціальних мережах) |
ВІК/координатор з гігієни рук, лідери думки, чемпіони |
постійно |
Створено групу в соціальній мережі для обміну досвідом та кращими практиками з гігієни рук. |
||
Нагадування на робочому місці |
|||||
Оцінка наявних ресурсів, включаючи наявні нагадування і досвід в їх розробці |
Координатор з гігієни рук |
1 місяць |
Проведено оцінку наявних нагадувань на робочих місцях (розміщення, якість друку, актуальність, стан тощо). Звіт направлено для ознайомлення зацікавленим сторонам. |
||
Встановити перелік та формат нагадувань на робочих місцях |
Координатор з гігієни рук, лідери думки, чемпіони |
1 місяць |
Визначені та затверджені типові нагадування на робочому місці. |
||
Визначити необхідні фінансові ресурси та їх джерела |
Координатор з гігієни рук, фінансовий відділ ЗОЗ/ЗСЗ |
1 місяць |
Визначена кількість нагадувань на робочому місці, яку заплановано закупити, виділено фінансування, заключено договір на друк. |
||
Оформити у вигляді інформаційних стендів, плакатів, бюлетенів рисунки що наведені в додатку 1 до цієї Інструкції |
Координатор з гігієни рук і його помічники |
1–3 місяці |
Визначена кількість нагадувань на робочому місці, яку заплановано закупити, виділено фінансування, заключено договір на друк. |
||
Розповсюдити інформаційні листівки або надати посилання для отримання інформації під час проходження навчання і підготовки |
ВІК/координатор з гігієни рук, інструктори |
постійно |
Працівникам надано доступ до нагадувань на робочому місці, які використовуються в ЗОЗ/ЗСЗ. |
||
Запланувати випуск додаткових інформаційних матеріалів, окрім листівок і плакатів |
ВІК/координатор з гігієни рук |
6–12 місяців |
Зацікавлені сторони сформували ініціативну групу, яка займається розробкою нових нагадувань на робочому місці. |
||
Моніторинг, оцінка і зворотній зв’язок |
|||||
Підготувати проведення моніторингу і оцінки: |
Керівник ВІК, координатор з гігієни рук, спостерігачі, фінансовий відділ |
1 місяць |
Розроблено/оновлено та затверджено керівником ЗОЗ/ЗСЗ протокол оцінки знань працівників. |
||
Розробити та затвердити графік проведення моніторингу, оцінки і зворотного зв’язку |
Керівник ВІК, координатор з гігієни рук |
1 місяць |
Керівником ЗОЗ/ЗСЗ затверджено графік проведення моніторингу, оцінки і зворотного зв’язку. |
||
Залучити необхідних спеціалістів (наприклад, медичного статистика, епідеміолога, адміністратора баз даних) |
Керівник ВІК, координатор з гігієни рук, фінансовий відділ, відділ кадрів |
1 місяць |
Визначено потребу в додатковому залученні фахівців. |
||
Витрати на моніторинг, оцінку і зворотній зв’язок затвердити у річному бюджеті |
Керівник ЗОЗ/ЗСЗ, фінансовий відділ, керівник ВІК, координатор з гігієни рук |
Керівником ЗОЗ/ЗСЗ затверджено витрати на моніторинг, оцінку і зворотній зв’язок у річному бюджеті. |
|||
Створити систему звітності по результатам оцінки, включаючи план дій по вирішенню проблем невідповідності |
Керівник ВІК, координатор з гігієни рук, спостерігачі |
1–3 місяці |
Керівником ЗОЗ/ЗСЗ затверджено типовий звіт за результатами проведеної оцінки. |
||
Визначити спостерігачів (якщо це ще не зроблено на попередніх етапах) |
Керівник ВІК, координатор з гігієни рук |
1 місяць |
Визначені спостерігачі. Відповідні зміни внесені в посадові обов’язки. |
||
Розробити та впровадити систему щорічного навчання спостерігачів |
Керівник ВІК/координатор з гігієни рук, освітній заклад |
1 місяць |
Керівником ЗОЗ/ЗСЗ затверджено програму навчання спостерігачів. |
||
Розробити та впровадити систему щорічної перевірки компетентності спостерігачів |
Координатор з гігієни рук |
1 місяць |
Керівником ЗОЗ/ЗСЗ затверджено алгоритм щорічної перевірки компетентності спостерігачів, що включає перевірку теоретичних знань і практичних навичок. |
||
Провести базову оцінку і отримати зворотній зв’язок із працівниками |
Координатор з гігієни рук, спостерігачі |
1 — 3 місяці |
Проведено базову оцінку наявної інфраструктури і ресурсів, сприйняття керівництвом ЗОЗ/ЗСЗ і працівниками гігієни рук, дотримання правил гігієни рук працівниками, використання засобів для гігієни рук, переносимості і прийнятності антисептику для рук. Звіти направлено для ознайомлення зацікавленим сторонам. |
||
Підготувати та розповсюдити графік поточного моніторингу (не рідше ніж один раз на місяць в кожному клінічному підрозділі і не рідше ніж раз на рік в підрозділах, які не проводять догляд за пацієнтами) |
Координатор з гігієни рук, спостерігачі |
1 місяць |
Керівником ЗОЗ/ЗСЗ затверджено графік поточного моніторингу і оцінки. |
||
Представляти звіти щодо проведених оцінювань та поквартальної динаміки результатів |
Координатор з гігієни рук |
щоквартально |
Звіти проведених моніторингу і оцінки містять інформацію щодо поквартальної динаміки результатів. |
||
Встановити цілі на рік із врахуванням поточних результатів |
Медичний директор/заступник керівника ЗОЗ/ЗСЗ, керівник ВІК, координатор з гігієни рук |
щорічно |
Цілі та індикатори їх виконання в річному Плані дій з впровадження гігієни рук визначені та переглядалися в залежності від отриманих результатів моніторингу і оцінки. |
||
Оцінити дані щодо розповсюдженості ІПНМД |
ВІК, епідеміолог ВІК |
щомісяця або щоквартально |
Визначений фоновий рівень розповсюдженості ІПНМД в ЗОЗ. |
||
Створити систему оцінювання розповсюдженості ІПНМД відповідно до показників дотримання практики гігієни рук |
ВІК, координатор з гігієни рук, епідеміолог ВІК |
щомісяця або щоквартально |
Створено інструмент для проведення оцінки. |
||
Провести оцінку економічної ефективності заходів з гігієни рук |
ВІК, фінансовий відділ |
щоквартально або щорічно |
Проведено оцінку економічної ефективності впровадження гігієни рук в ЗОЗ/ЗСЗ. Звіт надано для ознайомлення зацікавленим сторонам. |
||
Розглянути можливість представлення даних на тематичних конференціях, семінарах або з’їздах |
Керівник ЗОЗ/ЗСЗ, керівник ВІК, координатор з гігієни рук |
Результати щодо впровадження гігієни рук в ЗОЗ/ЗСЗ представлені на тематичному семінарі. |
|||
Культура дотримання гігієни рук |
|||||
Визначити чи потрібні будь-які покращення програми (на етапах навчання і підготовки, нагадувань на робочих місцях, моніторингу, оцінки і зворотного зв’язку) |
Керівник ВІК, координатор з гігієни рук |
постійно |
Проведено оцінку впроваджуваних заходів зовнішніми аудиторами, за результатами якої були внесені зміни в План дій. |
||
Підготувати економічне обґрунтування необхідності покращення гігієни рук і представити керівництву ЗОЗ |
Керівництво ЗОЗ/ЗСЗ, керівник ВІК, координатор з гігієни рук |
в разі потреби або вимоги |
Підготовано звіт за результатами п’яти років впровадження гігієни рук. Звіт надано для ознайомлення керівництву ЗОЗ/ЗСЗ. |
||
Проводити регулярні зустрічі із зацікавленими сторонами із метою реалізації зворотного зв’язку |
ВІК/координатор з гігієни рук |
щомісячно або щоквартально |
Затверджено графік проведення зустрічей із зацікавленими сторонами. Графік доведений до відома. |
||
Залучити громадські об’єднання до заходів з покращення гігієни рук |
Керівництво ЗОЗ/ЗСЗ, керівник ВІК/координатор з гігієни рук |
постійно |
Керівництвом ЗОЗ/ЗСЗ підписано меморандум про співпрацю з громадським об’єднанням. |
||
Розглянути можливість зовнішнього або перехресного оцінювання із залученням громадських об’єднань |
Керівництво ЗОЗ/ЗСЗ, керівник ВІК/координатор з гігієни рук |
постійно |
Проведено оцінку впроваджуваних заходів представниками громадського об’єднання, за результатами якої були внесені зміни в План дій. |
||
Проводити навчання пацієнтів правилам гігієни рук |
Керівник ЗОЗ/ЗСЗ, фінансовий відділ, координатор з гігієни рук, інструктори |
постійно |
Керівником ЗОЗ/ЗСЗ затверджені інформаційні матеріали для розміщення в палатах пацієнтів. |
||
Запровадити систему заохочень для працівників |
Керівництво ЗОЗ/ЗСЗ, фінансовий відділ, керівник ВІК/координатор з гігієни рук |
постійно |
Затверджено фонд преміювання кращих працівників. |
||
Включити оцінювання гігієни рук до інструментів визначення якості надання медичної допомоги |
Керівник ЗОЗ, відділ оцінки якості медичної допомоги, ВІК/координатор з гігієни рук |
Керівником ЗОЗ/ЗСЗ затверджено контрольні листи оцінки якості надання медичної допомоги, які включають гігієну рук. |
|||
Примітки:
1. даний примірний план включає всі основні компоненти ММС, однак не враховує місцевого контексту ЗОЗ/ЗСЗ. Тому, при розробці плану дій (для ЗОЗ може бути частиною плану дій з ПІІК), координатор з гігієни рук в ЗОЗ/ЗСЗ має визначити саме ті елементи, що відносяться до відповідного ЗОЗ/ЗСЗ та змінити заходи в залежності від місцевих потреб;
2. примірний план дій не містить хронологію подій, що мають бути реалізовані у ЗОЗ/ЗСЗ для досягнення позитивного результату, та містить лише огляд усіх можливо необхідних дій для забезпечення виконання кожного окремо взятого компоненту.
ЗАТВЕРДЖЕНО
Наказ Міністерства охорони здоров’я України
03 серпня 2021 року № 1614
Зареєстровано
в Міністерстві юстиції України
11 жовтня 2021 р. за № 1322/36944
Інструкція з впровадження адміністрування антимікробних препаратів в закладах охорони здоров’я, які надають медичну допомогу в стаціонарних умовах
I. Загальні положення
1. Ця Інструкція визначає організаційні засади призначення і використання антимікробних препаратів (далі — АМП) з метою запобігання появі і поширенню мікроорганізмів із антимікробною резистентністю (далі — АМР).
2. Ця Інструкція є обов’язковою для закладів охорони здоров’я, які надають стаціонарну медичну допомогу (далі — ЗОЗ), усіх форм власності та незалежно від їх відомчого підпорядкування.
3. Відповідальними за виконання цієї Інструкції у ЗОЗ є його керівник, у структурних підрозділах ЗОЗ — відділ з інфекційного контролю та керівники структурних підрозділів.
4. У цій Інструкції терміни та умовні скорочення вживаються у такому значенні:
аптека ЗОЗ (далі — аптека) — самостійний структурний підрозділ в закладі охорони здоров’я, основним завданням якого є забезпечення пацієнтів ЗОЗ лікарськими засобами;
деескалація АМП — переведення пацієнта на: пероральний прийом АМП після ін’єкційного введення; прийом АМП вузького спектру дії після призначення АМП широкого спектру; монотерапію АМП після комбінованої антимікробної терапії (далі — АМП-терапія);
ескалація АМП — переведення пацієнта на: ін’єкційне введення АМП після перорального; прийом АМП широкого спектру дії після АМП вузького спектру дії; комбіновану АМП-терапію після монотерапії АМП;
оптимізація АМП — незначні зміни в призначенні АМП, які не зазначені у визначеннях деескалації та ескалації АМП, такі як, наприклад, зниження добової дози і кратності введення АМП;
первинний афект — обмежений запальний процес на місці первинного потрапляння до організму збудників інфекційних хвороб;
профілактичне призначення антибіотиків в периопераційний період (далі — периопераційна АМП-профілактика) — введення пацієнту АМП до мікробної контамінації операційної рани або розвитку ранової інфекції, а також при наявності ознак контамінації та інфекції, коли методом лікування є хірургічне втручання, а призначені АМП мають за мету знизити до мінімуму ризик розвитку інфекцій області хірургічного втручання;
DDD — визначена добова доза;
MRSA — метицилін-резистентний золотистий стафілокок;
ВАП — вентилятор-асоційована пневмонія;
ВАРІТ — відділення анестезіології, реанімації та інтенсивної терапії;
ВІЛ — вірус імунодефіциту людини;
ВІК — відділ з інфекційного контролю;
ЗОЗ — заклад охорони здоров’я;
ІОХВ — інфекція області хірургічного втручання;
ІПНМД — інфекційні хвороби, пов’язані з наданням медичної допомоги;
КАІК — катетер-асоційована інфекція кровотоку;
КАІСВШ — катетер-асоційована інфекція сечовивідних шляхів;
КДІ — захворювання викликані C. difficile;
МАМР — множинна резистентність до антимікробних препаратів;
СОП — стандартна операційна процедура.
Інші терміни у цій Інструкції вживаються у значеннях, наведених в Законах України «Основи законодавства України про охорону здоров’я», «Про захист населення від інфекційних хвороб» та інших нормативно-правових актах у сфері охорони здоров’я.
II. Завдання та умови для впровадження адміністрування антимікробних препаратів
1. Завданнями впровадження заходів з адміністрування антимікробних препаратів (далі — ААП) є:
1) профілактика розповсюдження АМР в ЗОЗ і поза ним;
2) раціональне застосування АМП з профілактичною і лікувальною метою;
3) підвищення ефективності емпіричної АМП-терапії;
4) оптимізація/зниження витрат ЗОЗ на АМП;
5) зменшення терміну перебування пацієнтів на стаціонарному лікуванні;
6) оптимізація підходів до лікування ІПНМД.
2. Обов’язкові умови для впровадження та реалізації ААП:
1) у ЗОЗ створено ВІК, до складу якого входить клінічний провізор (координатор ААП);
2) наявність у структурі ЗОЗ мікробіологічної лабораторії або договору із мікробіологічною лабораторією, чи іншим ЗОЗ, у якого є мікробіологічна лабораторія, в якій впроваджено методику EUCAST;
3) наявність в структурі ЗОЗ аптеки, як структурного підрозділу;
4) СОП з раціоналізації використання АМП і моніторингу/контролю за АМР затверджено керівництвом ЗОЗ відповідно до положень цієї Інструкції і включають:
адміністрування призначення АМП в ЗОЗ;
алгоритми по діагностиці і лікуванню інфекційних захворювань;
преавторизація призначення АМП групи резерву;
моніторинг використання АМП групи резерву та АМР;
режими периопераційної АМП-профілактики.
III. Етапи впровадження адміністрування антимікробних препаратів
1. Перший або підготовчий етап — проведення клінічним провізором ВІК перевірки виконання ЗОЗ заходів з ААП відповідно до контрольного списку (чек-листа) наведеного в додатку 1 до цієї Інструкції, розробка і затвердження плану дій з ААП та СОП з адміністрування призначення АМП.
2. План дій з ААП затверджується керівником ЗОЗ на період одного року і довгостроковий (наприклад, п’ятирічний) з метою впровадження короткострокових і довгострокових заходів з раціоналізації споживання АМП. План дій включає заходи, індикатори їх виконання та визначення відповідальних за їх виконання осіб.
3. СОП з адміністрування призначення АМП розробляється та застосовується у ЗОЗ при призначенні, розподіленні, закупівлі та прийомі АМП з урахуванням наступного:
1) уніфікованих та нових клінічних протоколів медичної допомоги;
2) структури захворюваності в ЗОЗ;
3) даних локальної АМР клінічно значимих збудників інфекційних хвороб в ЗОЗ;
4) результатів клінічних досліджень щодо найбільш ефективних і безпечних схем АМП-терапії;
5) клінічної необхідності, науково доведеної і задокументованої клінічної ефективності АМП, відсутності в СОП АМП, який задовольняє такі ж потреби;
6) АМП задовольняє ЗОЗ по співвідношенню затрати/ефективність;
7) потреб ЗОЗ щодо профілактики і лікування основних нозологічних форм негоспітальних інфекцій та ІПНМД, профілю і спеціалізації ЗОЗ;
8) призначення пацієнтам ЗОЗ АМП, які не включено до цієї СОП заборонено, окрім випадків клінічного випробовування АМП, що проводиться відповідно до законодавства.
4. СОП з адміністрування призначення АМП включає:
1) перелік АМП з найбільшою доказовою базою щодо їх ефективності, безпеки та економічно вигідного використання коштів ЗОЗ, сформований на основі Локального формуляру лікарських засобів ЗОЗ, затвердженого відповідно до Положення про локальний формуляр лікарських засобів закладу охорони здоров’я, затвердженого наказом Міністерства охорони здоров’я України від 22 липня 2009 року № 529, зареєстрованого в Міністерстві юстиції України 29 жовтня 2009 року за № 1006/17022;
2) АМП для периопераційної АМП-профілактики та емпіричної АМП-терапії;
3) фармакотерапевтичні групи АМП;
4) групу преавторизації призначення щодо кожного АМП згідно із пунктом 6 цього розділу;
5) лікарську форму кожного з АМП;
6) стислий опис області застосування АМП (негоспітальні чи нозокоміальні інфекції, локалізація інфекційних захворювань);
7) клінічні підрозділи ЗОЗ, в яких дозволено використання кожного з АМП (за потреби).
5. СОП з адміністрування призначення АМП затверджується керівником ЗОЗ та переглядається мінімум один раз на рік із врахуванням локальних даних щодо АМР і появи нових АМП. Примірну СОП з адміністрування призначення АМП в ЗОЗ, який надає медичну допомогу в стаціонарних умовах дорослому населенню, наведено у додатку 2 до цієї Інструкції.
6. Визначення преавторизації призначення кожного АМП здійснюється шляхом віднесення його до однієї з трьох груп:
1) група А (група доступу) — АМП, які лікар ЗОЗ може призначити самостійно для лікування і профілактики інфекційних захворювань у відповідності до затверджених в ЗОЗ протоколів або алгоритмів лікування;
2) група В (група спостереження) — АМП, призначення яких має бути погоджено клінічним провізором ВІК, в тому числі шляхом впровадження в ЗОЗ нових клінічних протоколів емпіричної АМП-терапії;
3) група С (група резерву) — резервні АМП, призначення яких має бути узгоджено із клінічним провізором, шляхом заповнення форми преавторизації АМП групи резерву, яка наведена в додатку 3 до цієї Інструкції.
В багатопрофільних ЗОЗ переліки АМП в групах преавторизації можуть відрізнятися для деяких відділень (наприклад, для ВАРІТ рекомендовано об’єднати групи А і В в групу А).
Важливим фактором віднесення АМП до однієї із груп є поточна ситуація із локальною АМР. Наприклад, якщо для клінічного підрозділу або ЗОЗ характерна висока резистентність більшості бактерій до цефалоспоринів III покоління, їх слід віднести до групи В або С, мінімум для ІПНМД.
В ЗОЗ, що тимчасово недоукомплектовані клінічними провізорами, дозволяється використання спрощеної схеми преавторизації призначення АМП із застосуванням лише двох груп: групи А (призначаються лікуючим лікарем) та групи С (призначення має бути погоджено консиліумом лікарів і узгоджено із профільним заступником керівника ЗОЗ).
7. Другий етап включає впровадження нових клінічних протоколів периопераційної антибіотикопрофілактики і емпіричної АМП-терапії щодо найбільш поширених негоспітальних інфекцій (наприклад, інфекції дихальної системи, шкіри та підшкірної клітковини, кишкові інфекції) та ІПНМД (мінімум щодо ВАП, КАІК, КАІСВШ, ІОХВ), за необхідності (наприклад, у високоспеціалізованому стаціонарі) такі протоколи впроваджуються щодо інфекцій інших локалізації та походження.
Впровадження нових клінічних протоколів периопераційної антибіотикопрофілактики і емпіричної АМП-терапії здійснюється відповідно до Методики розробки та впровадження медичних стандартів медичної допомоги на засадах доказової медицини, затвердженої наказом Міністерства охорони здоров’я України від 28 вересня 2012 року № 751, зареєстрованої в Міністерстві юстиції України 29 листопада 2012 року за № 2001/22313, з урахуванням даних локальної АМР (мікробіологічного моніторингу).
Для формування репрезентативної вибірки при проведенні мікробіологічного моніторингу клінічним провізором ВІК та епідеміологом ВІК аналізуються результати посівів первинних зразків із первинних афектів мінімум за 12 місяців. До формування власної локальної бази чутливості мікроорганізмів до АМП, використовуються регіональні або національні дані.
Нові клінічні протоколи емпіричної АМП-терапії рекомендовано інтегрувати в інформаційну систему ЗОЗ з метою автоматичного нагадування лікуючому лікарю про необхідність проведення певних дій щодо призначеної АМП-терапії (наприклад, необхідності оцінки ефективності чи завершенні рекомендованого терміну лікування АМП).
8. Третій етап — навчання, підготовка і перевірка знань лікарів, що включає:
1) проведення навчально-підготовчих заходів (наприклад, семінари, лекції, тренінги, розповсюдження інформаційних матеріалів в електронному або друкованому вигляді) із наступною перевіркою знань (наприклад, тестування) необхідно проводити для кожної із цільових груп окремо (наприклад, лікарі-хірурги, лікарі-анестезіологи, лікарі-реаніматологи, лікарі-інфекціоністи, лікарі-пульмонологи);
2) проведення персональних консультувань з питань АМП-терапії та АМР клінічним провізором ВІК.
9. На четвертому етапі впроваджується система моніторингу, оцінки і зворотного зв’язку, що включає:
1) аналіз причин безпідставної видачі АМП широкого спектру дії з аптеки у клінічні відділення;
2) перевірку наявності та інформативність записів в медичній документації щодо обґрунтування призначення, заміни та відміни АМП;
3) ретроспективний аудит відповідності призначення АМП-терапії затвердженим медико-технологічним документам. Для проведення аудиту проводиться відбір та аналіз 5 — 10 % медичних карт стаціонарних хворих (форма первинної облікової документації № 003/о «Медична карта стаціонарного хворого № ____», затверджена наказом Міністерства охорони здоров’я України від 14 лютого 2012 року № 110 (у редакції наказу Міністерства охорони здоров’я України від 21 січня 2016 року № 29), зареєстрована в Міністерстві юстиції України 12 лютого 2016 року за № 230/28360, форма первинної облікової документації № 097/о «Медична карта новонародженого № ____», затверджена наказом Міністерства охорони здоров’я України від 21 січня 2016 року № 29, зареєстрована в Міністерстві юстиції України 12 лютого 2016 року за № 233/28363, форма первинної облікової документації № 096/о «Історія вагітності та пологів № ___», затверджена наказом Міністерства охорони здоров’я України від 21 січня 2016 року № 29, зареєстрована в Міністерстві юстиції України 12 лютого 2016 року за № 232/28362) або Реєстру медичних записів, записів про направлення та рецептів в електронній системі охорони здоров’я). Аналіз проводиться для кожного клінічного підрозділу ЗОЗ окремо.
Для проведення ретроспективного аудиту відповідності призначення АМП клінічним провізором ВІК ЗОЗ заповнюється форма, наведена в додатку 4 до цієї Інструкції. При заповненні форми ретроспективного аудиту відповідності призначення АМП заборонено використовувати ідентифікаційні дані про лікуючого(их) лікаря(ів), оскільки метою проведення аудиту не є його/їх покарання.
Для проведення ретроспективного аудиту рекомендовано використовувати електронні форми або відповідне програмне забезпечення медичної інформаційної системи ЗОЗ.
Заповнені форми для проведення ретроспективного аудиту відповідності призначення АМП після проведення їх аналізу можуть використовуватися для проведення навчання і підготовки лікарів ЗОЗ. Строки зберігання для цих форм не встановлюються;
4) рівень споживання АМП в ЗОЗ відповідно до розділу V цієї Інструкції.
10. Останній п’ятий етап впровадження — це оцінка ефективності ААП. Регулярний аналіз критеріїв ефективності дозволяє оцінити чи досягнені основні цілі ААП.
11. Після проведення оцінки ефективності (п’ятого етапу) слід повернутися до першого етапу: провести перевірку виконання ЗОЗ заходів з ААП відповідно до контрольного списку (чек-листа) наведеного в додатку 1 до цієї Інструкції і внести зміни або затвердити новий план дій в залежності від отриманих результатів. Реалізація ААП має бути циклічною і тривати постійно.
12. Незалежно від етапу реалізації ААП проводиться аналіз локальної АМР та забезпечення ресурсами (кадровими і фінансовими) мікробіологічної лабораторії.
IV. Показники оцінки ефективності адміністрування антимікробних препаратів
1. Аналіз ефективності ААП дозволяє оцінити ступінь досягнення цілей і своєчасно скорегувати направленість заходів.
2. До організаційних показників ефективності ААП відносяться показники, які характеризують дотримання вимог до ЗОЗ:
1) СОП з адміністрування призначення АМП в ЗОЗ забезпечений фінансово (наявність АМП в достатній кількості та у відповідності до потреб ЗОЗ);
2) впроваджено преавторизацію призначення АМП;
3) проводяться навчання, підготовка і перевірка знань лікарів з питань АМП-терапії;
4) наявний електронний інструмент (програмне забезпечення), що надає можливість відстежувати призначені і видані АМП, формувати вибірку в залежності від діагнозу і проводити DDD-аналіз.
3. Оцінка ефективності реалізації ААП проводиться за наступними показниками:
1) показники розповсюдженості АМР, що засновані на аналізі загальної структури збудників і структури збудників інфекційних захворювань різних локалізацій. Аналіз розповсюдженості є обов’язковим для групи бактерій ESKAPE, що включає:
E. faecium VR — ванкоміцинрезистентний E. faecium;
S. aureus MR — метицилінрезистентний золотистий стафілокок;
K. pneumoniae KPC — K. pneumoniae, що продукує карбапенемази;
A. baumannii MDR — A. baumannii із множинною резистентністю до антимікробних препаратів;
P. aeruginosa MDR — P. aeruginosa із множинною резистентністю до антимікробних препаратів;
Enterobacteriaceae ESBL — грамнегативні ентеробактерії, що продукують b-лактамази розширеного спектру;
2) показники фармакоекономічної ефективності АМП-терапії:
рівень загального споживання АМП / групи АМП / окремого АМП в ЗОЗ:
РСА — рівень загального споживання АМП / групи АМП / окремого АМП в ЗОЗ;
ЗКА — загальна кількість DDD АМП / групи АМП;
ЛД — загальна кількість ліжкоднів, які провели пацієнти в ЗОЗ;
число курсів АМП-терапії на одного пацієнта за одиницю часу:
ЧКТ — число курсів АМП-терапії за одиницю часу;
ККТ — кількість курсів АМП-терапії за одиницю часу;
КП — кількість пацієнтів за одиницю часу;
середня тривалість курсу АМП-терапії за одиницю часу:
СТК — середня тривалість курсу АМП-терапії за одиницю часу;
ДАТ — загальна кількість днів АМП-терапії у всіх пацієнтів за одиницю часу;
КПА — загальна кількість пацієнтів, які отримували АМП-терапію за одиницю часу;
кількість днів АМП-терапії за одиницю часу:
КДА — кількість днів АМП-терапії за одиницю часу;
ДАТ — загальна кількість днів АМП-терапії у всіх пацієнтів за одиницю часу;
КП — кількість пацієнтів за одиницю часу;
частота деескалації:
ЧД — частота деескалації;
ПД — загальна кількість випадків проведеної деескалації у всіх пацієнтів;
ВД — загальна кількість випадків можливої деескалації у всіх пацієнтів;
3) показники щодо лікування пацієнтів з інфекційними захворюваннями:
тривалість перебування пацієнтів із інфекційними захворюваннями у ВАРІТ та ЗОЗ в цілому;
частота бактеріємій, що викликані збудниками з МАМР;
частота кандідемій;
рівень летальності в групі пацієнтів з інфекційними захворюваннями;
4) індекс резистентності до АМП, методика розрахунку якого наведена в додатку 5 до цієї Інструкції;
5) показники оцінки ефективності адміністрування АМП, які використовуються для:
порівняльної оцінки дотримання протоколів діагностики інфекційних захворювань та АМП-терапії між різними відділеннями ЗОЗ;
визначення проблем та досягнень ААП;
розробки плану проведення навчальних програм і оцінки їх ефективності.
Показники оцінки ефективності адміністрування АМП визначаються ВІК із врахуванням рівня розповсюдженості ІПНМД, АМР та спеціалізації ЗОЗ для деяких найбільш проблемних і добре стандартизованих компонентів застосування АМП, таких як наприклад, але не обмежуються ними:
стафілококова бактеріємія (показники оцінки ефективності адміністрування АМП при стафілококовій бактеріємії наведено в додатку 6 до цієї Інструкції);
ентерококова бактеріємія;
периопераційна АМП-профілактика (показники оцінки ефективності адміністрування АМП при проведенні периопераційної антибіотикопрофілактики наведено в додатку 7 до цієї Інструкції);
сепсис;
тяжка негоспітальна пневмонія;
ВАП;
інфекційний ендокардит;
MRSA-інфекція.
4. Розрахунок показників, наведених в пункті 3 цього розділу, клінічному провізору ВІК слід проводити регулярно — мінімум один раз на рік, порівнюючи дані до та після впровадження заходів з ААП.
5. Звіт довільної форми щодо проведеної оцінки ефективності ААП надається керівнику ЗОЗ та його заступнику з медичної частини, керівникам клінічних підрозділів ЗОЗ і керівнику мікробіологічної лабораторії.
V. Моніторинг та ведення обліку споживання антимікробних лікарських засобів
1. На національному рівні моніторинг споживання АМП здійснюється шляхом збору даних щодо споживання АМП в ЗОЗ, аналізу та ведення обліку споживання АМП, резистентності до АМП основних збудників ІПНМД, підготовки інформації для прийняття управлінських рішень, підготовки даних звітності для інтеграції у європейську і міжнародну системи даних щодо споживання АМП.
2. На регіональному рівні (обласний, на рівні територіальних громад та окремих ЗОЗ) завданням моніторингу є спостереження за динамікою споживання АМП, факторами та умовами, що впливають на динаміку споживання АМП, узагальнення та аналіз одержаної інформації для розробки заходів, направлених на раціональне споживання АМП.
3. Моніторинг споживання АМП проводиться ВІК ЗОЗ (клінічним провізором) за наступними показниками:
1) рівень загального споживання АМП групи резерву за рік. До антибіотиків групи резерву належать:
азтреонам;
цефтаролін фосаміл;
цефтазидим-авібактам;
цефтобіпрол медокаріл;
цефтолозан-тазобактам;
колістин;
далбаванцин;
далфопрістин-квінупрістин;
даптоміцин;
еравациклін;
фаропенем;
фосфоміцин;
лінезолід;
меропенем-ваборбактам;
міноциклін;
омадациклін;
орітаванцин;
плазоміцин;
поліміксин В;
тедізолід;
телаванцин;
тайгециклін;
2) рівень загального споживання наступних АМП групи спостереження за рік:
цефтріаксон;
цефазолін;
цефуроксим;
ципрофлоксацин;
левофлоксацин;
моксифлоксацин;
меропенем;
3) індекс резистентності до АМП наступних бактерій:
E. coli;
K. pneumoniae;
Salmonella spp.;
P. aeruginosa;
Acinetobacter spp.;
S. aureus;
S. pneumoniae;
E. faecalis;
E. faecium.
Розрахунок рівня загального споживання АМП наведено в підпункті 2 пункту 3 розділу IV цієї Інструкції.
Розрахунок рівня індексу резистентності до АМП наведено в додатку 5 до цієї Інструкції.
4. Дані моніторингу за споживанням АМП в ЗОЗ протягом року вносяться лікарями клінічних структурних підрозділів або відповідальною особою, визначеною керівником клінічного структурного підрозділу, в форму моніторингу споживання антимікробних препаратів, наведену в додатку 8 до цієї Інструкції, та передаються у ВІК ЗОЗ, який надає зведені дані, відповідно до форми спостереження та ведення обліку споживання антимікробних препаратів, наведеної в додатку 9 до цієї Інструкції, в заклад громадського здоров’я, який реалізує заходи з боротьби з антимікробною резистентністю відповідно до адміністративно-територіальної належності (далі — ЗГЗ) до 1 березня року наступного за дослідним.
5. ЗГЗ передає зведені дані до державної установи «Центр громадського здоров’я Міністерства охорони здоров’я України» до 1 квітня року наступного за дослідним.
Генеральний директор Директорату громадського здоров’я
та профілактики захворюваності
І. Руденко
Додаток 1
до Інструкції з впровадження адміністрування
антимікробних препаратів в закладах охорони здоров’я,
які надають медичну допомогу в стаціонарних умовах
(пункти 1, 11 розділу III)
Контрольний лист з виконання обов’язкових умов та заходів для впровадження адміністрування антимікробних препаратів в закладі охорони здоров’я
Обов’язкова умова/захід |
Відмітка про виконання |
|
так |
ні |
|
1 |
2 |
3 |
Створено відділ з інфекційного контролю (далі — ВІК) |
||
ВІК укомплектовано клінічним провізором, який виконує функції виключно з ААП |
||
ВІК укомплектовано лікарем-епідеміологом |
||
Функціонує медична інформаційна система із можливістю відстежування призначення АМП |
||
Клінічним провізором ВІК розроблено та керівником ЗОЗ затверджено план дій щодо адміністрування АМП для забезпечення належного використання антибіотиків, на основі наявних національних та/або міжнародних настанов. |
||
План дій щодо адміністрування АМП переглядається мінімум один раз на рік |
||
На виконання заходів (пунктів) плану дій передбачено фінансування |
||
В структурі ЗОЗ наявна або заключено договір із мікробіологічною лабораторією, чи іншим ЗОЗ, у якого є мікробіологічна лабораторія, в якій впроваджено методику EUCAST |
||
В структурі ЗОЗ наявна аптека |
||
Керівником ЗОЗ затверджено СОП з адміністрування призначення антимікробних препаратів |
||
Затверджено алгоритми по діагностиці і лікуванню інфекційних захворювань |
||
Нові клінічні протоколи емпіричної АМП-терапії впроваджуються клінічним провізором ВІК і затверджені керівником ЗОЗ мінімум щодо негоспітальних інфекцій (інфекції дихальної системи, шкіри та підшкірної клітковини, кишкові інфекції) |
||
Нові клінічні протоколи емпіричної АМП-терапії впроваджуються клінічним провізором ВІК і затверджені керівником ЗОЗ мінімум щодо наступних ІПНМД: вентилятор-асоційована пневмонія, катетер-асоційована інфекція кровотоку, катетер-асоційована інфекція сечовивідних шляхів, інфекція області хірургічного втручання |
||
Нові клінічні протоколи емпіричної АМП-терапії в ЗОЗ на етапі розробки обов’язково погоджуються з лікарями-клініцистами |
||
Щодо нових клінічних протоколів емпіричної АМП-терапії в ЗОЗ проводяться навчання і підготовка |
||
Впроваджено систему преавторизації щонайменше для антимікробних препаратів групи резерву |
||
Проводиться моніторинг призначення антимікробних препаратів (щонайменше групи резерву) |
||
Керівником ЗОЗ затверджено режими периопераційної антимікробної профілактики |
||
Епідеміологом ВІК проводиться оцінка розповсюдженості антимікробної резистентності (щонайменше для групи бактерій ESKAPE) |
||
Клінічним провізором ВІК проводиться оцінка рівня споживання АМП (щонайменше групи резерву) |
||
Клінічним провізором ВІК проводиться оцінка числа курсів АМП на одного пацієнта за одиницю часу |
||
Клінічним провізором ВІК проводиться оцінка середньої тривалості курсу АМП-терапії за одиницю часу |
||
Клінічним провізором ВІК проводиться оцінка кількості днів АМП-терапії за одиницю часу |
||
Клінічним провізором ВІК проводиться оцінка частоти деескалації |
||
Клінічним провізором ВІК проводиться щорічне визначення індексу резистентності |
||
Клінічним провізором ВІК проводиться оцінка ефективності адміністрування АМП (щонайменше щодо стафілококової та ентерококової бактеріємій, сепсису, периопераційної антибіотикопрофілактики, тяжкої негоспітальної пневмонії, вентилятор-асоційованої пневмонії) |
||
Додаток 2
до Інструкції з впровадження адміністрування
антимікробних препаратів в закладах охорони здоров’я,
які надають медичну допомогу в стаціонарних умовах
(пункт 5 розділу III)
Примірна стандартна операційна процедура з адміністрування призначення антимікробних препаратів в закладі охорони здоров’я, який надає медичну допомогу в стаціонарних умовах дорослому населенню
Антимікробний препарат і група преавторизації |
Лікарська форма |
Область застосування |
Примітки/клінічні підрозділи, в яких дозволено використання (за потреби) |
1 |
2 |
3 |
4 |
Пеніциліни |
|||
Бензилпеніцилін (А) |
ПЕ |
Інфекційні захворювання центральної нервової системи, анаеробні інфекції шкіри і м’яких тканин, актиномікоз |
Може бути замінений іншими антимікробними лікарськими засобами (далі — АМП) |
Ампіцилін (А) |
ПЕ |
Нетяжкі інфекційні захворювання нижніх дихальних шляхів, інфекційні захворювання ЦНС, інфекційний ендокардит стрептококової етіології та інші стрептококові інфекції, інфекції викликані E. faecalis |
Пероральні форми використовувати не рекомендовано через низьку біодоступність |
Амоксицилін (А) |
ПО |
Нетяжкі інфекційні захворювання нижніх дихальних шляхів (пневмонія, бронхіт), гострий риносинусит, тонзиліт, інфекції викликані E. faecalis, в схемах ерадикації H. pylori |
|
Ампіцилін/сульбактам (А або В) |
ПЕ |
Інфекційні захворювання верхніх і нижніх дихальних шляхів, негоспітальні абдомінальні інфекції та інфекційні захворювання органів малого тазу, запалення легень, пов’язане із наданням медичної допомоги (окрім ВАП), інфекційні захворювання викликані Acinetobacter spp. |
|
Амоксицилін/клавуланат або амоксицилін/сульбактам (А або В) |
ПЕ і ПО |
Інфекційні захворювання верхніх і нижніх дихальних шляхів, негоспітальні абдомінальні інфекційні захворювання та інфекційні захворювання органів малого тазу, запалення легень, пов’язане із наданням медичної допомоги (окрім ВАП) |
У амоксициліна/клавуланата наявна більш повна доказова база клінічної ефективності |
Піперацилін/тазобактам © |
ПЕ |
ІПНМД поза ВАРІТ: шкіри і м’яких тканин, абдомінальні, бронхолегеневі, сечовидільної системи; інфекційні захворювання викликані P. aeruginosa |
В порівнянні із цефалоспоринами і фторхінолонами, використання піперациліну/тазобактаму супроводжується суттєво меншими екологічними збитками, а саме меншим ризиком селекції полірезистентних бактерій, в тому числі продуцентів b-лактамаз розширеного спектру |
Цефалоспорини |
|||
Цефазолін (А) |
ПЕ |
Інфекційні захворювання викликані стафілококом чутливим до оксациліну, периопераційна профілактика, інфекційний ендокардит |
|
Цефалексин (А) |
ПО |
Нетяжкі інфекційні захворювання викликані стафілококом чутливим до оксациліну, в якості засобу ступеневої терапії після використання цефазоліну |
|
Цефуроксим (А) |
ПЕ |
Периопераційна профілактика |
|
Цефуроксим аксетил (А) |
ПО |
Нетяжкі інфекційні захворювання дихальних шляхів |
Більш висока стійкість пневмококів (в порівнянні з амінопеніцилінами) лімітує ефективне використання |
Цефотаксим або цефтріаксон (А або В) |
ПЕ |
Негоспітальна пневмонія, інфекції сечовивідних шляхів, негоспітальні абдомінальні інфекційні захворювання, ІПНМД поза ВАРІТ, інфекційні захворювання ЦНС |
Антимікробна активність і клінічна ефективність цих препаратів схожа. Високий рівень стійкості лімітує використання цих АМП для лікування ІПНМД. Високий ризик колатеральних збитків (селекція ентеробактерій продуцентів b-лактамаз розширеного спектру). |
Цефтазидим або цефоперазон (В або С) |
ПЕ |
Інфекційні захворювання викликані P. aeruginosa, тяжке загострення ХОЗЛ, бронхоектатична хвороба |
По антимікробній активності цефтазидим переважає цефоперазон. Високий рівень стійкості лімітує використання цих АМП для лікування ІПНМД. Високий ризик колатеральних збитків (селекція ентеробактерій продуцентів b-лактамаз розширеного спектру). |
Цефіксим або цефдиторен (В) |
ПО |
Негоспітальні інфекції сечовивідних шляхів, загострення ХОЗЛ, риносинусит, в якості препарату ступінчастої терапії після використання цефотаксиму або цефтріаксону |
Низька антипневмококова активність лімітує застосування при респіраторних інфекційних захворюваннях. |
Цефдиторен (В) |
ПО |
Негоспітальна пневмонія, загострення ХОЗЛ, риносинусит, в якості препарату ступінчастої терапії після використання цефотаксиму або цефтріаксону |
|
Цефепім (В) |
ПЕ |
ІПНМД поза ВАРІТ, інфекційні захворювання викликані P. aeruginosa |
|
Цефоперазон/сульбактам © |
ПЕ |
ІПНМД у ВАРІТ, гострий деструктивний панкреатит, інфекційні захворювання викликані Acinetobacter spp. |
|
Карбапенеми |
|||
Іміпенем © |
ПЕ |
ІПНМД у ВАРІТ, тяжкий сепсис, інфекційні захворювання викликані продуцентами b-лактамаз розширеного спектру, гострий деструктивний панкреатит |
Повна перехресна стійкість до антипсевдомоназних карбапенемів серед неферментуючих збудників ІПНМД відсутня, тому в СОП мають бути присутні всі три препарати |
Меропенем © |
ПЕ |
ІПНМД у ВАРІТ, тяжкий сепсис, інфекційні захворювання викликані продуцентами b-лактамаз розширеного спектру, гострий деструктивний панкреатит, ІПНМД ЦНС |
|
Доріпенем © |
ПЕ |
ВАП, абдомінальні інфекційні захворювання, тяжкий сепсис, інфекційні захворювання викликані P. aeruginosa |
Володіє найвищою активністю серед карбапенемів по відношенню до P. aeruginosa та більш низьким потенціалом розвитку резистентності. |
Ертапенем © |
ПЕ |
Тяжкі негоспітальні інфекційні захворювання: абдомінальні, шкіри і м’яких тканин, органів малого тазу, сечовивідних шляхів. ІПНМД поза ВАРІТ: пневмонія, перитоніт, ІОХВ, післяродовий сепсис. Периопераційна профілактика при наявності високого ризику післяопераційних ускладнень, що зумовлені резистентною флорою |
Карбапенем 1-ї лінії при тяжкому сепсисі (негоспітальному і пов’язаному із наданням медичної допомоги) та за відсутності ризику P. aeruginosa |
Аміноглікозиди |
|||
Гентаміцин або тобраміцин (А) |
ПЕ |
Негоспітальні інфекційні захворювання сечовивідних шляхів, комбінована терапія стафілококових і ентерококових інфекцій (в поєднанні з оксациліном або ампіциліном) |
Високий рівень стійкості лімітує використання з метою лікування ІПНМД |
Амікацин (В) |
ПЕ |
ІПНМД сечовивідних шляхів, в комбінованій терапії інфекцій викликаних P. aeruginosa |
|
Макроліди |
|||
Еритроміцин (А) |
ПЕ |
В комбінованій терапії тяжкої негоспітальної пневмонії |
Суттєва різниця в антимікробній активності серед макролідів відсутня. Високий рівень стійкості пневмококів лімітує використання еритроміцину, кларитроміцину і азитроміцину при респіраторних інфекційних захворюваннях. Керуючись позицією мінімальної достатності, в СОП необхідно включити один ПЕ-макролід (еритроміцин або кларитроміцин) і два ПО-макроліда (джозаміцин і кларитроміцин). |
Кларитроміцин (А) |
ПЕ і ПО |
В комбінованій терапії тяжкої негоспітальної пневмонії, в схемах ерадикації H.pylori, в комбінованій терапії інфекційних захворювань органів малого тазу, захворювання викликані хламідіями і мікоплазмами |
|
Азитроміцин (А) |
ПЕ і ПО |
В комбінованій терапії інфекційних захворювань органів малого тазу, захворювання викликані хламідіями і мікоплазмами |
|
Джозаміцин (А) |
ПО |
Нетяжка негоспітальна пневмонія, в схемах ерадикації H. pylori |
|
Лінкозаміди |
|||
Кліндаміцин або лінкоміцин (В) |
ПЕ і ПО |
В комбінованій терапії ускладненої негоспітальної пневмонії, захворювання стафілококової етіології, інфекційні захворювання шкіри і м’яких тканин (в тому числі некротизуючі), інфекційні захворювання кісток і суглобів |
Препарати вибору при захворюваннях викликаних метицилін (оксацилін)-чутливими S. aureus у пацієнтів із непереносимістю b-лактамів. В СОП рекомендовано включити кліндаміцин, як препарат, що має більш виражену антистафілококову активність. |
Глікопептиди і ліпопептиди |
|||
Ванкоміцин © |
ПЕ |
Захворювання викликані MRSA, різноманітної локалізації, антибіотикасоційована діарея та псевдомембранозний коліт (ПО) |
Зниження чутливості MRSA до ванкоміцину лімітує ефективне його використання, особливо при ендокардиті, менінгіті і пневмонії. Дозволено застосування ванкоміцину у випадках MRSA з МІК Ј 1 мкг/мл, при більш високих МІК необхідно використовувати АМП інших класів. |
Даптоміцин © |
ПЕ |
Ангіогенні інфекції викликані MRSA, в тому числі викликані штамами зі зниженою чутливістю до ванкоміцину (МІК > 1 мкг/мл), ускладнені інфекційні захворювання шкіри і м’яких тканин, інфекційний ендокардит трикуспідального клапану або із задокументованою стафілококовою етіологією, інфекція м’яких тканин із залученням імпланту суглобу та/або кістки |
|
Оксазолідінони |
|||
Лінезолід © |
ПЕ і ПО |
Захворювання викликані MRSA, різноманітної локалізації (окрім ангіогенних і органів сечовидільної системи), в тому числі викликані штамами зі зниженою чутливістю до ванкоміцину (МІК > 1мкг/мл), в комбінованій терапії ВАП, ІПНМД шкіри і м’яких тканин |
Ризик лікарської взаємодії |
Рифаміцини |
|||
Рифампін, рифампіцин (В) |
ПЕ і ПО |
В комбінованій терапії захворювань викликаних MRSA (інфекційний ендокардит, менінгіт, остеомієліт) |
Ризик лікарської взаємодії |
Тетрацикліни |
|||
Доксициклін (А) |
ПЕ і ПО |
В комбінованій терапії інфекційних захворювань органів малого тазу, захворювання спричинені хламідіями і мікоплазмами |
|
Гліцилцикліни |
|||
Тігециклін © |
ПЕ |
Негоспітальні і пов’язані з наданням медичної допомоги ускладнення абдомінальних інфекційних захворювань, ІОХВ, захворювання викликані полірезистентними штамами Acinetobacter spp., E. coli, Klebsiella spp., в тому числі продуцентами карбапенемаз |
При захворюваннях викликаних продуцентами карбапенемаз ефективність в комбінованій терапії вище. |
Поліміксини |
|||
Колістин © |
ІН |
В комбінованій терапії ВАП з ризиком полірезистентних збудників, а також при захворюваннях спричинених Acinetobacter spp. та P. aeruginosa стійких до інших АМП |
|
Поліміксин В © |
ПЕ |
ІПНМД викликані полірезистентними грамнегативними бактеріями, насамперед Acinetobacter spp. і P. aeruginosa, а також E. coli і Klebsiella spp. стійких до карбапенемів |
При захворюваннях викликаних продуцентами карбапенемаз ефективність в комбінованій терапії вище. |
Фторхінолони |
|||
Ципрофлоксацин (Б або В) |
ПЕ і ПО |
ІПНМД різних локалізацій, інфекційні захворювання сечовивідних шляхів, бактеріальний простатит, тяжке ХОЗЛ з бронхоектазами, захворювання викликані чутливими штамами P. aeruginosa |
Висока стійкість штамів грамнегативних бактерій, які викликають ІПНМД, лімітує ефективне використання. Високий ризик колатеральних збитків (селекція полірезистентної P. aeruginosa та MRSA). |
Офлоксацин (Б) |
ПЕ і ПО |
ІПНМД різних локалізацій поза ВАРІТ без ризику P. aeruginosa, інфекційні захворювання сечовивідних шляхів і простатит (офлоксацин), інфекційні захворювання жовчовивідних шляхів (пефлоксацин) |
|
Левофлоксацин або моксифлоксацин (В або С) |
ПЕ і ПО |
Тяжка або ускладнена негоспітальна пневмонія, загострення ХОЗЛ, ускладнені інфекційні захворювання сечовивідних шляхів і простатит (левофлоксацин), негоспітальні ускладнені абдомінальні інфекційні захворювання та інфекційні захворювання органів малого тазу, негоспітальні ускладнені інфекційні захворювання шкіри і м’яких тканин, ВАП (левофлоксацин) |
Протимікробна активність цих препаратів приблизно однакова. Керуючись позицією мінімальної достатності, в СОП рекомендовано включити левофлоксацин, що має більш широкий спектр показань до призначення. |
Нітроімідазоли |
|||
Метронідазол (А) |
ПЕ і ПО |
В комбінованій терапії змішаних аеробно-анаеробних захворювань (абдомінальні, органів малого тазу, некротизуючі м’яких тканин, ЦНС), антибіотикасоційована діарея і псевдомембранозний коліт (КДІ), інфекційні захворювання печінки і жовчовивідних шляхів викликані лямбліями і амебами |
|
Нітрофурани |
|||
Нітрофурантоїн або фуразидин або фуразидин калію (А) |
ПО |
Негоспітальні інфекційні захворювання нижніх сечовивідних шляхів, в комбінованій терапії ІПНМД сечовивідних шляхів |
З позицій фармакокінетики і зручності дозування, в СОП рекомендовано включити фуразидин калію в лікарській формі з магнієм гідрокарбонатом |
Інші АМП |
|||
Ко-тримоксазол (В) |
ПЕ і ПО |
Пневмоцистна пневмонія (підтверджена або підозрювана), захворювання викликані S. maltophilia та Nocardia spp. |
|
Фосфоміцин © |
ПЕ |
Інфекційні захворювання викликані полірезистентними бактеріями стійкими до інших АМП (в комбінованій терапії) |
|
Мупіроцин © |
Місцево |
Назальна мазь для ерадикації носіїв MRSA у медичниз працівників або у пацієнтів перед оперативним втручанням. |
|
Антифунгальні препарати — азоли |
|||
Флуконазол (В) |
ПЕ і ПО |
Лікування і профілактика інвазивного кандидозу |
Збільшення стійкості Candida spp. лімітує ефективність використання. |
Вориконазол © |
ПЕ і ПО |
Препарат вибору при аспергильозі, альтернативний препарат при інвазивному кандидозі |
|
Ітраконазол © |
ПО (розчин) |
В якості препарату ступеневої терапії для завершення повного курсу лікування аспергільозу після прийому вориконазолу |
|
Антифунгальні препарати — ехінокандіни |
|||
Анідулафунгін або каспофунгін або мікафунгін © |
ПЕ |
Лікування і профілактика інвазивного кандидозу, особливо при ризику або документальному підтвердженні стійкості Candida spp. до флуконазолу або виявлення C. crusei |
Вибір ехінокандіну для стаціонару визначається його профілем. |
Противірусні препарати |
|||
Озельтамівір © |
ПО |
Лікування грипу |
Різниця в антивірусній активності і ефективності відсутня. В СОП слід включити один із двох препаратів. |
Занамівір © |
ІН |
Лікування грипу |
|
Ацикловір (В або С) |
ПЕ, ПО і місцево |
Захворювання викликані вірусами герпесу, в тому числі інфекційні захворювання ЦНС (енцефаліт, менінгіт, менінгоенцефаліт) |
|
Валацикловір або фамцикловір © |
ПО |
Захворювання викликані вірусом простого герпесу або варіцела-зостер вірусом |
Різниця в антивірусній активності і ефективності відсутня. В СОП слід включити один із двох препаратів. |
ПЕ — парентеральна лікарська форма; ПО — пероральна лікарська форма; ІН — інгаляційна лікарська форма; ЦНС — центральна нервова система; АМП — антимікробний препарат; ВАП — вентилятор-асоційована пневмонія; ІПНМД — інфекційні хвороби, пов’язані із наданням медичної допомоги; ВАРІТ — відділення анестезіології, реанімації та інтенсивної терапії; ХОЗЛ — хронічне обструктивне захворювання легень; ІОХВ — інфекція області хірургічного втручання; MRSA — метицилін (оксацилін)-резистентний S.aureus; МІК — мінімальна інгібуюча концентрація; КДІ — інфекційні захворювання викликані C. difficile. Повний перелік антимікробних засобів знаходиться за посиланням: https://www.whocc.no/atc_ddd_index/?code=J01&showdescription=no |
|||
Додаток 3
до Інструкції з впровадження адміністрування
антимікробних препаратів в закладах охорони здоров’я,
які надають медичну допомогу в стаціонарних умовах
(підпункт 3 пункту 6 розділу III)
Форма преавторизації антибактеріальних препаратів групи резерву.
Інформація про пацієнта |
|||||||||||||
Прізвище, ім’я та по батькові (за наявності)2 |
Вік3: |
Стать4: Ч |__| Ж |__| |
|||||||||||
Відділення5 |
Палата6 |
Алергія на АМП7: |
|||||||||||
Показання до антимікробної терапії8 |
|||||||||||||
Запит щодо дозволу на застосування антимікробних препаратів групи резерву |
|||||||||||||
Антибактеріальний препарат9 |
Доза і тривалість призначення10 |
Шлях введення11 |
Кратність введення на добу |
Причина призначення12 |
|||||||||
Чи наявні результати мікробіологічного дослідження з визначенням чутливості? Так |__| Ні |__| Якщо так, вкажіть деталі13:
|
|||||||||||||
Чи отримував пацієнт антимікробний препарат(и) до цього? Так |__| Ні |__| |
|||||||||||||
Антибіотик(и) |
Доза і тривалість призначення |
Шлях введення |
Кратність введення на добу |
Причина відміни |
|||||||||
Прізвище, ім’я та по батькові (за наявності) лікаря/контактний номер15: ______________ |
|||||||||||||
Коментар клінічного провізора16 |
|
Схвалення |
|
|__| СХВАЛЕНО |
|__| НЕ СХВАЛЕНО |
Примітки17: _________________________________________________________________________________ Прізвище, ім’я та по батькові (за наявності) / підпис клінічного провізора18: ________ / _______ Дата19:________ |
|
Примітки: 1. розділи форми преавторизації антибіотиків групи резерву (далі — форма) «Інформація про пацієнта», «Показання до антимікробної терапії» та «Запит щодо дозволу на застосування антимікробних препаратів групи резерву» заповнює лікуючий лікар; 2. розділи форми «Коментар клінічного провізора» та «Схвалення» заповнює клінічний провізор ВІК; 3. отримання схвалення клінічного провізора ВІК перед призначенням антибіотиків групи резерву є обов’язковим за наступним виключенням: форма не заповнюється в разі необхідності невідкладного призначення антибіотиків групи резерву пацієнту, який перебуває у відділенні реанімації та/або інтенсивної терапії за життєвими показаннями, про що є відповідний запис консиліуму лікарів у складі не менше трьох фахівців різних спеціальностей (наприклад, лікар-анестезіолог, лікар-хірург та лікар-інфекціоніст). ________ 2 прізвище, ім’я та по батькові (за наявності) пацієнта; 3 число повних років пацієнта; 4 слід відзначити «ч», якщо пацієнт чоловічої статі або «ж», якщо жіночої; 5 відділення, в якому перебуває пацієнт на час заповнення форми; 6 номер палати/кімнати, в якій перебуває пацієнт на час заповнення форми; 7 зазначається про наявність або відсутність алергічних реакцій на антимікробні препарати (далі — АМП), в тому числі відповідно до даних анамнезу. Якщо алергічні реакції наявні, слід зазначити АМП або групу АМП, на який(і) такі реакції відзначалися; 8 зазначається(ються) показання до призначення антибактеріальних препаратів групи резерву — наприклад, пневмонія, інфекція області хірургічного втручання, перитоніт. У випадках, якщо призначення антибактеріальних препаратів групи резерву засноване на стратифікації відповідно до ризиків інфікування пацієнта бактеріями з резистентністю, а не ґрунтується на результатах бактеріологічного обстеження, слід зазначити такі ризики; 9 зазначається один із наступних антибактеріальних препаратів: азтреонам, цефтаролін фосаміл, цефтазидим-авібактам, цефтобіпрол медокаріл, цефтолозан-тазобактам, колістин, далбаванцин, далфопрістин-квінупрістин, даптоміцин, еравациклін, фаропенем, фосфоміцин, лінезолід, меропенем-ваборбактам, міноциклін, омадациклін, орітаванцин, плазоміцин, поліміксин В, тедізолід, телаванцин, тайгециклін; 10 одноразова доза антибактеріального препарату групи резерву із зазначенням одиниць виміру (мкг, мг, гр, ОД, МО тощо) та прогнозована тривалість призначення в днях; 11 шлях введення антибактеріального препарату групи резерву пацієнту (пероральний, внутрішньовенний, внутрішньом’язевий, інгаляційний тощо); 12 зазначається причина призначення запитуваного антибактеріального препарату групи резерву (неефективність другого курсу антибіотикотерапії, результат бактеріологічного дослідження, високий ризик інфікування бактерією з множинною резистентністю тощо); 13 у відповідних графах зазначаються день, місяць і рік отримання результату дослідження, біологічний зразок (матеріал, який забрано для дослідження), бактерію та її чутливість до АМП (рекомендовано зазначати чутливість до групи АМП); 14 у відповідних графах зазначаються всі антибактеріальні препарати (діюча речовина або речовини), які пацієнт отримував до моменту заповнення форми, їх дози в одиницях виміру (мкг, мг, гр, ОД, МО тощо), тривалість призначення в днях, шлях введення (пероральний, парентеральний, інгаляційний тощо), кратність введення на добу та причини відміни (погіршення стану пацієнта, прогресування запального процесу, генералізація процесу, приєднання інфекційної хвороби, пов’язаної з наданням медичної допомоги тощо); 15 прізвище, ім’я, по батькові (за наявності) та контактний номер телефону лікуючого лікаря; 16 коментарі, які пояснюють схвалення / не схвалення видачі пацієнту антибактеріального препарату групи резерву (невірно заповнена форма, відсутні показання до призначення антибіотика групи резерву, пацієнт недостатньо обстежений, наявні інші варіанти антибактеріальної терапії без використання антибіотиків групи резерву тощо); 17 зазначаються вказівки для аптеки (наприклад, видати із відповідним розчинником); 18 прізвище, ім’я та по батькові (за наявності) клінічного провізора ВІК та його підпис; 19 день, місяць і рік заповнення форми. |
Додаток 4
до Інструкції з впровадження адміністрування
антимікробних препаратів в закладах охорони здоров’я,
які надають медичну допомогу в стаціонарних умовах
(підпункт 3 пункту 9 розділу III)
Форма для проведення ретроспективного аудиту відповідності призначення антимікробних препаратів
I. Інформація про пацієнта1 |
|||||||||||
Дата поступлення: |
Відділення: |
№ медичної карти: |
|||||||||
Прізвище, ім’я та по батькові (за наявності): |
Вік: |
Стать: Ч |__| Ж |__| |
|||||||||
Призначення антибіотиків2 |
|||||||||||
Антибіотик |
Доза |
Шлях введення |
Кратність введення на добу |
Дата початку терапії |
|||||||
II. Показання для антибіотикотерапії3 |
|||||||||||
Профілактика |__| |
Інфекція сечовивідних шляхів |__| |
Пневмонія |__| |
Інфекція ШКТ |__| |
Інфекція кровотоку |__| |
|||||||
Інфекція ЦНС |__| |
Шкірна інфекція |__| |
Інфекція кісток |__| |
Інше: |
||||||||
III. Первинний аналіз антибіотикотерапії |
|||||||||||
Чи задокументоване показання для призначення антибіотика?4 |
Чи призначено антибіотик відповідно до національних чи локальних настанов?5 |
Коментарі6 |
|||||||||
Чи коректна доза?7 |
Чи коректний шлях введення?8 |
Чи коректна тривалість лікування?9 |
|||||||||
IV. Аналіз антибіотикотерапії через 48 годин |
|||||||||||
1. Чи була переглянута антибіотикотерапія?10 Так |__| Ні |__| Якщо так, які дії? |
|||||||||||
Ескалація |__| |
Продовження |__| |
Деескалація |__| |
Припинення |__| |
Зміна в/в на per os |__| |
|||||||
2. Чому антибіотикотерапію було продовжено?11 |
|||||||||||
Наявність клінічних ознак інфекції |__| |
Підтвердження інфекції |__| |
Інше (коментар): |
|||||||||
3. Чи здійснено забір матеріалу для мікробіологічного дослідження?12 |
4. Чи отримано результати мікробіологічного дослідження?13 |
5. Чи вплинули на вибір АМП результати мікробіологічного дослідження?14 |
|||||||||
Загальні коментарі/висновок15: |
|||||||||||
Примітки: ________ 2 зазначається діюча речовина АМП в графі «Антибіотик», одноразова доза із зазначенням одиниці виміру (мкг, мг, гр, ОД, МО тощо) в графі «Доза», шлях введення у відповідній графі (пероральний, парентеральний, інгаляційний, місцево тощо), кратність введення на добу у відповідній графі та день, місяць і рік початку антибіотикотерапії у графі «Дата початку терапії». У випадках призначання комбінованого АМП (наприклад, цефоперазон + сульбактам), зазначаються дві діючі речовини комбінованого АМП та їх одноразові дози через розподільну риску (цефоперазон/сульбактам в графі «Антибіотик» та 1000 мг / 1000 мг в графі «Доза»); 3 відповідно до записів, які зазначені в медичній карті, може бути відмічено декілька пунктів: з профілактичною метою, лікування інфекції сечовивідних шляхів, пневмонії, інфекції шлунково-кишкового тракту, інфекції кровотоку (сепсису), інфекції центральної нервової системи, інфекції шкірних покривів, інфекції кісткових тканин або інше (зазначається, у тому числі додаткова причина призначення АМП); 4 «так», якщо лікуючим лікарем задокументовано в медичній карті показання для призначення антибіотика або «ні», якщо призначення антибіотика не задокументовано; 5 «так», якщо антибіотик призначено відповідно до нормативно-правових актів або протоколів антибіотикотерапії, затверджених керівником закладу, «ні» — якщо антибіотик призначено поза протоколів та зазначається причина в графі «Коментар»; 6 лаконічно зазначається причина невідповідного призначення антибіотика — наприклад, тяжкий стан пацієнта, який унеможливив додаткове обстеження, відсутність відповідного протоколу лікування, недотримання лікарем протоколу лікування; 7 відмічається «так» або «ні», якщо доза антибактеріального лікарського засобу відповідає або не відповідає рекомендованим відповідно до інструкції виробника та/або медико-технологічних документів (клінічні настанови, стандарти медичної допомоги, уніфіковані клінічні протоколи медичної допомоги, нові клінічні протоколи медичної допомоги); 8 відмічається «так» або «ні», якщо шлях введення антибактеріального препарату відповідає або не відповідає рекомендованим інструкцією виробника; 9 відмічається «так» або «ні», якщо тривалість лікування відповідає або не відповідає рекомендованій відповідно до інструкції виробника та/або медико-технологічних документів (клінічні настанови, стандарти медичної допомоги, уніфіковані клінічні протоколи медичної допомоги, нові клінічні протоколи медичної допомоги); 10 відмічається «так», якщо в медичній карті зазначено проведення лікарем аналізу/перегляду необхідності продовження/корекції антибіотикотерапії через 48 годин після її призначення, і одне з наступного: «Ескалація» (посилення), «Продовження» (антибіотикотерапія залишена без змін), «Деескалація» (послаблення), «Припинення» (відміна), «Зміна в/в на per os» (перехід на пероральний прийом одного і того ж антибіотика, в тому числі в межах групи антибіотиків) або «ні», якщо в медичній карті не зазначено проведення лікарем аналізу/перегляду необхідності продовження/корекції антибіотикотерапії через 48 годин після її призначення; 11 заповнюється, якщо переглядалась антибіотикотерапія, відмічається відповідна позиція, якщо в медичній карті зазначено, що в пацієнта наявні (зберігаються) клінічні ознаки запалення інфекційного генезу або отримано підтвердження інфекційної етіології запального процесу, причина продовження антибіотикотерапії або доповнення/пояснення в стовпчику «Інше (коментар)», якщо антибіотикотерапію продовжено, але наявні варіанти відповідей не пояснюють або в не повною мірою пояснюють подовження антибактеріальної терапії; 12 відмічається «Дата» і зазначається день, місяць і рік забору біологічного матеріалу для проведення дослідження, або відмічається «ні», якщо забір матеріалу не проводився; 13 заповнюється, якщо здійснювався забір матеріалу для мікробіологічного дослідження, відмічається «Дата» і зазначається день, місяць і рік отримання результатів мікробіологічного дослідження, або відмічається «ні», якщо мікробіологічне дослідження не було проведене (відсутній результат) з будь-яких причин; 14 заповнюється, якщо було отримано результати мікробіологічного дослідження. Як коментар лаконічно зазначається чи вплинули і, якщо так, то яким чином на призначення лікуючого лікаря отримані результати мікробіологічного дослідження — наприклад, антибактеріальний препарат замінено на антибіотик з іншої групи; 15 зазначається висновок щодо відповідності призначення антимікробних препаратів та, в разі необхідності, додаткові відомості, які не були зазначені; 16 день, місяць і рік заповнення форми/проведення аналізу; 17 прізвище, ім’я, по батькові (за наявності) та підпис клінічного провізора. |
Додаток 5
до Інструкції з впровадження адміністрування
антимікробних препаратів в закладах охорони здоров’я,
які надають медичну допомогу в стаціонарних умовах
(підпункт 4 пункту 3 розділу IV, пункт 3 розділу V)
Методика розрахунку індексу резистентності до АМП
1. Етап I — розрахунок частоти виявлення резистентних штамів певного мікроорганізму до певних груп АМП за зразком таблиці 1.
У графу «АМП» записують АМП або групу АМП, які потенційно ефективні по відношенню до збудника. В графу «Всього ізолятів» — загальну кількість штамів мікроорганізму, відносно яких проводилося визначення чутливості до відповідного АМП. В графу «Кількість резистентних ізолятів» — загальну кількість штамів, які резистентні до того ж АМП. «Частота резистентних ізолятів» розраховується як відношення кількості резистентних штамів до загальної кількості штамів вказаного патогену.
Таблиця 1. Дані мікробіологічного моніторингу
Рік |
Збудник |
АМП |
Всього ізолятів |
Кількість резистентних ізолятів |
Частота резистентних ізолятів |
1 |
2 |
3 |
4 |
5 |
6 |
2017 |
K. pneumoniae |
Аміноглікозиди |
536 |
145 |
0,27 |
Фторхінолони |
622 |
359 |
0,58 |
||
Амінопеніциліни |
636 |
601 |
0,94 |
||
Захищені пеніциліни |
636 |
588 |
0,92 |
||
Цефалоспорини I–IV покоління |
602 |
265 |
0,44 |
||
Карбапенеми |
603 |
18 |
0,03 |
||
Тигециклін |
603 |
15 |
0,02 |
||
Колістин |
603 |
0 |
0 |
||
2018 |
K. pneumoniae |
Аміноглікозиди |
625 |
301 |
0,48 |
Фторхінолони |
586 |
300 |
0,51 |
||
Амінопеніциліни |
641 |
635 |
0,99 |
||
Захищені пеніциліни |
641 |
631 |
0,98 |
||
Цефалоспорини I–IV покоління |
625 |
298 |
0,47 |
||
Карбапенеми |
625 |
25 |
0,04 |
||
Тигециклін |
625 |
11 |
0,02 |
||
Колістин |
625 |
0 |
0 |
2. Етап II — збір даних щодо споживання класів АМП, які аналізуються. З цією метою підраховується сума встановлених добових доз (далі — DDD) АМП кожного класу. Для розрахунку необхідний DDD для кожного АМП, який можна дізнатися на сайті «WHO Collaborating Center for Drug Statistics Methodology»: www.whocc.no/atc_DDD_index/.
Наприклад, для класу карбапенемів за 2017 рік використано 360 флаконів ертапенему по 1,0, 10920 флаконів меропенему по 1,0 та 2795 флаконів іміпенему/циластатиту по 0,5.
Для ертапенему DDD = 1,0 г DDD ертапенему = 360 / 1 = 360.
Для меропенему DDD = 2,0 г DDD меропенему = 10920 / 2 = 5460.
Для імепенему/циластатину DDD = 2,0 по іміпенему DDD іміпенему/циластатину = 2795 / 4 = 699.
Загальна кількість DDD для карбапенемів = 360 + 5460 + 699 = 6519.
Наступний крок — розрахунок споживання АМП на 100 ліжкоднів (далі — л/д) по формулі:
СД100 — споживання АМП на 100 л/д;
DDD — загальна кількість DDD для АМП або групи АМП;
КЛД — загальна кількість л/д;
100 — 100 л/д.
Для прикладу, в нашому випадку СД100 становить 3,38.
Загальне СД100 — сума СД100 для всіх АМП.
Дані щодо споживання вносяться за зразком таблиці 2. «Частоту споживання АМП» визначають як відношення споживання кожного класу АМП (стовпчик «СД100») до загального споживання за період часу (стовпчик загальне СД100).
Таблиця 2. Споживання антимікробних препаратів
Рік |
АМП |
СД100 |
Загальне СД100 |
Частота споживання АМП |
2017 |
Аміноглікозиди |
1,37 |
41,87 |
0,03 |
Фторхінолони |
12,3 |
0,29 |
||
Амінопеніциліни |
1,44 |
0,03 |
||
Захищені пеніциліни |
6,71 |
0,16 |
||
Цефалоспорини I–IV покоління |
16,28 |
0,39 |
||
Карбапенеми |
3,38 |
0,081 |
||
Тигециклін |
0,34 |
0,008 |
||
Колістин |
0,05 |
0 |
||
2018 |
Аміноглікозиди |
1,72 |
35,76 |
0,05 |
Фторхінолони |
10,07 |
0,28 |
||
Амінопеніциліни |
0,75 |
0,02 |
||
Захищені пеніциліни |
8,38 |
0,23 |
||
Цефалоспорини I–IV покоління |
10,14 |
0,28 |
||
Карбапенеми |
4,12 |
0,117 |
||
Тигециклін |
0,37 |
0,01 |
||
Колістин |
0,21 |
0,01 |
3. Етап III — розрахунок індексу резистентності до АМП (дані ІРАМП) за зразком таблиці 3. «АМР» — частота резистентних ізолятів помножена на частоту споживання АМП. ІРАМП — сума показників АМР до всіх АМП, що використовувалися за даний період часу.
Таблиця 3. Індекс резистентності до антимікробних препаратів
Рік |
Збудник |
АМП |
Частота резистентних ізолятів |
Частота споживання АМП |
АМР |
ІРАМП |
2017 |
K. pneumoniae |
Аміноглікозиди |
0,27 |
0,03 |
0,081 |
0,6 |
Фторхінолони |
0,58 |
0,29 |
0,168 |
|||
Амінопеніциліни |
0,94 |
0,03 |
0,028 |
|||
Захищені пеніциліни |
0,92 |
0,16 |
0,147 |
|||
Цефалоспорини I–IV покоління |
0,44 |
0,39 |
0,172 |
|||
Карбапенеми |
0,03 |
0,081 |
0,002 |
|||
Тигециклін |
0,02 |
0,008 |
0 |
|||
Колістин |
0 |
0 |
0 |
|||
2018 |
K. pneumoniae |
Аміноглікозиди |
0,48 |
0,05 |
0,024 |
0,55 |
Фторхінолони |
0,51 |
0,28 |
0,143 |
|||
Амінопеніциліни |
0,99 |
0,02 |
0,02 |
|||
Захищені пеніциліни |
0,98 |
0,23 |
0,225 |
|||
Цефалоспорини I–IV покоління |
0,47 |
0,28 |
0,132 |
|||
Карбапенеми |
0,04 |
0,117 |
0,004 |
|||
Тигециклін |
0,02 |
0,01 |
0 |
|||
Колістин |
0 |
0,01 |
0 |
4. Етап IV — інтерпретація результатів. В наведеному випадку ІРАМП у K. pneumoniae зменшився за рахунок зменшення споживання амінопеніцилінів та цефалоспоринів.
Додаток 6
до Інструкції з впровадження адміністрування
антимікробних препаратів в закладах охорони здоров’я,
які надають медичну допомогу в стаціонарних умовах
(підпункт 5 пункту 3 розділу IV)
Показники оцінки ефективності адміністрування антимікробних препаратів при стафілококовій бактеріємії
Показник |
Цільове значення |
Необхідне значення показника, % |
Час введення першої дози антибіотика після діагностики бактеріємії |
Протягом 6 годин |
95 |
Контрольне дослідження гемокультури після початку терапії |
Через 48–72 години |
100 |
Кількість негативних гемокультур для оцінки ефективності терапії |
Мінімум два |
100 |
Видалення або заміна (не по провіднику) внутрішньосудинного катетеру після діагностики бактеріємії |
Обов’язково |
95 |
Консультація клінічного провізора після виявлення бактеріємії |
В перші 48 годин |
90 |
Проведення УЗД внутрішніх органів, ЕХО-КГ і рентгенографії легень |
Діагностика ускладнень бактеріємії |
100 |
Антибактеріальна терапія при MSSA-бактеріємії |
Оксацилін або цефазолін в 1-й лінії терапії |
90 |
Антибактеріальна терапія при MRSA-бактеріємії |
Ванкоміцин або даптоміцин в 1-й лінії терапії |
90 |
Визначення МПК ванкоміцину для MRSA |
Прогнозування адекватності терапії ванкоміцином |
80 |
Дозування ванкоміцину |
Розрахунок і корекція дози у відповідності до кліренсу креатиніну |
100 |
Дозування даптоміцину по масі тіла пацієнта |
6 — 8 мг/кг |
100 |
Тривалість антибактеріальної терапії після нормалізації температури і першої негативної гемокультури |
Неускладнена бактеріємія — 14–21 день |
100 |
УЗД — ультразвукове дослідження; ЕХО-КГ — ехокардіографія; MSSA — метицилін-чутливий золотистий стафілокок; MRSA — метицилін-резистентний золотистий стафілокок. |
||
Додаток 7
до Інструкції з впровадження адміністрування
антимікробних препаратів в закладах охорони здоров’я,
які надають медичну допомогу в стаціонарних умовах
(підпункт 5 пункту 3 розділу IV)
Показники оцінки ефективності адміністрування антимікробних препаратів при проведенні периопераційної антибіотикопрофілактики
Показник |
Цільове значення |
Необхідне значення показника, % |
Частота проведення периопераційної антибіотикопрофілактики |
Антибіотикопрофілактика необхідна при «умовно чистих» і «брудних» операціях, а також при «чистих» операціях у пацієнтів з факторами ризику ускладнень. |
90 |
Час введення антибіотика |
За 30–60 хвилин до розрізу шкіри |
100 |
Антибіотик для периопераційної антибіотикопрофілактики |
Використання для профілактики цефазоліну |
близько 80 |
Використання для профілактики цефалоспорину III покоління |
0 |
|
Використання для профілактики цефуроксиму |
близько 20 |
|
Використання для профілактики ванкоміцину |
менше 5 |
|
Тривалість периопераційної антибіотикопрофілактики |
Одна периопераційна доза |
80 |
Одна периопераційна доза і одна протягом 48 годин після оперативного втручання у пацієнтів групи ризику гнійних ускладнень |
20 |
|
Понад 48 годин |
0 |
Додаток 8
до Інструкції з впровадження адміністрування
антимікробних препаратів в закладах охорони здоров’я,
які надають медичну допомогу в стаціонарних умовах
(пункт 4 розділу V)
Форма моніторингу споживання антимікробних препаратів
№ |
Антимікробний препарат |
Доза, г/мг/МО/ОД |
Кратність введення на добу |
Тривалість призначення, дні |
DDD |
Загальна кількість DDD |
Примітки:
1. В графу «Антимікробний препарат» вписується один з наступних АМП:
1) азтреонам;
2) цефтаролін фосаміл;
3) цефтазидим-авібактам;
4) цефтобіпрол медокаріл;
5) цефтолозан-тазобактам;
6) колістин;
7) далбаванцин;
8) далфопрістин-квінупрістин;
9) даптоміцин;
10) еравациклін;
11) фаропенем;
12) фосфоміцин;
13) лінезолід;
14) меропенем-ваборбактам;
15) міноциклін;
16) омадациклін;
17) орітаванцин;
18) плазоміцин;
19) поліміксин В;
20) тедізолід;
21) телаванцин;
22) тайгециклін;
23) цефтріаксон;
24) цефазолін;
25) цефуроксим;
26) меропенем;
27) ципрофлоксацин;
28) левофлоксацин;
29) моксифлоксацин.
2. В графі «Доза» вказується доза одноразового введення АМП.
3. В графі «Кратність введення на добу» вказується кратність введення АМП на добу.
4. В графі «Тривалість призначення» вказується кількість днів призначення АМП.
5. В графі «DDD» — вказується визначена добова доза для АМП відповідно до інформації на сайті «WHO Collaborating Center for Drug Statistics Methodology»: www.whocc.no/atc_DDD_index/.
6. Загальна кількість DDD зазначається після розрахунку за формулою:
Додаток 9
до Інструкції з впровадження адміністрування
антимікробних препаратів в закладах охорони здоров’я,
які надають медичну допомогу в стаціонарних умовах
(пункт 4 розділу V)
Форма спостереження та ведення обліку за споживанням антимікробних препаратів
Азтреонам |
Цефтаролін фосаміл |
Цефтазидим- |
Цефтобіпрол медокаріл |
Цефтолозан- |
Колістин |
Далбаванцин |
Далфопрістин- |
Даптоміцин |
Еравациклін |
|
Рівень загального споживання АМП1 |
||||||||||
Фаропенем |
Фосфоміцин |
Лінезолід |
Меропенем- |
Міноциклін |
Омадациклін |
Орітаванцин |
Плазоміцин |
Поліміксин В |
Тедізолід |
|
Рівень загального споживання АМП1 |
||||||||||
Телаванцин |
Тайгециклін |
Цефтріаксон |
Цефазолін |
Цефуроксим |
Меропенем |
Ципрофлоксацин |
Левофлоксацин |
Моксифлоксацин |
Меропенем |
|
Рівень загального споживання АМП1 |
||||||||||
E. coli |
K. pneumoniae |
Salmonella spp. |
P. aeruginosa |
Acinetobacter spp. |
S. aureus |
S. pneumoniae |
E. faecalis |
E. faecium |
||
Індекс резистентності до АМП2 |
||||||||||
Примітки:
____________
1 зазначається рівень споживання відповідного АМП, що розраховується за формулою: РСА = ЗКА/ЛД × 100, де РСА — рівень загального споживання окремого АМП в ЗОЗ, ЗКА — загальна кількість DDD АМП, ЛД — загальна кількість ліжкоднів, які провели пацієнти в ЗОЗ;
2 зазначається індекс резистентності до АМП відповідної бактерії, що розраховується відповідно до додатку 5 до цієї Інструкції.
ЗАТВЕРДЖЕНО
Наказ Міністерства охорони здоров’я України
03 серпня 2021 року № 1614
Зареєстровано
в Міністерстві юстиції України
11 жовтня 2021 р. за № 1323/36945
Положення про відділ з інфекційного контролю закладу охорони здоров’я та установи / закладу надання соціальних послуг / соціального захисту населення
I. Загальні положення
1. Відділ з інфекційного контролю (далі — ВІК) діє як самостійний структурний підрозділ в закладі охорони здоров’я (далі — ЗОЗ) та установах / закладах надання соціальних послуг / соціального захисту населення (далі — ЗСЗ) незалежно від форми власності та підпорядкування.
2. ВІК підпорядковується безпосередньо керівнику ЗОЗ/ЗСЗ.
3. Оснащення ВІК засобами зв’язку, комп’ютерною технікою здійснюється відповідно до функцій з профілактики інфекцій та інфекційного контролю, які виконуються ВІК.
4. ВІК у своїй діяльності керується Конституцією України, законами України, указами Президента України та постановами Верховної Ради України, прийнятими відповідно до Конституції та законів України, актами Кабінету Міністрів України, цим Положенням та іншими нормативно-правовими актами у сфері охорони здоров’я.
II. Завдання та функції ВІК
1. Основним завданням ВІК є організація профілактики інфекцій та інфекційного контролю в ЗОЗ/ЗСЗ з метою запобігання поширенню інфекційних хвороб, у тому числі пов’язаних із наданням медичної допомоги, мікроорганізмів із антимікробною резистентністю та формування культури безпеки в ЗОЗ/ЗСЗ.
2. Відповідно до покладених завдань ВІК здійснює:
1) розробку планів дій/заходів ЗОЗ/ЗСЗ на виконання нормативно-правових актів з питань профілактики інфекцій та інфекційного контролю;
2) розрахунок та обґрунтування щорічного бюджету для реалізації планів дій/заходів ЗОЗ/ЗСЗ з питань профілактики інфекцій та інфекційного контролю;
3) моніторинг, оцінку та зворотній зв’язок щодо виконання ЗОЗ/ЗСЗ та його структурними підрозділами заходів з профілактики інфекцій та інфекційного контролю, впровадження покращення гігієни рук, профілактики інфекційних хвороб, пов’язаних із наданням медичної допомоги, впровадження адміністрування антимікробних препаратів;
4) епідеміологічний нагляд та ведення обліку інфекційних хвороб в ЗОЗ/ЗСЗ в установленому законодавством порядку;
5) розповсюдження новітніх даних в області профілактики інфекцій та інфекційного контролю, підтримку культури безпеки в ЗОЗ/ЗСЗ;
6) підготовку звітів та надання консультацій для керівництва, структурних підрозділів та працівників ЗОЗ/ЗСЗ з питань профілактики інфекцій та інфекційного контролю, впровадження покращення гігієни рук, профілактики інфекційних хвороб, пов’язаних із наданням медичної допомоги, впровадження адміністрування антимікробних препаратів;
7) консультування з питань закупівлі обладнання і витратних матеріалів для ЗОЗ/ЗСЗ з метою дотримання санітарних норм і забезпечення профілактики інфекцій та інфекційного контролю;
8) розробку стандартних операційних процедур;
9) впровадження нових клінічних протоколів з емпіричної антимікробної терапії та периопераційної антибіотикопрофілактики в установленому законодавством порядку;
10) проведення ретроспективного аудиту відповідності призначення антимікробних препаратів;
11) навчання та перевірку знань працівників ЗОЗ/ЗСЗ з питань профілактики інфекцій та інфекційного контролю, покращення гігієни рук, профілактики інфекційних хвороб, пов’язаних із наданням медичної допомоги, адміністрування антимікробних препаратів;
12) подання пропозицій для керівництва ЗОЗ/ЗСЗ щодо робочого навантаження медичних працівників, укомплектування штатами і розміщення ліжок, приміщень, матеріалів та обладнання в частині забезпечення профілактики інфекцій та інфекційного контролю;
13) складання попереднього плану розслідування спалаху інфекційних хвороб, пов’язаних з наданням медичної допомоги в ЗОЗ та попередження його поширення;
14) надання даних споживання антимікробних препаратів в заклад громадського здоров’я, який реалізує заходи з боротьби з антимікробною резистентністю відповідно до адміністративно-територіальної належності;
15) просування та популяризацію заходів з профілактики інфекційних хвороб серед працівників ЗОЗ/ЗСЗ та пацієнтів/відвідувачів, співпрацю з громадськими об’єднаннями;
16) виконання заходів з інфекційного контролю за туберкульозом, відповідно до Стандарту інфекційного контролю для закладів охорони здоров’я, що надають допомогу хворим на туберкульоз, затвердженого наказом Міністерства охорони здоров’я України від 01 лютого 2019 року № 287, зареєстрованого в Міністерстві юстиції України 17 квітня 2019 року за № 408/33379;
17) інші функції, пов’язані з профілактикою інфекцій та інфекційним контролем.
III. Права та обов’язки ВІК
1. ВІК має право:
1) запитувати у адміністрації, керівників структурних підрозділів, лабораторії ЗОЗ/ЗСЗ інформацію, необхідну для виконання завдань та функцій відповідно до пунктів 1 та 2 розділу II цього Положення;
2) залучати зацікавлені сторони (представників структурних підрозділів ЗОЗ/ЗСЗ, старших сестер медичних, спеціалістів) для розробки планів дій, заходів, графіків та стандартних операційних процедур з профілактики інфекцій та інфекційного контролю;
3) проводити моніторинг та оцінку стану виконання заходів з профілактики інфекцій та інфекційного контролю працівниками структурних підрозділів ЗОЗ/ЗСЗ за графіком, погодженим із керівниками структурних підрозділів;
4) визначати процеси і практики, які підлягають моніторингу та оцінці, інструменти, за допомогою яких проводиться моніторинг та оцінка, механізми зворотного зв’язку;
5) ініціювати та проводити епідеміологічні розслідування в ЗОЗ;
6) подавати письмові пропозиції до керівництва ЗОЗ/ЗСЗ щодо тимчасової зупинки (на період карантину та проведення протиепідемічних заходів) функціонування окремих відділень ЗОЗ/ЗСЗ у зв’язку зі спалахом інфекційних захворювань серед пацієнтів та/або працівників;
7) подавати письмові пропозиції до адміністрації ЗОЗ щодо внесення коректив до проведення профілактичних та протиепідемічних заходів, спрямованих на профілактику післяопераційних інфекцій, спричинених резистентними штамами мікроорганізмів;
8) надавати висновки для допуску/не допуску до виконання своїх функціональних обов’язків нових працівників (при працевлаштуванні, після випробувального терміну) та щодо компетентності працівника за результатами оцінки знань з гігієни рук, профілактики інфекцій та інфекційного контролю;
9) брати участь у розгляді питань щодо робочого навантаження медичних працівників, укомплектування штатами і розміщення ліжок, приміщень, матеріалів та обладнання в частині забезпечення профілактики інфекцій та інфекційного контролю;
10) користуватися відповідними матеріально-технічними засобами, необхідними для виконання завдань/функцій.
2. ВІК забезпечує:
1) виконання завдань та функцій відповідно до пунктів 1 та 2 розділу II цього Положення;
2) надання оперативної інформації за запитом керівництва;
3) здійснення координації взаємодії ВІК з іншими структурними підрозділами ЗОЗ/ЗСЗ;
4) ведення документації та підготовку звітів;
5) дотримання встановленого порядку обліку матеріально-технічних засобів, цільове та дбайливе використання закріпленого за ВІК майна;
6) створення належних виробничих умов, додержання працівниками правил внутрішнього трудового розпорядку, охорони праці та протипожежної безпеки.
3. Працівники ВІК проходять регулярне навчання з питань профілактики інфекцій та інфекційного контролю з метою забезпечення виконання ними своїх функціональних обов’язків.
IV. Структура та штатний розпис ВІК
1. Структура та штатний розпис ВІК визначається в залежності від розміру і спеціалізації ЗОЗ/ЗСЗ, виду медичної допомоги та затверджуються у встановленому законодавством порядку.
2. До складу ВІК ЗОЗ, які надають медичну допомогу у стаціонарних умовах цілодобово, входять як мінімум:
1) лікар-епідеміолог (госпітальний епідеміолог);
2) помічник лікаря-епідеміолога (мінімум один на кожні 250 ліжок);
3) клінічний провізор (координатор з адміністрування антимікробних препаратів);
4) сектор з покращення гігієни рук / працівники, які виконують функції координатора з гігієни рук, його заступника, інструктора/тренера, спостерігача, спеціаліста зі збору та аналізу даних відповідно до Інструкції з впровадження покращення гігієни рук в закладах охорони здоров’я та установах / закладах надання соціальних послуг / соціального захисту населення, затвердженої наказом Міністерства охорони здоров’я України від 03 серпня 2021 року № 1614;
5) лікар будь-якої лікарської спеціальності (координатор навчання і підготовки з профілактики інфекцій та інфекційного контролю);
6) статистик.
3. В ЗСЗ та ЗОЗ, окрім визначених пунктом 2 цього розділу та фармацевтичних (аптечних) закладів, керівник ВІК виконує функції координатора з гігієни рук і до складу ВІК входять як мінімум інструктор/тренер та спеціаліст зі збору та аналізу даних.
Завдання та функції ВІК у ЗСЗ та ЗОЗ, окрім визначених пунктом 2 цього розділу, можуть виконуватися суб'єктами господарювання на умовах договору підряду.
4. Керівником ВІК в ЗОЗ, що надають цілодобову медичну допомогу в стаціонарних умовах може бути призначено особу з вищою освітою II рівня за ступенем магістра у галузі знань 22 «Охорона здоров’я», проходження інтернатури за однією зі спеціальностей медичного профілю та стажем роботи не менше трьох років.
5. Керівником ВІК в ЗСЗ та ЗОЗ, окрім визначених пунктом 2 цього розділу та фармацевтичних (аптечних) закладів, може бути призначено особу з професійною освітою (молодший спеціаліст) або вищою освітою (молодший бакалавр, бакалавр, магістр), галузь знань 22 «Охорона здоров’я», спеціальність «Медсестринство» та стажем роботи не менше трьох років, або з лікарською спеціальністю (без спеціальних вимог до стажу роботи).
6. Положення про ВІК, посадові інструкції працівників ВІК затверджуються керівником ЗОЗ/ЗСЗ.
V. Взаємодія та співпраця ВІК
1. ВІК взаємодіє та співпрацює зі структурними підрозділами, робочими групами, комісіями ЗОЗ/ЗСЗ з питань реалізації суміжних напрямів діяльності, контролю якості медичного обслуговування та мікробіологічними лабораторіями.
2. ВІК взаємодіє із регіональними закладами громадського здоров’я та готує для них інформацію та звітність у встановленому законодавством порядку.
3. ВІК взаємодіє із ЗОЗ/ЗСЗ з метою обміну досвідом щодо впровадження заходів з профілактики інфекцій та інфекційного контролю, організації спільних заходів, партнерських моніторингових візитів тощо.
4. ВІК співпрацює з громадськими об’єднаннями з метою популяризації заходів з профілактики інфекцій та інфекційного контролю.
Генеральний директор Директорату громадського здоров’я
та профілактики захворюваності
І. Руденко
ЗАТВЕРДЖЕНО
Наказ Міністерства охорони здоров’я України
03 серпня 2021 року № 1614
Зареєстровано
в Міністерстві юстиції України
11 жовтня 2021 р. за № 1324/36946
Зміни до деяких наказів Міністерства охорони здоров’я України
1. У таблиці Експертного висновку про відповідність закладу стандартам акредитації додатку до Положення про Головну акредитаційну комісію при Міністерстві охорони здоров’я України, затвердженого наказом Міністерства охорони здоров’я України від 14 березня 2011 року № 142, зареєстрованого в Міністерстві юстиції України 06 червня 2011 року за № 678/19416:
1) пункт 7 викласти в такій редакції:
«
7. Профілактика інфекцій та інфекційний контроль (335) |
||
7.1 |
0-3-5 |
|
7.2 |
0-3-5 |
|
7.3 |
0-5 |
|
7.4 |
0-3-5 |
|
7.5 |
0-3-5 |
|
7.6 |
0-3-5 |
|
7.7 |
0-3-5 |
|
7.8 |
0-3-5 |
|
7.9 |
0-3-5 |
|
7.10 |
0-3-5 |
|
7.11 |
0-3-5 |
|
7.12 |
0-5 |
|
7.13 |
0-5 |
|
7.14 |
0-5 |
|
7.15 |
0-5 |
|
7.16 |
0-5 |
|
7.17 |
0-5 |
|
7.18 |
0-3 |
|
7.19 |
0-1-3 |
|
7.20 |
0-3 |
|
7.21 |
0-5 |
|
7.22 |
0-5 |
|
7.23 |
0-5 |
|
7.24 |
0-3-5 |
|
7.25 |
0-3-5 |
|
7.26 |
0-1-3 |
|
7.27 |
0-5 |
|
7.28 |
0-3-5 |
|
7.29 |
0-3-5 |
|
7.30 |
0-5 |
|
7.31 |
0-5 |
|
7.32 |
0-5 |
|
7.33 |
0-5 |
|
7.34 |
0-5 |
|
7.35 |
0-5 |
|
7.36 |
0-2-3 |
|
7.37 |
0-1-3 |
|
7.38 |
0-2-3 |
|
7.39 |
0-3 |
|
7.40 |
0-2-3 |
|
7.41 |
0-5-10 |
|
7.42 |
0-5 |
|
7.43 |
0-3 |
|
7.44 |
0-3 |
|
7.45 |
0-2-3 |
|
7.46 |
0-3 |
|
7.47 |
0-3 |
|
7.48 |
0-3 |
|
7.49 |
0-1-3 |
|
7.50 |
0-3-5 |
|
7.51 |
0-3-5 |
|
7.52 |
0-3-5 |
|
7.53 |
0-3-5 |
|
7.54 |
0-3-5 |
|
7.55 |
0-3-5 |
|
7.56 |
0-3-5 |
|
7.57 |
0-3-5 |
|
7.58 |
0-3-5 |
|
7.59 |
0-3-5 |
|
7.60 |
0-3-5 |
|
7.61 |
0-3-5 |
|
7.62 |
0-3-5 |
|
7.63 |
0-3-5 |
|
7.64 |
0-3-5 |
|
7.65 |
0-3-5 |
|
7.66 |
0-5 |
|
7.67 |
0-3-5 |
|
7.68 |
0-3-5 |
|
7.69 |
0-3-5 |
|
7.70 |
0-3-5 |
|
7.71 |
0-5 |
|
7.72 |
0-3-5 |
|
7.73 |
0-3-5 |
|
»;
2) у пункті 10:
у назві пункту цифру «117» замінити цифрами «114»;
підпункт 10.30 виключити. У зв’язку з цим підпункти 10.31–10.36 вважати відповідно підпунктами 10.30–10.35;
3) пункт 15 викласти в такій редакції:
«
15. Хірургія, анестезіологія та інтенсивна терапія (реанімація) (89) |
||
15.1 |
0-3 |
|
15.2 |
0-3 |
|
15.3 |
0-3 |
|
15.4 |
0-3 |
|
15.5 |
0-3 |
|
15.6 |
0-3 |
|
15.7 |
0-3 |
|
15.8 |
0-3 |
|
15.9 |
0-3 |
|
15.10 |
0-3 |
|
15.11 |
0-1-3 |
|
15.12 |
0-3 |
|
15.13 |
0-3 |
|
15.14 |
0-1-3 |
|
15.15 |
0-3 |
|
15.16 |
0-3 |
|
15.17 |
0-3 |
|
15.18 |
0-3 |
|
15.19 |
0-1-3 |
|
15.20 |
0-3 |
|
15.21 |
0-1-3 |
|
15.22 |
0-1-3 |
|
15.23 |
0-1-3 |
|
15.24 |
0-1-3 |
|
15.25 |
0-1-3 |
|
15.26 |
0-1-3 |
|
15.27 |
0-1-3 |
|
15.28 |
0-1-3 |
|
15.29 |
0-3-5 |
|
»;
4) у пункті 16:
у назві пункту цифри «140» замінити цифрами «134»;
підпункт 16.17 виключити. У зв’язку з цим підпункти 16.18–16.46 вважати відповідно підпунктами 16.17–16.45;
підпункт 16.34 виключити. У зв’язку з цим підпункти 16.35–16.45 вважати відповідно підпунктами 16.34–16.44;
5) у пункті 18:
у назві пункту цифри «42» замінити цифрами «41»;
підпункт 18.5 викласти в такій редакції:
«
18.5 |
0-3-5 |
»;
підпункти 18.7, 18.8 виключити, у зв’язку з цим підпункти 18.9–18.14 вважати відповідно підпунктами 18.7–18.12;
6) у пункті 19:
у назві пункту цифри «105» замінити цифрами «102»;
підпункт 19.14 виключити. У зв’язку з цим підпункти 19.15–19.18 вважати відповідно підпунктами 19.14–19.17;
7) у пункті 24:
у назві пункту цифри «21» замінити цифрами «26»;
доповнити підпунктом 24.8 такого змісту:
24.8 |
0-5 |
2. У розділі II Стандартів акредитації закладів охорони здоров’я, затверджених наказом Міністерства охорони здоров’я України від 14 березня 2011 року № 142, зареєстрованих в Міністерстві юстиції України 06 червня 2011 року за № 680/19418:
1) главу 7 викласти в такій редакції:
«7. Профілактика інфекцій та інфекційний контроль
7.1. Наявність відділу з інфекційного контролю
0 балів |
3 бали |
5 балів |
Вид лікувально-профілактичної допомоги |
||
невідповідність |
часткова відповідність |
відповідність |
первинна |
вторинна |
третинна |
ОВ:
Н — відділ з інфекційного контролю не створений;
ЧВ — відділ з інфекційного контролю створений, але недоукомплектований кадрами та/або не затверджені посадові обов’язки/інструкції кожного із працівників та/або мінімум один із працівників відділу працює не на повний робочий день та/або підпорядкований не керівнику закладу;
В — відділ з інфекційного контролю створений та укомплектований кадрами відповідно до Положення про відділ з інфекційного контролю закладу охорони здоров’я та установи / закладу надання соціальних послуг / соціального захисту населення, затвердженого наказом Міністерства охорони здоров’я України від 03 серпня 2021 року № 1614.
7.2. В закладі охорони здоров’я, що надає стаціонарну медичну допомогу наявний лікар-епідеміолог
0 балів |
3 бали |
5 балів |
Вид лікувально-профілактичної допомоги |
|
невідповідність |
часткова відповідність |
відповідність |
вторинна |
третинна |
ОВ:
Н — лікар-епідеміолог не входить до складу відділу з інфекційного контролю закладу або працює на неповну ставку;
ЧВ — лікар-епідеміолог входить до складу відділу з інфекційного контролю закладу, працює на повну ставку, але епідеміологічні дослідження проводяться безсистемно (не аналізуються та/або не враховуються для впровадження/оцінки заходів з профілактики інфекцій та інфекційного контролю);
В — лікар-епідеміолог входить до складу відділу з інфекційного контролю закладу, працює на повну ставку, епідеміологічні дослідження проводяться системно (аналізуються та враховуються для впровадження/оцінки заходів з профілактики інфекцій та інфекційного контролю).
7.3. Наявні помічники лікаря-епідеміолога
0 балів |
5 балів |
Вид лікувально-профілактичної допомоги |
|
невідповідність |
відповідність |
вторинна |
третинна |
ОВ:
Н — помічник(и) лікаря-епідеміолога відсутній(і) або їх кількість менша ніж один на 250 ліжок закладу;
В — помічник(и) лікаря-епідеміолога наявний(і) в кількості мінімум один на 250 ліжок закладу.
7.4. Наявність річного плану дій з впровадження профілактики інфекцій та інфекційного контролю
0 балів |
3 бали |
5 балів |
Вид лікувально-профілактичної допомоги |
||
невідповідність |
часткова відповідність |
відповідність |
первинна |
вторинна |
третинна |
ОВ:
Н — річний план дій з впровадження профілактики інфекцій та інфекційного контролю відсутній або не затверджений керівником закладу або не виділено фінансування;
ЧВ — річний план дій з впровадження профілактики інфекцій та інфекційного контролю затверджений, але не адаптований під потреби і можливості (фінансові та кадрові), реалізація плану не включає мультимодальні стратегії (підхід), план не містить чітко визначених заходів та/або індикаторів;
В — річний план дій з впровадження профілактики інфекцій та інфекційного контролю затверджений керівником закладу, адаптований під потреби і можливості (фінансові та кадрові), реалізація плану включає мультимодальні стратегії (підхід), план містить чітко визначені заходи та індикатори.
7.5. Наявність довготривалого (мінімум п’ятирічного) плану дій з впровадження профілактики інфекцій та інфекційного контролю
0 балів |
3 бали |
5 балів |
Вид лікувально-профілактичної допомоги |
||
невідповідність |
часткова відповідність |
відповідність |
первинна |
вторинна |
третинна |
ОВ:
Н — довготривалий план дій з впровадження профілактики інфекцій та інфекційного контролю відсутній, розроблений менше ніж на п’ять років або не затверджений керівником закладу або не виділено фінансування;
ЧВ — довготривалий план дій з впровадження профілактики інфекцій та інфекційного контролю затверджений, але не адаптований під потреби і можливості (фінансові та кадрові), реалізація плану не включає мультимодальні стратегії (підхід), план не містить чітко визначених заходів та/або індикаторів;
В — довготривалий план дій з впровадження профілактики інфекцій та інфекційного контролю затверджений керівником закладу, адаптований під потреби і можливості (фінансові та кадрові), реалізація плану включає мультимодальні стратегії (підхід), план містить чітко визначені заходи та індикатори.
7.6. Наявність річного плану дій з впровадження покращення гігієни рук
0 балів |
3 бали |
5 балів |
Вид лікувально-профілактичної допомоги |
||
невідповідність |
часткова відповідність |
відповідність |
первинна |
вторинна |
третинна |
ОВ:
Н — річний план дій з впровадження покращення гігієни рук відсутній або не затверджений керівником закладу або не виділено фінансування;
ЧВ — річний план дій з впровадження покращення гігієни рук затверджений, але не адаптований під потреби і можливості закладу охорони здоров’я (фінансові та кадрові), реалізація плану не включає мультимодальні стратегії (підхід), план не містить чітко визначених заходів та/або індикаторів;
В — річний план дій з впровадження покращення гігієни рук затверджений керівником закладу, адаптований під потреби і можливості (фінансові та кадрові), реалізація плану включає мультимодальні стратегії (підхід), план містить чітко визначені заходи та індикатори.
7.7. Наявність довготривалого (мінімум п’ятирічного) плану дій з впровадження покращення гігієни рук
0 балів |
3 бали |
5 балів |
Вид лікувально-профілактичної допомоги |
||
невідповідність |
часткова відповідність |
відповідність |
первинна |
вторинна |
третинна |
ОВ:
Н — довготривалий план дій з впровадження покращення гігієни рук відсутній, розроблений менше ніж на п’ять років або не затверджений керівником закладу або не виділено фінансування;
ЧВ — довготривалий план дій з впровадження покращення гігієни рук затверджений, але не адаптований під потреби і можливості (фінансові та кадрові), реалізація плану не включає мультимодальні стратегії (підхід), план не містить чітко визначених заходів та/або індикаторів;
В — довготривалий план дій з впровадження покращення гігієни рук затверджений керівником закладу, адаптований під потреби і можливості (фінансові та кадрові), реалізація плану включає мультимодальні стратегії (підхід), план містить чітко визначені заходи та індикатори.
7.8. Наявність адміністрування антимікробних препаратів
0 балів |
3 бали |
5 балів |
Вид лікувально-профілактичної допомоги |
|
невідповідність |
часткова відповідність |
відповідність |
вторинна |
третинна |
ОВ:
Н — адміністрування антимікробних препаратів відсутнє або не виділено фінансування;
ЧВ — адміністрування антимікробних препаратів не адаптоване під потреби і можливості (фінансові та кадрові), реалізація не включає мультимодальні стратегії (підхід), не містить чітко визначених заходів та/або індикаторів;
В — адміністрування антимікробних препаратів адаптоване під потреби і можливості (фінансові та кадрові), реалізація включає мультимодальні стратегії (підхід), містить чітко визначені заходи та індикатори.
7.9. Наявний річний план навчання і підготовки з профілактики інфекцій та інфекційного контролю медичних працівників закладу
0 балів |
3 бали |
5 балів |
Вид лікувально-профілактичної допомоги |
||
невідповідність |
часткова відповідність |
відповідність |
первинна |
вторинна |
третинна |
ОВ:
Н — річний план навчання і підготовки відсутній/не затверджений керівником або в закладі відсутня визначена особа, відповідальна за проведення навчання і підготовки, або навчання проводиться без оцінки знань медичних працівників / якості проведеного навчання;
ЧВ — річний план навчання і підготовки затверджений керівником, наявна визначена особа, відповідальна за проведення навчання і підготовки, навчання проводиться з оцінкою знань медичних працівників / якості проведеного навчання, але до навчання залучені не всі медичні працівники;
В — річний план навчання і підготовки затверджений керівником, наявна визначена особа, відповідальна за проведення навчання і підготовки, навчання проводиться з оцінкою знань медичних працівників / якості проведеного навчання, до навчання залучені всі медичні працівники.
7.10. Наявний річний план навчання і підготовки з профілактики інфекцій та інфекційного контролю немедичних працівників закладу
0 балів |
3 бали |
5 балів |
Вид лікувально-профілактичної допомоги |
||
невідповідність |
часткова відповідність |
відповідність |
первинна |
вторинна |
третинна |
ОВ:
Н — річний план навчання і підготовки відсутній/не затверджений керівником або в закладі відсутня визначена особа, відповідальна за проведення навчання і підготовки, або навчання проводиться без оцінки знань немедичних працівників / якості проведеного навчання;
ЧВ — річний план навчання і підготовки затверджений керівником, наявна визначена особа, відповідальна за проведення навчання і підготовки, навчання проводиться з оцінкою знань немедичних працівників / якості проведеного навчання, але до навчання залучені не всі немедичні працівники;
В — річний план навчання і підготовки затверджений керівником, наявна визначена особа, відповідальна за проведення навчання і підготовки, навчання проводиться з оцінкою знань немедичних працівників / якості проведеного навчання, до навчання залучені всі немедичні працівники.
7.11. Наявні навчальні матеріали з профілактики інфекцій та інфекційного контролю для пацієнтів
0 балів |
3 бали |
5 балів |
Вид лікувально-профілактичної допомоги |
||
невідповідність |
часткова відповідність |
відповідність |
первинна |
вторинна |
третинна |
ОВ:
Н — навчальні матеріали для пацієнтів відсутні або доступні у менш ніж 50 % клінічних підрозділах або не містять мінімум одну із наступних позицій: миття рук з милом і водою, респіраторна гігієна і етикет кашлю, заходи особистої гігієни;
ЧВ — навчальні матеріали для пацієнтів доступні у менш ніж 75 % клінічних підрозділах та містять інформацію щодо миття рук з милом і водою, респіраторної гігієни і етикету кашлю, заходів особистої гігієни;
В — навчальні матеріали для пацієнтів доступні у всіх клінічних підрозділах та містять інформацію щодо миття рук з милом і водою, респіраторної гігієни і етикету кашлю, заходів особистої гігієни.
7.12. Наявність ліжок в коридорах
0 балів |
5 балів |
Вид лікувально-профілактичної допомоги |
|
невідповідність |
відповідність |
вторинна |
третинна |
ОВ:
Н — пацієнти розміщуються на ліжках, що знаходяться в коридорах;
В — пацієнти не розміщуються на ліжках, що знаходяться в коридорах.
7.13. Зайнятість ліжок в кімнатах/палатах клінічних підрозділів відповідає положенню «одне ліжко — один пацієнт»
0 балів |
5 балів |
Вид лікувально-профілактичної допомоги |
|
невідповідність |
відповідність |
вторинна |
третинна |
ОВ:
Н — положення «одне ліжко — один пацієнт» не дотримується;
В — положення «одне ліжко — один пацієнт» дотримується.
7.14. Відстань між ліжками у кімнатах/палатах клінічних підрозділів становить не менше одного метра
0 балів |
5 балів |
Вид лікувально-профілактичної допомоги |
|
невідповідність |
відповідність |
вторинна |
третинна |
ОВ:
Н — відстань між ліжками у кімнатах/палатах клінічних підрозділів становить менше одного метра;
В — відстань між ліжками у кімнатах/палатах клінічних підрозділів становить один метр і більше.
7.15. Наявність системи реагування на результати оцінки кадрових потреб на випадок надзвичайних ситуацій
0 балів |
5 балів |
Вид лікувально-профілактичної допомоги |
||
невідповідність |
відповідність |
первинна |
вторинна |
третинна |
ОВ:
Н — система реагування відсутня або не ведеться перелік працівників запасу, яких можливо залучити на випадок виникнення надзвичайної ситуації;
ЧВ — система реагування наявна та ведеться перелік працівників запасу, яких можливо залучити на випадок виникнення надзвичайної ситуації, але не визначені відповідальні особи або список контактів працівників запасу не оновлювався понад 3 роки;
В — система реагування наявна та ведеться перелік працівників запасу, яких можливо залучити на випадок виникнення надзвичайної ситуації, визначені відповідальні особи, список контактів працівників запасу оновлюється мінімум один раз на 3 роки.
7.16. Наявність системи реагування на випадки, коли кількість пацієнтів перевищує кількість ліжок
0 балів |
5 балів |
Вид лікувально-профілактичної допомоги |
|
невідповідність |
відповідність |
вторинна |
третинна |
ОВ:
Н — система реагування відсутня або не визначені відповідальні особи;
В — система реагування наявна, визначені відповідальні особи.
7.17. Наявність централізованого водопостачання
0 балів |
5 балів |
Вид лікувально-профілактичної допомоги |
||
невідповідність |
відповідність |
первинна |
вторинна |
третинна |
ОВ:
Н — проточна вода не доступна в будь-який час і в достатній кількості для всіх видів використання;
В — проточна вода доступна в будь-який час і в достатній кількості для всіх видів використання.
7.18. Наявність системи опалення
0 балів |
3 бали |
Вид лікувально-профілактичної допомоги |
||
невідповідність |
відповідність |
первинна |
вторинна |
третинна |
ОВ:
Н — система опалення відсутня;
В — система опалення наявна.
7.19. Ефективність роботи системи вентиляції
0 балів |
1 бал |
3 бали |
Вид лікувально-профілактичної допомоги |
||
невідповідність |
часткова відповідність |
відповідність |
первинна |
вторинна |
третинна |
ОВ:
Н — система вентиляції працює неефективно;
ЧВ — система вентиляції працює ефективно, але не в усіх приміщеннях;
В — система вентиляції працює ефективно.
7.20. Відповідність природного та штучного освітлення приміщень їх функціональному призначенню
0 балів |
3 бали |
Вид лікувально-профілактичної допомоги |
|
невідповідність |
відповідність |
вторинна |
третинна |
ОВ:
Н — не відповідає функціональному призначенню;
В — відповідає функціональному призначенню.
7.21. Наявність туалетів у клінічних підрозділах закладів охорони здоров’я, що надають стаціонарну медичну допомогу
0 балів |
5 балів |
Вид лікувально-профілактичної допомоги |
|
невідповідність |
відповідність |
вторинна |
третинна |
ОВ:
Н — у клінічних підрозділах кількість туалетів становить менше ніж 1 на 20 ліжок;
В — у клінічних підрозділах кількість туалетів становить 1 на 20 ліжок або більше.
7.22. Наявність туалетів у амбулаторно-поліклінічних закладах
0 балів |
5 балів |
Вид лікувально-профілактичної допомоги |
невідповідність |
відповідність |
первинна |
ОВ:
Н — у амбулаторно-поліклінічному закладі наявно менше 4 туалетів;
В — у амбулаторно-поліклінічному закладі наявні 4 туалети і більше.
7.23. Наявність електроенергії
0 балів |
5 балів |
Вид лікувально-профілактичної допомоги |
||
невідповідність |
відповідність |
первинна |
вторинна |
третинна |
ОВ:
Н — електроенергія в закладі відсутня або подається з перебоями;
В — електроенергія в закладі наявна постійно.
7.24. Наявність ізоляторів/палат індивідуального перебування для пацієнтів із аерогенними інфекційними захворюваннями
0 балів |
3 бали |
5 балів |
Вид лікувально-профілактичної допомоги |
||
невідповідність |
часткова відповідність |
відповідність |
первинна |
вторинна |
третинна |
ОВ:
Н — ізолятори/палати індивідуального перебування для пацієнтів із аерогенними інфекційними захворюваннями відсутні;
ЧВ — ізолятори/палати індивідуального перебування для пацієнтів із аерогенними інфекційними захворюваннями наявні, але не відповідають національним нормам;
В — ізолятори/палати індивідуального перебування для пацієнтів із аерогенними інфекційними захворюваннями наявні і відповідають національним нормам.
7.25. Наявність засобів індивідуального захисту
0 балів |
3 бали |
5 балів |
Вид лікувально-профілактичної допомоги |
||
невідповідність |
часткова відповідність |
відповідність |
первинна |
вторинна |
третинна |
ОВ:
Н — засоби індивідуального захисту не доступні для усіх працівників постійно або засоби індивідуального захисту не відповідають національним стандартам або не проведені розрахунки необхідної кількості для кожного з підрозділів або не забезпечено фактичну наявність з урахуванням можливої необхідності надання допомоги при надзвичайних ситуаціях;
ЧВ — засоби індивідуального захисту доступні для усіх працівників постійно, засоби індивідуального захисту відповідають національним стандартам, проведені розрахунки необхідної кількості для кожного з підрозділів, забезпечено фактичну наявність з урахуванням можливої необхідності надання допомоги при надзвичайних ситуаціях, але відсутній запас засобів індивідуального захисту мінімум на один місяць роботи;
В — засоби індивідуального захисту доступні для усіх працівників постійно, засоби індивідуального захисту відповідають національним стандартам, проведені розрахунки необхідної кількості для кожного з підрозділів, забезпечено фактичну наявність з урахуванням можливої необхідності надання допомоги при надзвичайних ситуаціях, наявний запас засобів індивідуального захисту мінімум на один місяць роботи.
7.26. Забезпечення закладу білизною, дотримання вимог щодо зберігання та якості прання білизни
0 балів |
1 бал |
3 бали |
Вид лікувально-профілактичної допомоги |
||
невідповідність |
часткова відповідність |
відповідність |
первинна |
вторинна |
третинна |
ОВ:
Н — забезпечення недостатнє, вимоги щодо зберігання та прання білизни не дотримуються;
ЧВ — забезпечення достатнє, але вимоги щодо зберігання та прання білизни не дотримуються;
В — забезпечення достатнє, вимоги щодо зберігання та прання білизни дотримуються.
7.27. Наявність ємностей для збору медичних відходів категорії А у підрозділах
0 балів |
5 балів |
Вид лікувально-профілактичної допомоги |
||
невідповідність |
відповідність |
первинна |
вторинна |
третинна |
ОВ:
Н — ємності для збору медичних відходів категорії А відсутні;
В — ємності для збору медичних відходів категорії А наявні.
7.28. Наявність ємностей для збору медичних відходів категорії В
0 балів |
3 бали |
5 балів |
Вид лікувально-профілактичної допомоги |
||
невідповідність |
часткова відповідність |
відповідність |
первинна |
вторинна |
третинна |
ОВ:
Н — ємності для збору відходів категорії В відсутні або не відповідають національним стандартам;
ЧВ — ємності для збору відходів категорії В наявні, відповідають національним стандартам, але знаходяться поза межами безпосереднього(іх) місця(ь) утворення відходів;
В — ємності для збору відходів категорії В наявні, відповідають національним стандартам і знаходяться безпосередньо в місці(ях) утворення відходів.
7.29. Наявність контейнерів для збору відходів категорії В «небезпечно гострі предмети»
0 балів |
3 бали |
5 балів |
Вид лікувально-профілактичної допомоги |
||
невідповідність |
часткова відповідність |
відповідність |
первинна |
вторинна |
третинна |
ОВ:
Н — контейнери для збору відходів категорії В «небезпечно гострі предмети» відсутні або не відповідають національним стандартам;
ЧВ — контейнери для збору відходів категорії В «небезпечно гострі предмети» наявні, відповідають національним стандартам, але знаходяться поза межами безпосереднього(іх) місця(ь) утворення відходів;
В — контейнери для збору відходів категорії В «небезпечно гострі предмети» наявні, відповідають національним стандартам і знаходяться безпосередньо в місці(ях) утворення відходів.
7.30. Наявність витяжних шаф для нейтралізації відходів категорії С у закладах, які використовують цитостатики і генотоксичні препарати
0 балів |
5 балів |
Вид лікувально-профілактичної допомоги |
|
невідповідність |
відповідність |
вторинна |
третинна |
ОВ:
Н — шафа(и) для нейтралізації відходів категорії С відсутні або не відповідають національним стандартам;
В — шафа(и) для нейтралізації відходів категорії С наявні, відповідають національним стандартам.
7.31. Наявність спеціальних ємностей (контейнери, шафи тощо) для зберігання відходів категорії D у закладах, які використовують радіоізотопи у медичних та/або наукових цілях у будь-якому агрегатному стані, що перевищують допустимі рівні, встановлені нормами радіаційної безпеки
0 балів |
5 балів |
Вид лікувально-профілактичної допомоги |
|
невідповідність |
відповідність |
вторинна |
третинна |
ОВ:
Н — ємності (контейнери, шафи тощо) для зберігання відходів категорії D відсутні або не відповідають національним стандартам;
В — ємності (контейнери, шафи тощо) для зберігання відходів категорії D наявні, відповідають національним стандартам.
7.32. Наявність договору на вивіз відходів категорії А
0 балів |
5 балів |
Вид лікувально-профілактичної допомоги |
||
невідповідність |
відповідність |
первинна |
вторинна |
третинна |
ОВ:
Н — договір на вивіз відходів категорії А відсутній;
В — договір на вивіз відходів категорії А наявний.
7.33. Наявність договору на вивіз небезпечних відходів
0 балів |
5 балів |
Вид лікувально-профілактичної допомоги |
||
невідповідність |
відповідність |
первинна |
вторинна |
третинна |
ОВ:
Н — договір на вивіз небезпечних відходів відсутній;
В — договір на вивіз небезпечних відходів наявний.
7.34. Наявність центрального стерилізаційного відділення у закладах, які надають хірургічну допомогу
0 балів |
5 балів |
Вид лікувально-профілактичної допомоги |
||
невідповідність |
відповідність |
первинна |
вторинна |
третинна |
ОВ:
Н — центральне стерилізаційне відділення відсутнє або не відповідає національним вимогам або не заключено договір щодо надання послуг із очищення, дезінфекції та стерилізації (репроцесингу) виробів медичного призначення;
В — наявне центральне стерилізаційне відділення, яке відповідає національним вимогам або заключено договір щодо надання послуг із очищення, дезінфекції та стерилізації (репроцесингу) виробів медичного призначення.
7.35. Профілактичні медичні огляди працівників закладу проводяться у відповідності до вимог законодавства
0 балів |
5 балів |
Вид лікувально-профілактичної допомоги |
||
невідповідність |
відповідність |
первинна |
вторинна |
третинна |
ОВ:
Н — вимоги не дотримуються;
В — вимоги дотримуються.
7.36. Дотримання санітарних норм і правил щодо площ та розташування приміщень закладу
0 балів |
2 бали |
3 бали |
Вид лікувально-профілактичної допомоги |
||
невідповідність |
часткова відповідність |
відповідність |
первинна |
вторинна |
третинна |
ОВ:
Н — норми і правила не дотримуються;
ЧВ — норми і правила дотримуються частково;
В — норми і правила дотримуються.
7.37. Дотримання санітарних норм і правил щодо внутрішнього оздоблення приміщень відповідно до функціонального призначення
0 балів |
1 бал |
3 бали |
Вид лікувально-профілактичної допомоги |
||
невідповідність |
часткова відповідність |
відповідність |
первинна |
вторинна |
третинна |
ОВ:
Н — внутрішнє оздоблення приміщень не відповідає їх функціональному призначенню;
ЧВ — внутрішнє оздоблення приміщень частково відповідає їх функціональному призначенню;
В — внутрішнє оздоблення приміщень відповідає їх функціональному призначенню.
7.38. Дотримання санітарних норм і правил щодо холодного та гарячого водопостачання
0 балів |
2 бали |
3 бали |
Вид лікувально-профілактичної допомоги |
||
невідповідність |
часткова відповідність |
відповідність |
первинна |
вторинна |
третинна |
ОВ:
Н — у закладі наявне лише холодне водопостачання;
ЧВ — холодне та гаряче водопостачання непостійне;
В — у закладі наявне холодне та гаряче водопостачання.
7.39. Наявність ефективної системи каналізації
0 балів |
3 бали |
Вид лікувально-профілактичної допомоги |
||
невідповідність |
відповідність |
первинна |
вторинна |
третинна |
ОВ:
Н — система каналізації неефективна та/або наявні свідчення про часті перебої в її роботі;
В — система каналізації ефективна.
7.40. Дотримання санітарних норм і правил щодо розташування харчоблоку
0 балів |
2 бали |
3 бали |
Вид лікувально-профілактичної допомоги |
||
невідповідність |
часткова відповідність |
відповідність |
первинна |
вторинна |
третинна |
ОВ:
Н — норми і правила не дотримуються;
ЧВ — норми і правила дотримуються частково;
В — норми і правила дотримуються.
7.41. Дотримання санітарних норм і правил щодо обладнання, інвентарю, посуду і тари харчоблоку
0 балів |
5 балів |
10 балів |
Вид лікувально-профілактичної допомоги |
||
невідповідність |
часткова відповідність |
відповідність |
первинна |
вторинна |
третинна |
ОВ:
Н — норми і правила не дотримуються;
ЧВ — норми і правила дотримуються частково;
В — норми і правила дотримуються.
7.42. Дотримання вимог щодо заборони організації загальних місць для прийому їжі пацієнтами в клінічних підрозділах
0 балів |
5 балів |
Вид лікувально-профілактичної допомоги |
|
невідповідність |
відповідність |
вторинна |
третинна |
ОВ:
Н — вимоги не дотримуються;
В — вимоги дотримуються.
7.43. Дотримання санітарних норм і правил щодо транспортування, приймання та зберігання харчової сировини та продуктів харчування
0 балів |
3 бали |
Вид лікувально-профілактичної допомоги |
|
невідповідність |
відповідність |
вторинна |
третинна |
ОВ:
Н — норми і правила не дотримуються;
В — норми і правила дотримуються.
7.44. Дотримання санітарних норм і правил щодо виробництва харчових продуктів у закладі
0 балів |
3 бали |
Вид лікувально-профілактичної допомоги |
|
невідповідність |
відповідність |
вторинна |
третинна |
ОВ:
Н — норми і правила не дотримуються;
В — норми і правила дотримуються.
7.45. Дотримання вимог щодо складання меню-розкладки, розробки планового меню та забезпечення хворих дієтичним харчуванням
0 балів |
2 бали |
3 бали |
Вид лікувально-профілактичної допомоги |
|
невідповідність |
часткова відповідність |
відповідність |
вторинна |
третинна |
ОВ:
Н — вимоги не дотримуються;
ЧВ — вимоги дотримуються частково;
В — вимоги дотримуються.
7.46. Дотримання вимог щодо проведення бракеражу готової продукції та відбору і зберіганню добових проб
0 балів |
3 бали |
Вид лікувально-профілактичної допомоги |
|
невідповідність |
відповідність |
вторинна |
третинна |
ОВ:
Н — вимоги не дотримуються;
В — вимоги дотримуються.
7.47. Проведення систематичного контролю за дотриманням вимог щодо постачання пацієнтам доброякісних і безпечних харчових продуктів з документальним підтвердженням
0 балів |
3 бали |
Вид лікувально-профілактичної допомоги |
|
невідповідність |
відповідність |
вторинна |
третинна |
ОВ:
Н — контроль не проводиться;
В — контроль проводиться систематично, що підтверджено документально.
7.48. Дотримання вимог щодо безпеки харчування дітей до 1 року
0 балів |
3 бали |
Вид лікувально-профілактичної допомоги |
|
невідповідність |
відповідність |
вторинна |
третинна |
ОВ:
Н — вимоги не дотримуються;
В — вимоги дотримуються.
7.49. Дотримання вимог щодо допуску до роботи працівників харчоблоку та роздавальних
0 балів |
1 бал |
3 бали |
Вид лікувально-профілактичної допомоги |
|
невідповідність |
часткова відповідність |
відповідність |
вторинна |
третинна |
ОВ:
Н — вимоги не дотримуються;
ЧВ — вимоги дотримуються частково;
В — вимоги дотримуються, працівники харчоблоку та роздавальних пройшли медичний огляд при прийомі на роботу, щоквартальні періодичні медичні огляди та щоденний огляд на наявність гнійничкових захворювань.
7.50. Наявність стандартних операційних процедур з адміністрування антимікробних препаратів і моніторингу/контролю за антимікробною резистентністю
0 балів |
3 бали |
5 балів |
Вид лікувально-профілактичної допомоги |
|
невідповідність |
часткова відповідність |
відповідність |
вторинна |
третинна |
ОВ:
Н — стандартні операційні процедури з адміністрування антимікробних препаратів і моніторингу/контролю за антимікробною резистентністю відсутні або не затверджені керівником закладу або не забезпечено їх фінансування (не забезпечена наявність антимікробних препаратів);
ЧВ — стандартні операційні процедури з адміністрування антимікробних препаратів і моніторингу/контролю за антимікробною резистентністю затверджені, але не переглядалися більше одного року;
В — стандартні операційні процедури з адміністрування антимікробних препаратів і моніторингу/контролю за антимікробною резистентністю затверджені керівником закладу і вчасно переглядаються (раз на рік).
7.51. Наявність нових клінічних протоколів емпіричної антибіотикотерапії при найбільш розповсюджених бактеріальних інфекційних хворобах
0 балів |
3 бали |
5 балів |
Вид лікувально-профілактичної допомоги |
|
невідповідність |
часткова відповідність |
відповідність |
вторинна |
третинна |
ОВ:
Н — нові клінічні протоколи емпіричної антибіотикотерапії відсутні або не затверджені керівником закладу;
ЧВ — нові клінічні протоколи емпіричної антибіотикотерапії затверджені керівником закладу, але не переглядалися більше одного року;
В — нові клінічні протоколи емпіричної антибіотикотерапії затверджені керівником закладу і вчасно переглядаються (раз на рік).
7.52. Наявність стандартних операційних процедур щодо стандартних заходів захисту
0 балів |
3 бали |
5 балів |
Вид лікувально-профілактичної допомоги |
||
невідповідність |
часткова відповідність |
відповідність |
первинна |
вторинна |
третинна |
ОВ:
Н — стандартні операційні процедури щодо стандартних заходів захисту відсутні або не затверджені керівником закладу або не внесені до плану з навчання і підготовки працівників;
ЧВ — стандартні операційні процедури щодо стандартних заходів захисту затверджені керівником закладу, внесені до плану з навчання і підготовки працівників, але обов’язковість їх дотримання працівниками не зазначена в посадових обов’язках/інструкціях;
В — стандартні операційні процедури (протоколи, алгоритми) щодо стандартних заходів захисту затверджені керівником закладу, внесені до плану з навчання і підготовки працівників, обов’язковість їх дотримання працівниками зазначена в посадових обов’язках/інструкціях.
7.53. Наявність стандартних операційних процедур щодо гігієни рук
0 балів |
3 бали |
5 балів |
Вид лікувально-профілактичної допомоги |
||
невідповідність |
часткова відповідність |
відповідність |
первинна |
вторинна |
третинна |
ОВ:
Н — стандартні операційні процедури щодо гігієни рук відсутні або не затверджені керівником закладу або не внесені до плану з навчання і підготовки працівників;
ЧВ — стандартні операційні процедури щодо гігієни рук затверджені керівником закладу, внесені до плану з навчання і підготовки працівників, але обов’язковість їх дотримання працівниками не зазначена в посадових обов’язках/інструкціях;
В — стандартні операційні процедури щодо гігієни рук затверджені керівником закладу, внесені до плану з навчання і підготовки працівників, обов’язковість їх дотримання працівниками зазначена в посадових обов’язках/інструкціях.
7.54. Наявність стандартних операційних процедур щодо контактних заходів захисту (недопущення інфікування контактним шляхом)
0 балів |
3 бали |
5 балів |
Вид лікувально-профілактичної допомоги |
||
невідповідність |
часткова відповідність |
відповідність |
первинна |
вторинна |
третинна |
ОВ:
Н — стандартні операційні процедури щодо контактних заходів захисту відсутні або не затверджені керівником закладу або не внесені до плану з навчання і підготовки працівників;
ЧВ — стандартні операційні процедури щодо контактних заходів захисту затверджені керівником закладу, внесені до плану з навчання і підготовки працівників, але обов’язковість їх дотримання працівниками не зазначена в посадових обов’язках/інструкціях;
В — стандартні операційні процедури щодо контактних заходів захисту затверджені керівником закладу, внесені до плану з навчання і підготовки працівників, обов’язковість їх дотримання працівниками зазначена в посадових обов’язках/інструкціях.
7.55. Наявність стандартних операційних процедур щодо крапельних заходів захисту (недопущення інфікування крапельним шляхом)
0 балів |
3 бали |
5 балів |
Вид лікувально-профілактичної допомоги |
||
невідповідність |
часткова відповідність |
відповідність |
первинна |
вторинна |
третинна |
ОВ:
Н — стандартні операційні процедури щодо крапельних заходів захисту відсутні або не затверджені керівником закладу або не внесені до плану з навчання і підготовки працівників;
ЧВ — стандартні операційні процедури щодо крапельних заходів захисту затверджені керівником закладу, внесені до плану з навчання і підготовки працівників, але обов’язковість їх дотримання працівниками не зазначена в посадових обов’язках/інструкціях;
В — стандартні операційні процедури щодо крапельних заходів захисту затверджені керівником закладу, внесені до плану з навчання і підготовки працівників, обов’язковість їх дотримання працівниками зазначена в посадових обов’язках/інструкціях.
7.56. Наявність стандартних операційних процедур щодо повітряних (аерогенних) заходів захисту (недопущення інфікування повітряним (аерогенним) шляхом)
0 балів |
3 бали |
5 балів |
Вид лікувально-профілактичної допомоги |
||
невідповідність |
часткова відповідність |
відповідність |
первинна |
вторинна |
третинна |
ОВ:
Н — стандартні операційні процедури щодо повітряних (аерогенних) заходів захисту відсутні або не затверджені керівником закладу або не внесені до плану з навчання і підготовки працівників;
ЧВ — стандартні операційні процедури щодо повітряних (аерогенних) заходів захисту затверджені керівником закладу, внесені до плану з навчання і підготовки працівників, але обов’язковість їх дотримання працівниками не зазначена в посадових обов’язках/інструкціях;
В — стандартні операційні процедури щодо повітряних (аерогенних) заходів захисту затверджені керівником закладу, внесені до плану з навчання і підготовки працівників, обов’язковість їх дотримання працівниками зазначена в посадових обов’язках/інструкціях.
7.57. Наявність стандартних операційних процедур щодо виявлення і боротьби із спалахами інфекційних хвороб
0 балів |
3 бали |
5 балів |
Вид лікувально-профілактичної допомоги |
||
невідповідність |
часткова відповідність |
відповідність |
первинна |
вторинна |
третинна |
ОВ:
Н — стандартні операційні процедури щодо виявлення і боротьби із спалахами інфекційних хвороб відсутні або не затверджені керівником закладу або не внесені до плану з навчання і підготовки працівників;
ЧВ — стандартні операційні процедури щодо виявлення і боротьби із спалахами інфекційних хвороб затверджені керівником закладу, внесені до плану з навчання і підготовки працівників, але обов’язковість їх дотримання працівниками не зазначена в посадових обов’язках/інструкціях;
В — стандартні операційні процедури щодо виявлення і боротьби із спалахами інфекційних хвороб затверджені керівником закладу, внесені до плану з навчання і підготовки працівників, обов’язковість їх дотримання працівниками зазначена в посадових обов’язках/інструкціях.
7.58. Наявність стандартних операційних процедур щодо профілактики катетер-асоційованих інфекцій кровотоку
0 балів |
3 бали |
5 балів |
Вид лікувально-профілактичної допомоги |
|
невідповідність |
часткова відповідність |
відповідність |
вторинна |
третинна |
ОВ:
Н — стандартні операційні процедури щодо профілактики катетер-асоційованих інфекцій кровотоку відсутні або не затверджені керівником закладу або не внесені до плану з навчання і підготовки працівників;
ЧВ — стандартні операційні процедури щодо профілактики катетер-асоційованих інфекцій кровотоку затверджені керівником закладу, внесені до плану з навчання і підготовки працівників, але обов’язковість їх дотримання працівниками не зазначена в посадових обов’язках/інструкціях;
В — стандартні операційні процедури щодо профілактики катетер-асоційованих інфекцій кровотоку затверджені керівником закладу, внесені до плану з навчання і підготовки працівників, обов’язковість їх дотримання працівниками зазначена в посадових обов’язках/інструкціях.
7.59. Наявність стандартних операційних процедур щодо профілактики нозокоміальних пневмоній
0 балів |
3 бали |
5 балів |
Вид лікувально-профілактичної допомоги |
|
невідповідність |
часткова відповідність |
відповідність |
вторинна |
третинна |
ОВ:
Н — стандартні операційні процедури щодо профілактики нозокоміальних пневмоній відсутні або не затверджені керівником закладу або не внесені до плану з навчання і підготовки працівників;
ЧВ — стандартні операційні процедури щодо профілактики нозокоміальних пневмоній затверджені керівником закладу, внесені до плану з навчання і підготовки працівників, але обов’язковість їх дотримання працівниками не зазначена в посадових обов’язках/інструкціях;
В — стандартні операційні процедури щодо профілактики нозокоміальних пневмоній затверджені керівником закладу, внесені до плану з навчання і підготовки працівників, обов’язковість їх дотримання працівниками зазначена в посадових обов’язках/інструкціях.
7.60. Наявність стандартних операційних процедур щодо профілактики катетер-асоційованих інфекцій сечовивідних шляхів
0 балів |
3 бали |
5 балів |
Вид лікувально-профілактичної допомоги |
|
невідповідність |
часткова відповідність |
відповідність |
вторинна |
третинна |
ОВ:
Н — стандартні операційні процедури щодо профілактики катетер-асоційованих інфекцій сечовивідних шляхів відсутні або не затверджені керівником закладу або не внесені до плану з навчання і підготовки працівників;
ЧВ — стандартні операційні процедури щодо профілактики катетер-асоційованих інфекцій сечовивідних шляхів затверджені керівником закладу, внесені до плану з навчання і підготовки працівників, але обов’язковість їх дотримання працівниками не зазначена в посадових обов’язках/інструкціях;
В — стандартні операційні процедури щодо профілактики катетер-асоційованих інфекцій сечовивідних шляхів затверджені керівником закладу, внесені до плану з навчання і підготовки працівників, обов’язковість їх дотримання працівниками зазначена в посадових обов’язках/інструкціях.
7.61. Наявність стандартних операційних процедур щодо профілактики передавання мікроорганізмів із множинною резистентністю до антимікробних препаратів
0 балів |
3 бали |
5 балів |
Вид лікувально-профілактичної допомоги |
|
невідповідність |
часткова відповідність |
відповідність |
вторинна |
третинна |
ОВ:
Н — стандартні операційні процедури щодо профілактики передавання мікроорганізмів із множинною резистентністю до антимікробних препаратів відсутні або не затверджені керівником закладу або не внесені до плану з навчання і підготовки працівників;
ЧВ — стандартні операційні процедури щодо профілактики передавання мікроорганізмів із множинною резистентністю до антимікробних препаратів затверджені керівником закладу, внесені до плану з навчання і підготовки працівників, але обов’язковість їх дотримання працівниками не зазначена в посадових обов’язках/інструкціях;
В — стандартні операційні процедури щодо профілактики передавання мікроорганізмів із множинною резистентністю до антимікробних препаратів затверджені керівником закладу, внесені до плану з навчання і підготовки працівників, обов’язковість їх дотримання працівниками зазначена в посадових обов’язках/інструкціях.
7.62. Наявність стандартних операційних процедур щодо очищення та дезінфекції
0 балів |
3 бали |
5 балів |
Вид лікувально-профілактичної допомоги |
||
невідповідність |
часткова відповідність |
відповідність |
первинна |
вторинна |
третинна |
ОВ:
Н — стандартні операційні процедури щодо очищення та дезінфекції відсутні або не затверджені керівником закладу або не внесені до плану з навчання і підготовки працівників;
ЧВ — стандартні операційні процедури щодо очищення та дезінфекції затверджені керівником закладу, внесені до плану з навчання і підготовки працівників, але обов’язковість їх дотримання працівниками не зазначена в посадових обов’язках/інструкціях;
В — стандартні операційні процедури щодо очищення та дезінфекції затверджені керівником закладу, внесені до плану з навчання і підготовки працівників, обов’язковість їх дотримання працівниками зазначена в посадових обов’язках/інструкціях.
7.63. Наявність стандартних операційних процедур щодо очищення, дезінфекції та стерилізації медичних виробів (репроцесингу медичних виробів)
0 балів |
3 бали |
5 балів |
Вид лікувально-профілактичної допомоги |
||
невідповідність |
часткова відповідність |
відповідність |
первинна |
вторинна |
третинна |
ОВ:
Н — стандартні операційні процедури щодо очищення, дезінфекції та стерилізації медичних виробів (репроцесингу медичних виробів) відсутні або не затверджені керівником закладу або не внесені до плану з навчання і підготовки працівників;
ЧВ — стандартні операційні процедури щодо очищення, дезінфекції та стерилізації медичних виробів (репроцесингу медичних виробів) затверджені керівником закладу, внесені до плану з навчання і підготовки працівників, але обов’язковість їх дотримання працівниками не зазначена в посадових обов’язках/інструкціях;
В — стандартні операційні процедури щодо очищення, дезінфекції та стерилізації медичних виробів (репроцесингу медичних виробів) затверджені керівником закладу, внесені до плану з навчання і підготовки працівників, обов’язковість їх дотримання працівниками зазначена в посадових обов’язках/інструкціях.
7.64. Наявність стандартних операційних процедур щодо поводження з відходами
0 балів |
3 бали |
5 балів |
Вид лікувально-профілактичної допомоги |
||
невідповідність |
часткова відповідність |
відповідність |
первинна |
вторинна |
третинна |
ОВ:
Н — стандартні операційні процедури щодо поводження з відходами відсутні або не затверджені керівником закладу або не внесені до плану з навчання і підготовки працівників;
ЧВ — стандартні операційні процедури щодо поводження з відходами затверджені керівником закладу, внесені до плану з навчання і підготовки працівників, але обов’язковість їх дотримання працівниками не зазначена в посадових обов’язках/інструкціях;
В — стандартні операційні процедури щодо поводження з відходами затверджені керівником закладу, внесені до плану з навчання і підготовки працівників, обов’язковість їх дотримання працівниками зазначена в посадових обов’язках/інструкціях.
7.65. Наявний локальний мікробіологічний моніторинг
0 балів |
3 бали |
5 балів |
Вид лікувально-профілактичної допомоги |
|
невідповідність |
часткова відповідність |
відповідність |
вторинна |
третинна |
ОВ:
Н — локальний мікробіологічний моніторинг не проводиться або проводиться періодично, через незабезпеченість/недостатню забезпеченість мікробіологічної лабораторії;
ЧВ — локальний мікробіологічний моніторинг проводиться, однак його дані не враховуються для корекції нових клінічних протоколів емпіричної антибіотикотерапії;
В — локальний мікробіологічний моніторинг проводиться і його дані враховуються для корекції нових клінічних протоколів емпіричної антибіотикотерапії.
7.66. Проводиться контроль за побічними реакціями при використанні антимікробних препаратів
0 балів |
5 балів |
Вид лікувально-профілактичної допомоги |
||
невідповідність |
відповідність |
первинна |
вторинна |
третинна |
ОВ:
Н — реєстрація та звітування щодо побічних реакцій при використанні антимікробних препаратів не проводиться;
В — реєстрація та звітування щодо побічних реакцій при використанні антимікробних препаратів здійснюються відповідно до Порядку здійснення фармаконагляду, затвердженого наказом Міністерства охорони здоров’я України від 27 грудня 2006 року № 898 (у редакції наказу Міністерства охорони здоров’я України від 26 вересня 2016 року № 996), зареєстрованого в Міністерстві юстиції України 29 січня 2007 року за № 73/13340.
7.67. Проводиться аналіз ефективності адміністрування антимікробних препаратів
0 балів |
3 бали |
5 балів |
Вид лікувально-профілактичної допомоги |
|
невідповідність |
часткова відповідність |
відповідність |
вторинна |
третинна |
ОВ:
Н — аналіз ефективності адміністрування антимікробних препаратів не проводиться;
ЧВ — аналіз ефективності адміністрування антимікробних препаратів проводиться, але не включає визначення одного з показників розповсюдженості антимікробної резистентності, індексу резистентності до антимікробних препаратів, фармакоекономічної ефективності і якості антимікробної терапії (рівень загального споживання антимікробного препарату або групи антимікробних препаратів, число курсів антимікробної терапії на одного пацієнта за одиницю часу, середня тривалість курсу антимікробної терапії за одиницю часу, кількість днів антимікробної терапії за одиницю часу, частота деескалації антимікробної терапії);
В — аналіз ефективності адміністрування антимікробних препаратів проводиться та включає визначення показників розповсюдженості антимікробної резистентності, індексу резистентності до антимікробних препаратів, фармакоекономічної ефективності і якості антимікробної терапії (рівень загального споживання антимікробного препарату або групи антимікробних препаратів, число курсів антимікробної терапії на одного пацієнта за одиницю часу, середня тривалість курсу антимікробної терапії за одиницю часу, кількість днів антимікробної терапії за одиницю часу, частота деескалації антимікробної терапії).
7.68. Проводяться моніторинг і оцінка щодо дотримання працівниками правил і практик гігієни рук
0 балів |
3 бали |
5 балів |
Вид лікувально-профілактичної допомоги |
||
невідповідність |
часткова відповідність |
відповідність |
первинна |
вторинна |
третинна |
ОВ:
Н — моніторинг і оцінка не проводяться або в закладі відсутній працівник, який проводить моніторинг і оцінку щодо дотримання працівниками правил і практик гігієни рук;
ЧВ — моніторинг і оцінка проводяться, в закладі наявний працівник, який проводить моніторинг і оцінку щодо дотримання працівниками правил і практик гігієни рук, але результати проведених моніторингу і оцінки не використовуються для удосконалення навчання і підготовки з профілактики інфекцій та інфекційного контролю;
В — моніторинг і оцінка проводяться, в закладі наявний працівник, який проводить моніторинг і оцінку щодо дотримання працівниками правил і практик гігієни рук, результати проведених моніторингу і оцінки використовуються для удосконалення навчання і підготовки з профілактики інфекцій та інфекційного контролю.
7.69. Проводяться моніторинг і оцінка щодо дотримання працівниками стандартної операційної процедури очищення і дезінфекції поверхонь
0 балів |
3 бали |
5 балів |
Вид лікувально-профілактичної допомоги |
||
невідповідність |
часткова відповідність |
відповідність |
первинна |
вторинна |
третинна |
ОВ:
Н — моніторинг і оцінка не проводяться або в закладі відсутній працівник, який проводить моніторинг і оцінку;
ЧВ — моніторинг і оцінка проводяться, в закладі наявний працівник, який проводить моніторинг і оцінку щодо дотримання працівниками стандартної операційної процедури очищення і дезінфекції поверхонь, але результати проведених моніторингу і оцінки не використовуються для удосконалення навчання і підготовки з профілактики інфекцій та інфекційного контролю;
В — моніторинг і оцінка проводяться, в закладі наявний працівник, який проводить моніторинг і оцінку щодо дотримання працівниками стандартної операційної процедури очищення і дезінфекції поверхонь, результати проведених моніторингу і оцінки використовуються для удосконалення навчання і підготовки з профілактики інфекцій та інфекційного контролю.
7.70. Проводяться моніторинг і оцінка щодо дотримання працівниками стандартної операційної процедури очищення, дезінфекції та стерилізації (репроцесингу) виробів медичного призначення
0 балів |
3 бали |
5 балів |
Вид лікувально-профілактичної допомоги |
||
невідповідність |
часткова відповідність |
відповідність |
первинна |
вторинна |
третинна |
ОВ:
Н — моніторинг і оцінка не проводяться або в закладі відсутній працівник, який проводить моніторинг і оцінку;
ЧВ — моніторинг і оцінка проводяться, в закладі наявний працівник, який проводить моніторинг і оцінку щодо дотримання працівниками стандартної операційної процедури очищення, дезінфекції та стерилізації (репроцесингу) виробів медичного призначення, але результати проведених моніторингу і оцінки не використовуються для удосконалення навчання і підготовки з профілактики інфекцій та інфекційного контролю;
В — моніторинг і оцінка проводяться, в закладі наявний працівник, який проводить моніторинг і оцінку щодо дотримання працівниками стандартної операційної процедури очищення, дезінфекції та стерилізації (репроцесингу) виробів медичного призначення, результати проведених моніторингу і оцінки використовуються для удосконалення навчання і підготовки з профілактики інфекцій та інфекційного контролю.
7.71. Проводяться моніторинг і оцінка щодо споживання/використання підрозділами закладу спиртовмісного антисептику для рук
0 балів |
5 балів |
Вид лікувально-профілактичної допомоги |
||
невідповідність |
відповідність |
первинна |
вторинна |
третинна |
ОВ:
Н — моніторинг і оцінка не проводяться або в закладі відсутній працівник, який проводить моніторинг і оцінку або результати моніторингу і оцінки не враховуються при проведенні закупівель;
В — моніторинг і оцінка проводяться, в закладі наявний працівник, який проводить моніторинг і оцінку щодо споживання/використання підрозділами спиртовмісного антисептику для рук, результати моніторингу і оцінки враховуються при проведенні закупівель.
7.72. Проводяться моніторинг і оцінка щодо дотримання працівниками стандартної операційної процедури поводження з медичними відходами
0 балів |
3 бали |
5 балів |
Вид лікувально-профілактичної допомоги |
||
невідповідність |
часткова відповідність |
відповідність |
первинна |
вторинна |
третинна |
ОВ:
Н — моніторинг і оцінка не проводяться або в закладі відсутній працівник, який проводить моніторинг і оцінку;
ЧВ — моніторинг і оцінка проводяться, в закладі наявний працівник, який проводить моніторинг і оцінку щодо дотримання працівниками стандартної операційної процедури поводження з медичними відходами, але результати проведених моніторингу і оцінки не використовуються для удосконалення навчання і підготовки з профілактики інфекцій та інфекційного контролю;
В — моніторинг і оцінка проводяться, в закладі наявний працівник, який проводить моніторинг і оцінку щодо дотримання працівниками стандартної операційної процедури поводження з медичними відходами, результати проведених моніторингу і оцінки використовуються для удосконалення навчання і підготовки з профілактики інфекцій та інфекційного контролю.
7.73. Проводяться моніторинг і оцінка щодо дотримання працівниками стандартної операційної процедури постановки та догляду за внутрішньосудинним катетером
0 балів |
3 бали |
5 балів |
Вид лікувально-профілактичної допомоги |
|
невідповідність |
часткова відповідність |
відповідність |
вторинна |
третинна |
ОВ:
Н — моніторинг і оцінка не проводяться або в закладі відсутній працівник, який проводить моніторинг і оцінку;
ЧВ — моніторинг і оцінка проводяться, в закладі наявний працівник, який проводить моніторинг і оцінку щодо дотримання працівниками стандартної операційної процедури постановки та догляду за внутрішньосудинним катетером, але результати проведених моніторингу і оцінки не використовуються для удосконалення навчання і підготовки з профілактики інфекцій та інфекційного контролю;
В — моніторинг і оцінка проводяться, в закладі наявний працівник, який проводить моніторинг і оцінку щодо дотримання працівниками стандартної операційної процедури постановки та догляду за внутрішньосудинним катетером, результати проведених моніторингу і оцінки використовуються для удосконалення навчання і підготовки з профілактики інфекцій та інфекційного контролю.»;
2) підпункт 10.30 виключити. У зв’язку з цим підпункти 10.31–10.36 вважати відповідно підпунктами 10.30–10.35;
3) пункт 15 викласти в такій редакції:
«15. Хірургія, анестезіологія та інтенсивна терапія (реанімація)
15.1. Проведення в повному обсязі обстеження хворих на планове оперативне втручання на догоспітальному етапі
0 балів |
1 бал |
3 бали |
Вид лікувально-профілактичної допомоги |
|
невідповідність |
часткова відповідність |
відповідність |
вторинна |
третинна |
ОВ:
Н — проведення обстеження не здійснюється або здійснюється не в повному обсязі;
ЧВ — проведення обстеження здійснюється в повному обсязі, за виключенням мікробіологічного обстеження (окрім пацієнтів з прогнозовано чистими операційними ранами);
В — проведення обстеження здійснюється в повному обсязі.
15.2. Наявність затвердженого розкладу усіх планових оперативних втручань із зазначенням необхідної інформації
0 балів |
3 бали |
Вид лікувально-профілактичної допомоги |
|
невідповідність |
відповідність |
вторинна |
третинна |
ОВ:
Н — відсутній затверджений розклад планових операцій або у розкладі відсутня необхідна інформація;
В — наявний розклад операцій із зазначенням необхідної інформації.
15.3. Наявність у відділенні обладнаної(го) операційної (операційного блоку)
0 балів |
3 бали |
Вид лікувально-профілактичної допомоги |
|
невідповідність |
відповідність |
вторинна |
третинна |
ОВ:
Н — операційна (операційний блок) відсутній або не обладнана(ий);
В — операційна (операційний блок) наявна(ий) та обладнана(ий).
15.4. Наявність обладнання для проведення гемотрансфузій (сироватки, приладів для визначення груп крові, обладнання для проведення необхідних проб на сумісність)
0 балів |
3 бали |
Вид лікувально-профілактичної допомоги |
|
невідповідність |
відповідність |
вторинна |
третинна |
ОВ:
Н — відсутнє або перебуває в неробочому стані;
В — наявне і перебуває в робочому стані.
15.5. Наявність у формі первинної облікової документації № 003/о «Медична карта стаціонарного хворого № ____», затвердженій наказом Міністерства охорони здоров’я України від 14 лютого 2012 року № 110 (у редакції наказу Міністерства охорони здоров’я України від 21 січня 2016 року № 29), зареєстрованій в Міністерстві юстиції України 12 лютого 2016 року за № 230/28360, формі первинної облікової документації № 097/о «Медична карта новонародженого № ____», затвердженій наказом Міністерства охорони здоров’я України від 21 січня 2016 року № 29, зареєстрованій в Міністерстві юстиції України 12 лютого 2016 року за № 233/28363, формі первинної облікової документації № 096/о «Історія вагітності та пологів № ___», затвердженій наказом Міністерства охорони здоров’я України від 21 січня 2016 року № 29, зареєстрованій в Міністерстві юстиції України 12 лютого 2016 року за № 232/28362, або у Реєстрі медичних записів, записів про направлення та рецептів в електронній системі охорони здоров’я (далі — медична карта стаціонарного хворого) запису лікаря-анестезіолога про огляд пацієнта перед оперативним втручанням
0 балів |
3 бали |
Вид лікувально-профілактичної допомоги |
|
невідповідність |
відповідність |
вторинна |
третинна |
ОВ:
Н — запис відсутній;
В — запис наявний.
15.6. Наявність інформації щодо об’єктивного стану хворого в медичній карті стаціонарного хворого огляду лікаря-анестезіолога
0 балів |
3 бали |
Вид лікувально-профілактичної допомоги |
|
невідповідність |
відповідність |
вторинна |
третинна |
ОВ:
Н — інформація відсутня;
В — інформація наявна.
15.7. Проведення аналізу результатів обстежень анестезіологом (не пізніше ніж за 12 годин) до планового оперативного втручання
0 балів |
3 бали |
Вид лікувально-профілактичної допомоги |
|
невідповідність |
відповідність |
вторинна |
третинна |
ОВ:
Н — аналіз не проводиться або проводиться після установленого терміну;
В — аналіз проводиться у встановлений термін.
15.8. Наявність післяопераційних палат для перебування хворих
0 балів |
3 бали |
Вид лікувально-профілактичної допомоги |
|
невідповідність |
відповідність |
вторинна |
третинна |
ОВ:
Н — відсутні післяопераційні палати;
В — наявні післяопераційні палати.
15.9. Здійснення лікарського контролю у післяопераційному періоді
0 балів |
3 бали |
Вид лікувально-профілактичної допомоги |
|
невідповідність |
відповідність |
вторинна |
третинна |
ОВ:
Н — контроль не здійснюється;
В — контроль здійснюється.
15.10. Проведення сестринського догляду в післяопераційному періоді
0 балів |
3 бали |
Вид лікувально-профілактичної допомоги |
|
невідповідність |
відповідність |
вторинна |
третинна |
ОВ:
Н — догляд не проводиться;
В — догляд проводиться.
15.11. Наявність стандартних операційних процедур щодо профілактики інфекцій області хірургічного втручання
0 балів |
1 бали |
3 балів |
Вид лікувально-профілактичної допомоги |
|
невідповідність |
часткова відповідність |
відповідність |
вторинна |
третинна |
ОВ:
Н — стандартні операційні процедури щодо профілактики інфекцій області хірургічного втручання відсутні або не затверджені керівником закладу або не внесені до плану з навчання і підготовки працівників;
ЧВ — стандартні операційні процедури щодо профілактики інфекцій області хірургічного втручання затверджені керівником закладу, внесені до плану з навчання і підготовки працівників, але обов’язковість їх дотримання працівниками не зазначена в посадових обов’язках/інструкціях;
В — стандартні операційні процедури щодо профілактики інфекцій області хірургічного втручання затверджені керівником закладу, внесені до плану з навчання і підготовки працівників, обов’язковість їх дотримання працівниками зазначена в посадових обов’язках/інструкціях.
15.12. Наявність інформації щодо результатів патогістологічних та цитологічних досліджень видалених тканин у медичний карті стаціонарного хворого із зазначенням дати і номера дослідження, прізвищ виконавців, а також у витягу із медичної карти (якщо була виконана експрес-біопсія під час операції, то результат заноситься до протоколу операції)
0 балів |
3 бали |
Вид лікувально-профілактичної допомоги |
|
невідповідність |
відповідність |
вторинна |
третинна |
ОВ:
Н — інформація відсутня або наявна не в усіх випадках;
В — інформація наявна у всіх випадках.
15.13. Проведення оперативного втручання у призначений час
0 балів |
3 бали |
Вид лікувально-профілактичної допомоги |
|
невідповідність |
відповідність |
вторинна |
третинна |
ОВ:
Н — не проводяться або такі випадки не розбираються, причини не встановлюються;
В — проводяться, у разі непроведення кожен такий випадок детально розбирається, розробляються заходи для попередження такого в майбутньому.
15.14. Наявність стандартних операційних процедур підготовки пацієнта до оперативного втручання
0 балів |
1 бали |
3 балів |
Вид лікувально-профілактичної допомоги |
|
невідповідність |
часткова відповідність |
відповідність |
вторинна |
третинна |
ОВ:
Н — стандартні операційні процедури підготовки пацієнта до оперативного втручання відсутні або не затверджені керівником закладу або не внесені до плану з навчання і підготовки працівників;
ЧВ — стандартні операційні процедури підготовки пацієнта до оперативного втручання затверджені керівником закладу, внесені до плану з навчання і підготовки працівників, але обов’язковість їх дотримання працівниками не зазначена в посадових обов’язках/інструкціях;
В — стандартні операційні процедури підготовки пацієнта до оперативного втручання затверджені керівником закладу, внесені до плану з навчання і підготовки працівників, обов’язковість їх дотримання працівниками зазначена в посадових обов’язках/інструкціях.
15.15. Дотримання терміну перебування оперованого хворого в післяопераційній палаті
0 балів |
3 бали |
Вид лікувально-профілактичної допомоги |
|
невідповідність |
відповідність |
вторинна |
третинна |
ОВ:
Н — не дотримується або такі випадки не розбираються, причини не встановлюються;
В — дотримується, у разі недотримання кожен такий випадок детально розбирається, розробляються заходи для попередження такого в майбутньому.
15.16. Проведення повторних оперативних втручань (за винятком запланованих)
0 балів |
3 бали |
Вид лікувально-профілактичної допомоги |
|
невідповідність |
відповідність |
вторинна |
третинна |
ОВ:
Н — випадки проведення повторних оперативних втручань не розбираються, причини не встановлюються;
В — випадки проведення повторних оперативних втручань детально розбираються, розробляються заходи для попередження такого в майбутньому.
15.17. Наявність післяопераційних ускладнень (інфаркт міокарда, кровотеча, гематома, пневмонія, тромбоемболія легеневої артерії, інсульт тощо)
0 балів |
3 бали |
Вид лікувально-профілактичної допомоги |
|
невідповідність |
відповідність |
вторинна |
третинна |
ОВ:
Н — випадки не розбираються, причини не встановлюються;
В — кожен такий випадок детально розбирається, розробляються заходи для попередження такого в майбутньому.
15.18. Наявність летальних випадків як наслідків оперативного втручання
0 балів |
3 бали |
Вид лікувально-профілактичної допомоги |
|
невідповідність |
відповідність |
вторинна |
третинна |
ОВ:
Н — випадки не розбираються, причини не встановлюються;
В — кожен такий випадок детально розбирається, розробляються заходи для попередження такого в майбутньому.
15.19. Наявність у відділенні інтенсивної терапії медичного обладнання, у тому числі лабораторного, відповідно до табеля матеріально-технічного оснащення
0 балів |
1 бал |
3 бали |
Вид лікувально-профілактичної допомоги |
|
невідповідність |
часткова відповідність |
відповідність |
вторинна |
третинна |
ОВ:
Н — відсутнє;
ЧВ — обладнання наявне, але не в повному обсязі або в неробочому стані;
В — наявне в повному обсязі.
15.20. Проведення заходів щодо знеболення при проведенні оперативних втручань у дітей
0 балів |
3 бали |
Вид лікувально-профілактичної допомоги |
|
невідповідність |
відповідність |
вторинна |
третинна |
ОВ:
Н — проведення знеболювання у менше ніж 90% випадків;
В — проведення знеболювання у більше ніж 90% випадків.
15.21. Наявність стандартних операційних процедур профілактики вентилятор-асоційованої пневмонії
0 балів |
1 бали |
3 балів |
Вид лікувально-профілактичної допомоги |
|
невідповідність |
часткова відповідність |
відповідність |
вторинна |
третинна |
ОВ:
Н — стандартні операційні процедури профілактики вентилятор-асоційованої пневмонії відсутні або не затверджені керівником закладу або не внесені до плану з навчання і підготовки працівників;
ЧВ — стандартні операційні процедури профілактики вентилятор-асоційованої пневмонії затверджені керівником закладу, внесені до плану з навчання і підготовки працівників, але обов’язковість їх дотримання працівниками не зазначена в посадових обов’язках/інструкціях;
В — стандартні операційні процедури профілактики вентилятор-асоційованої пневмонії затверджені керівником закладу, внесені до плану з навчання і підготовки працівників, обов’язковість їх дотримання працівниками зазначена в посадових обов’язках/інструкціях.
15.22. Наявність стандартних операційних процедур постановки центральних судинних катетерів
0 балів |
1 бали |
3 балів |
Вид лікувально-профілактичної допомоги |
|
невідповідність |
часткова відповідність |
відповідність |
вторинна |
третинна |
ОВ:
Н — стандартні операційні процедури постановки центральних судинних катетерів відсутні або не затверджені керівником закладу або не внесені до плану з навчання і підготовки працівників;
ЧВ — стандартні операційні процедури постановки центральних судинних катетерів затверджені керівником закладу, внесені до плану з навчання і підготовки працівників, але обов’язковість їх дотримання працівниками не зазначена в посадових обов’язках/інструкціях;
В — стандартні операційні процедури постановки центральних судинних катетерів затверджені керівником закладу, внесені до плану з навчання і підготовки працівників, обов’язковість їх дотримання працівниками зазначена в посадових обов’язках/інструкціях.
15.23. Наявність стандартних операційних процедур інтубації трахеї
0 балів |
1 бали |
3 балів |
Вид лікувально-профілактичної допомоги |
|
невідповідність |
часткова відповідність |
відповідність |
вторинна |
третинна |
ОВ:
Н — стандартні операційні процедури інтубації трахеї відсутні або не затверджені керівником закладу або не внесені до плану з навчання і підготовки працівників;
ЧВ — стандартні операційні процедури інтубації трахеї затверджені керівником закладу, внесені до плану з навчання і підготовки працівників, але обов’язковість їх дотримання працівниками не зазначена в посадових обов’язках/інструкціях;
В — стандартні операційні процедури інтубації трахеї затверджені керівником закладу, внесені до плану з навчання і підготовки працівників, обов’язковість їх дотримання працівниками зазначена в посадових обов’язках/інструкціях.
15.24. Проводяться моніторинг і оцінка щодо дотримання працівниками стандартних операційних процедур профілактики інфекцій області хірургічного втручання
0 балів |
1 бали |
3 балів |
Вид лікувально-профілактичної допомоги |
||
невідповідність |
часткова відповідність |
відповідність |
первинна |
вторинна |
третинна |
ОВ:
Н — моніторинг і оцінка не проводяться або в закладі відсутній працівник, який проводить моніторинг і оцінку щодо дотримання працівниками стандартних операційних процедур профілактики інфекцій області хірургічного втручання;
ЧВ — моніторинг і оцінка проводяться, в закладі наявний працівник, який проводить моніторинг і оцінку щодо дотримання працівниками стандартних операційних процедур профілактики інфекцій області хірургічного втручання, але результати проведених моніторингу і оцінки не використовуються для удосконалення навчання і підготовки з профілактики інфекцій та інфекційного контролю;
В — моніторинг і оцінка проводяться, в закладі наявний працівник, який проводить моніторинг і оцінку щодо дотримання працівниками стандартних операційних процедур профілактики інфекцій області хірургічного втручання, результати проведених моніторингу і оцінки використовуються для удосконалення навчання і підготовки з профілактики інфекцій та інфекційного контролю.
15.25. Проводяться моніторинг і оцінка щодо дотримання працівниками стандартних операційних процедур підготовки пацієнта до оперативного втручання
0 балів |
1 бали |
3 балів |
Вид лікувально-профілактичної допомоги |
||
невідповідність |
часткова відповідність |
відповідність |
первинна |
вторинна |
третинна |
ОВ:
Н — моніторинг і оцінка не проводяться або в закладі відсутній працівник, який проводить моніторинг і оцінку щодо дотримання працівниками стандартних операційних процедур підготовки пацієнта до оперативного втручання;
ЧВ — моніторинг і оцінка проводяться, в закладі наявний працівник, який проводить моніторинг і оцінку щодо дотримання працівниками стандартних операційних процедур підготовки пацієнта до оперативного втручання, але результати проведених моніторингу і оцінки не використовуються для удосконалення навчання і підготовки з профілактики інфекцій та інфекційного контролю;
В — моніторинг і оцінка проводяться, в закладі наявний працівник, який проводить моніторинг і оцінку щодо дотримання працівниками стандартних операційних процедур підготовки пацієнта до оперативного втручання, результати проведених моніторингу і оцінки використовуються для удосконалення навчання і підготовки з профілактики інфекцій та інфекційного контролю.
15.26. Проводяться моніторинг і оцінка щодо дотримання працівниками стандартних операційних процедур профілактики вентилятор-асоційованої пневмонії
0 балів |
1 бали |
3 балів |
Вид лікувально-профілактичної допомоги |
||
невідповідність |
часткова відповідність |
відповідність |
первинна |
вторинна |
третинна |
ОВ:
Н — моніторинг і оцінка не проводяться або в закладі відсутній працівник, який проводить моніторинг і оцінку щодо дотримання працівниками стандартних операційних процедур профілактики вентилятор-асоційованої пневмонії;
ЧВ — моніторинг і оцінка проводяться, в закладі наявний працівник, який проводить моніторинг і оцінку щодо дотримання працівниками стандартних операційних процедур профілактики вентилятор-асоційованої пневмонії, але результати проведених моніторингу і оцінки не використовуються для удосконалення навчання і підготовки з профілактики інфекцій та інфекційного контролю;
В — моніторинг і оцінка проводяться, в закладі наявний працівник, який проводить моніторинг і оцінку щодо дотримання працівниками стандартних операційних процедур профілактики вентилятор-асоційованої пневмонії, результати проведених моніторингу і оцінки використовуються для удосконалення навчання і підготовки з профілактики інфекцій та інфекційного контролю.
15.27. Проводяться моніторинг і оцінка щодо дотримання працівниками стандартних операційних процедур постановки центральних судинних катетерів
0 балів |
1 бали |
3 балів |
Вид лікувально-профілактичної допомоги |
||
невідповідність |
часткова відповідність |
відповідність |
первинна |
вторинна |
третинна |
ОВ:
Н — моніторинг і оцінка не проводяться або в закладі відсутній працівник, який проводить моніторинг і оцінку щодо дотримання працівниками стандартних операційних процедур постановки центральних судинних катетерів;
ЧВ — моніторинг і оцінка проводяться, в закладі наявний працівник, який проводить моніторинг і оцінку щодо дотримання працівниками стандартних операційних процедур постановки центральних судинних катетерів, але результати проведених моніторингу і оцінки не використовуються для удосконалення навчання і підготовки з профілактики інфекцій та інфекційного контролю;
В — моніторинг і оцінка проводяться, в закладі наявний працівник, який проводить моніторинг і оцінку щодо дотримання працівниками стандартних операційних процедур постановки центральних судинних катетерів, результати проведених моніторингу і оцінки використовуються для удосконалення навчання і підготовки з профілактики інфекцій та інфекційного контролю.
15.28. Проводяться моніторинг і оцінка щодо дотримання працівниками стандартних операційних процедур інтубації трахеї
0 балів |
1 бали |
3 балів |
Вид лікувально-профілактичної допомоги |
||
невідповідність |
часткова відповідність |
відповідність |
первинна |
вторинна |
третинна |
ОВ:
Н — моніторинг і оцінка не проводяться або в закладі відсутній працівник, який проводить моніторинг і оцінку щодо дотримання працівниками стандартних операційних процедур інтубації трахеї;
ЧВ — моніторинг і оцінка проводяться, в закладі наявний працівник, який проводить моніторинг і оцінку щодо дотримання працівниками стандартних операційних процедур інтубації трахеї, але результати проведених моніторингу і оцінки не використовуються для удосконалення навчання і підготовки з профілактики інфекцій та інфекційного контролю;
В — моніторинг і оцінка проводяться, в закладі наявний працівник, який проводить моніторинг і оцінку щодо дотримання працівниками стандартних операційних процедур інтубації трахеї, результати проведених моніторингу і оцінки використовуються для удосконалення навчання і підготовки з профілактики інфекцій та інфекційного контролю.
15.29. Наявність припливно-витяжної з механічним спонуканням вентиляції у операційній
0 балів |
3 бали |
5 балів |
Вид лікувально-профілактичної допомоги |
||
невідповідність |
часткова відповідність |
відповідність |
первинна |
вторинна |
третинна |
ОВ:
Н — вентиляційна система відсутня або в неробочому стані;
ЧВ — вентиляційна система в робочому стані, але не проводиться технічне обслуговування або не перевіряється щороку відповідність вимогам інфекційного контролю (кратність повітрообміну по витяжці, напрямок руху повітря, стан фільтрів) або не проведено розрахунок вартості експлуатації або відсутня проектна документація та/або бюджет на експлуатацію механічної вентиляції;
В — вентиляційна система в робочому стані, проводиться технічне обслуговування, перевіряється щороку відповідність вимогам інфекційного контролю (кратність повітрообміну по витяжці, напрямок руху повітря, стан фільтрів), проведено розрахунок вартості експлуатації, наявні проектна документація та бюджет на експлуатацію механічної вентиляції.«;
4) у пункті 16:
підпункт 16.17 виключити. У зв’язку з цим підпункти 16.18–16.46 вважати відповідно підпунктами 16.17–16.45;
підпункт 16.33 виключити. У зв’язку з цим підпункти 16.34–16.45 вважати відповідно пунктами 16.33–16.44;
5) у пункті 18:
підпункт 18.5 викласти в такій редакції:
«18.5 Наявність припливно-витяжної з механічним спонуканням вентиляції у рентгенологічному кабінеті
0 балів |
3 бали |
5 балів |
Вид лікувально-профілактичної допомоги |
||
невідповідність |
часткова відповідність |
відповідність |
первинна |
вторинна |
третинна |
ОВ:
Н — вентиляційна система відсутня або в неробочому стані;
ЧВ — вентиляційна система в робочому стані, але не проводиться технічне обслуговування або не перевіряється щороку відповідність вимогам інфекційного контролю (кратність повітрообміну по витяжці, організований витяг повітря із верхньої та нижньої зон приміщення, напрямок руху повітря, стан фільтрів) або не проведено розрахунок вартості експлуатації або відсутня проектна документація та/або бюджет на експлуатацію механічної вентиляції;
В — вентиляційна система в робочому стані, проводиться технічне обслуговування, перевіряється щороку відповідність вимогам інфекційного контролю (кратність повітрообміну по витяжці, організований витяг повітря із верхньої та нижньої зон приміщення, напрямок руху повітря, стан фільтрів), проведено розрахунок вартості експлуатації, наявні проектна документація та бюджет на експлуатацію механічної вентиляції.»;
підпункти 18.7, 18.8 виключити. У зв’язку з цим підпункти 18.9–18.14 вважати відповідно підпунктами 18.7–18.12;
6) підпункт 19.14 пункту 19 виключити. У зв’язку з цим підпункти 19.15–19.18 вважати відповідно підпунктами 19.14–19.17;
7) пункт 24 доповнити новим підпунктом 24.8 такого змісту:
«24.8 Наявність у центрі трансплантації кісткового мозку палат захисної ізоляції пацієнтів
0 балів |
5 балів |
Вид лікувально-профілактичної допомоги |
невідповідність |
відповідність |
третинна |
ОВ:
Н — відсутні або наявні в недостатній кількості (відповідно до розрахункової потреби);
В — наявні в достатній кількості (відповідно до розрахункової потреби).»;
8) підпункт 27.10 пункту 27 викласти у такій редакції:
«27.10. Дотримання вимог інфекційного контролю за туберкульозом відповідно до Стандарту інфекційного контролю для закладів охорони здоров’я, що надають допомогу хворим на туберкульоз, затвердженого наказом Міністерства охорони здоров’я України від 01 лютого 2019 року № 287, зареєстрованого в Міністерстві юстиції України 17 квітня 2019 року за № 408/33379.
0 балів |
3 бали |
Вид лікувально-профілактичної допомоги |
||
невідповідність |
відповідність |
первинна |
вторинна |
третинна |
ОВ:
Н — вимоги не дотримуються;
В — вимоги дотримуються.».
3. Пункт 1.3 розділу 1 Державних санітарних норм та правил «Гігієнічні вимоги до розміщення, облаштування, обладнання та експлуатації перинатальних центрів», затверджених наказом Міністерства охорони здоров’я України від 26 січня 2012 року № 55, зареєстрованих в Міністерстві юстиції України 20 лютого 2012 року за № 248/20561, викласти у такій редакції:
«1.3. Заходи профілактики інфекцій та інфекційного контролю здійснюються відповідно до Порядку впровадження профілактики інфекцій та інфекційного контролю в закладах охорони здоров’я, які надають медичну допомогу в стаціонарних умовах, затвердженого наказом Міністерства охорони здоров’я України від 03 серпня 2021 року № 1614, Інструкції з впровадження покращення гігієни рук в закладах охорони здоров’я та установах / закладах надання соціальних послуг / соціального захисту населення, затвердженої наказом Міністерства охорони здоров’я України від 03 серпня 2021 року № 1614, Порядку профілактики інфекційних хвороб, пов’язаних з наданням медичної допомоги, в закладах охорони здоров’я, які надають медичну допомогу в стаціонарних умовах, затвердженого наказом Міністерства охорони здоров’я України від 03 серпня 2021 року № 1614, Порядку здійснення епідеміологічного нагляду та ведення обліку інфекційних хвороб, пов’язаних з наданням медичної допомоги, затвердженого наказом Міністерства охорони здоров’я України від 03 серпня 2021 року № 1614, Інструкції з впровадження адміністрування антимікробних препаратів в закладах охорони здоров’я, які надають медичну допомогу в стаціонарних умовах, затвердженої наказом Міністерства охорони здоров’я України від 03 серпня 2021 року № 1614, Заходів та Засобів щодо попередження інфікування при проведенні догляду за пацієнтами, затверджених наказом Міністерства охорони здоров’я України від 03 серпня 2020 року № 1777, зареєстрованих в Міністерстві юстиції України 10 листопада 2020 року за № 1110/35393.»
4. Форму первинної облікової документації № 008/о «Журнал запису оперативних втручань у стаціонарі», затверджену наказом Міністерства охорони здоров’я України від 14 лютого 2012 року № 110, зареєстровану в Міністерстві юстиції України 28 квітня 2012 року за № 661/20974, викласти у такій редакції:
«ЗАТВЕРДЖЕНО
Наказ Міністерства охорони здоров’я України
14 лютого 2012 року № 110
(в редакції наказу Міністерства охорони здоров’я України
від 03 серпня 2021 року № 1614)
Найменування міністерства, іншого органу виконавчої влади, підприємства, установи, організації, до сфери управління якого належить заклад охорони здоров’я Найменування та місцезнаходження (повна поштова адреса) закладу охорони здоров’я, де заповнюється форма Код за ЄДРПОУ |__|__|__|__|__|__|__|__| |
МЕДИЧНА ДОКУМЕНТАЦІЯ |
|
Форма первинної облікової документації ЗАТВЕРДЖЕНО |__|__|__|__|__|__|__| № |__|__|__|__| |
||
ЖУРНАЛ |
||
Розпочато «___» ________ 20__ року |
Завершено «___» ________ 20__ року__ |
|
Операція № ___________ |
||
від |__|___|___|___|___|___| |
||
1. Прізвище, ім’я, по батькові хворого (за наявності) 2. Хірург ________________________________ 3. Анестезіолог _____________________________ 4. Діагноз до операції ______________________ 5. Вид анестезії ________________________ |
7. Медична карта стаціонарного 8. Асистенти _________________________ 9. Сестра медична операційна 10. Сестра медична-анестезист |
|
6. Діагноз після операції _______________________________________________________________ __________________________________________________________________________________________ |
||
11. Контрольний список дій щодо безпеки в операційній |
||
11.1. До початку анестезії |
11.2. До розрізу шкіри |
11.3. До того як пацієнт покине операційну |
11.1.1. Місце оперативного втручання марковане 11.1.2. Проведено перевірку обладнання та лікарських засобів для анестезії 11.1.3. Пульсоксиметр, капнограф, ЕКГ-електроди та манжетка тонометра та температурні датчики зафіксовані на пацієнтові і правильно функціонують 11.1.4. Уточнено наявність у пацієнта: Складних дихальних шляхів або ризик аспірації |
11.2.1. |__| Всі члени операційної бригади представилися по імені і назвали свою роль 11.2.2. |__| Підтверджено процедуру і місце, де буде проведено розріз 11.2.3. Проведено антимікробну профілактику за 60 хв (або за дві години, якщо використовувався ванкоміцин) 11.2.4. Очікувані критичні події попередньо обговорено Зі сторони хірурга: Зі сторони анестезіолога: Зі сторони операційних медичних сестер: 11.2.5. Візуалізація необхідних зображень забезпечена |
11.3.1. Хірург / сестра медична операційна: 11.3.2. Хірург та анестезіолог: Сестра медична-анестезист: |
12. ОПИС ОПЕРАТИВНОГО ВТРУЧАННЯ |
Опис препарату (видаленого органа, частини органа) |
Підпис хірурга ____________________ |
».
5. Інструкцію щодо заповнення форми первинної облікової документації № 008/о «Журнал запису оперативних втручань у стаціонарі», затверджену наказом Міністерства охорони здоров’я України від 14 лютого 2012 року № 110, зареєстровану в Міністерстві юстиції України 28 квітня 2012 року за № 665/20978, викласти у такій редакції:
«ЗАТВЕРДЖЕНО
Наказ Міністерства охорони здоров’я України
14 лютого 2012 року № 110
(в редакції наказу Міністерства охорони здоров’я України
від 03 серпня 2021 року № 1614)
Інструкція щодо заповнення форми первинної облікової документації № 008/о «Журнал запису оперативних втручань у стаціонарі»
1. Ця Інструкція визначає порядок заповнення форми первинної облікової документації № 008/о «Журнал запису оперативних втручань у стаціонарі» (далі — форма № 008/о).
2. У формі № 008/о реєструються всі оперативні втручання, які проведені в стаціонарі.
3. На кожне оперативне втручання відводиться окремий листок, у якому вказуються прізвище, ім’я, по батькові (за наявності) хворого (пункт 1), прізвище та ім’я хірурга (пункт 2), анестезіолога (пункт 3), діагноз до операції (пункт 4), вид анестезії, що застосовувалась (пункт 5), діагноз після операції (пункт 6), а також зазначаються номер медичної карти стаціонарного хворого (пункт 7), прізвища та імена асистентів (пункт 8) прізвище та ім’я сестри медичної операційної (пункт 9), прізвище та ім’я сестри медичної-анестезиста (пункт 10), виконання контрольного списку дій щодо безпеки в операційній (пункт 11) та опис операції (пункт 12).
4. У пункті 11 форми 008/о підпункти 11.1., 11.2. та 11.3. заповнюються у послідовності, що відповідає послідовності проведення оперативного втручання: до початку анестезії, до розрізу шкіри та до того, як пацієнт покине операційну. Медичною сестрою-анестезистом усно перевіряється та послідовно підтверджується виконання кожного із підпунктів, перш ніж операційна бригада переходить до наступних дій.
Підтвердження виконання підпунктів відмічається позначками «V» або «+», якщо підпункт не виконано — позначка не ставиться.
5. Підпункт 11.1 заповнюється за обов’язкової присутності щонайменше анестезіолога:
1) у підпункті 11.1.1 відмічається «так», якщо місце оперативного втручання марковане, або «не застосовується», якщо оперативне втручання не потребує маркування місця первинного розрізу шкіри;
2) у підпункті 11.1.2 відмічається «так», якщо анестезіолог усно підтвердив проведення формальної інспекції необхідних протягом операції обладнання для проведення анестезії, дихального контуру та медичних виробів (включно з лікарськими засобами, які використовуються для надання невідкладної медичної допомоги). У випадку, якщо підпункт не виконано, переходити до наступних дій забороняється;
3) у підпункті 11.1.3 відмічається «так», якщо пульсоксиметр, капнограф, ЕКГ-електроди, манжетка тонометра та температурні датчики зафіксовані на пацієнтові і правильно функціонують. Дані вимірювань пульсоксиметра (ступінь насичення гемоглобіну артеріальної крові киснем, частота пульсу та плетизмограма), капнографа (парціальний тиск CO2 в кінці видиху пацієнта (EtCO2) та частота дихання, за умови проведення загальної анестезії чи глибокої седації), ЕКГ-монітора (відображення електричної активності серця в режимі реально часу у кількох суміжних відведеннях), тонометра (велична артеріального тиску в мм. рт. ст., що виміряна неінвазивно (інвазивно при наявності показів для цього), температурних датчиків (температура ядра тіла) виведені на монітор, який візуально доступний анестезіологу і сестрі медичній-анестезисту, а також ввімкнена звукова система оповіщення щодо досягнення критичних показників. У випадку, якщо цей підпункт не виконано, переходити до наступних дій забороняється;
4) у підпункті 11.1.4 уточняється наявність у пацієнта алергії, ознак, які дозволяють запідозрити наявність складних дихальних шляхів, тяжкої інтубації або ризику аспірації, ризику крововтрати більше 500 мл (більше 7 мл/кг у дітей). У разі їх відсутності відмічається «ні», у разі наявності відмічається «так».
У разі якщо у пацієнта наявні ознаки складних дихальних шляхів, тяжкої інтубації або ризику аспірації, але анестезіолог не підтвердив наявність всього необхідного обладнання та/або лікарських засобів для надання медичної допомоги в разі настання критичних/невідкладних станів з боку дихальної системи, переходити до наступних дій забороняється.
У разі, якщо у пацієнта наявний ризик крововтрати більше 500 мл для дорослих або більше 7 мл/кг для дітей, але анестезіолог не підтвердив наявності всього необхідного для надання медичної допомоги в разі крововтрати, переходити до наступних дій забороняється.
6. Підпункт 11.2 заповнюється за обов’язкової присутності щонайменше хірурга, сестри медичної операційної, сестри медичної-анестезиста та анестезіолога:
1) у підпункті 11.2.1 підтверджується, що всі члени операційної бригади представилися по імені і назвали свою роль, або що всі члени операційної бригади знайомі і знають ролі кожного члена бригади. У разі невиконання цього підпункту, переходити до наступних дій забороняється;
2) у підпункті 11.2.2 відмічається про підтвердження процедури і місця, де буде проведено розріз. У разі невиконання цього підпункту, переходити до наступних дій забороняється;
3) у підпункті 11.2.3 відмічається «так», якщо антибактеріальний лікарський засіб з метою профілактики було введено пацієнту за 60 хвилин, які передували оперативному втручанню або, якщо пацієнту було введено ванкоміцин, за дві години, які передували оперативному втручанню. У разі якщо антибіотикопрофілактику було проведено більше ніж за 60 хвилин до первинного розрізу (двох годин для ванкоміцину), переходити до оперативного втручання заборонено до повторного введення антибіотика.
Відмічається «не застосовується», якщо під час оперативного втручання відсутнє проникнення у колонізовану нормальною мікрофлорою частину тіла або порожнину при запланованих та контрольованих умовах (хірургічна рана відповідає визначенню чистої);
4) у підпункті 11.2.4 відмічається про обговорення очікуваних критичних подій під час операції зі сторони хірурга, зі сторони анестезіолога, зі сторони сестер медичних операційних та можливого реагування на них. За відсутності у операційної бригади готовності реагувати на критичні події та надати весь комплекс допомоги пацієнту в разі їх виникнення переходити до наступних дій забороняється;
5) у підпункті 11.2.5 відмічається «так» у разі забезпечення візуалізації необхідних для проведення оперативного втручання зображень та відсутності будь-яких зауважень до її якості. У разі відсутності необхідної візуалізації зображень, переходити до наступних дій забороняється. Відмічається «не застосовується», якщо проведення оперативного втручання не потребує візуалізації зображень.
7. Підпункт 11.3 заповнюється за обов’язкової присутності щонайменше хірурга, сестри медичної операційної, сестри медичної-анестезиста та анестезіолога:
1) у підпункті 11.3.1 відмічається виконаним або невиконаним щодо проведення хірургом/сестрою медичною операційною уточнення назви проведеної процедури/операції, підрахунку інструментів, тампонів, голок та інших медичних виробів, перевірки правильності маркування біологічних зразків, фіксації усно або письмово наявності проблем із обладнанням, що потребують усунення. У разі невиконання підрахунку інструментів, тампонів, голок та інших медичних виробів, фіксації усно або письмово наявності проблем із обладнанням, що потребують усунення, переходити до наступних дій забороняється;
2) у підпункті 11.3.2 відмічається виконаним або невиконаним щодо узгодження хірургом та анестезіологом плану післяопераційного ведення і реабілітації пацієнта, включно з діями, які необхідно виконати в операційній до переведення пацієнта в післяопераційне відділення/палату. У разі невиконання цього підпункту операційній бригаді покидати операційну заборонено.
8. Пункт 11 форми 008/о не заповнюється, в разі якщо оперативне втручання є невідкладним (виконується для врятування життя пацієнта, без попередньої підготовки).
9. У пункті 12 надається детальний опис ходу операції, де вказуються вид знеболення, доза наркотичного препарату, відмічається тривалість операції, стан хворого під час оперативного втручання, а також вказуються лікувальні заходи, які проводились в період проведення оперативного втручання (ін’єкції препаратів, інсуфляція кисню тощо).
10. Пункти 1–9 та 12 форми № 008/о заповнюється лікарями-хірургами розбірливим почерком. Після завершення оперативного втручання форма № 008/о обов’язково завіряється підписом лікаря, який проводив операцію.
11. Пункти 10 та 11 форми № 008/о заповнюється сестрою медичною-анестезистом до початку оперативного втручання та після його завершення. Після завершення оперативного втручання інформація заповнена у пункті 11 форми № 008/о обов’язково завіряється підписом сестри медичної-анестезиста, яка заповнювала цю форму.
12. Форма № 008/о заповнюється для кожного оперативного втручання окремо.
13. Форма № 008/о має бути пронумерована, прошита, засвідчена підписом керівника та печаткою закладу охорони здоров’я (за наявності).
14. У разі ведення форми № 008/о в електронному форматі в неї має бути включена вся інформація, яка міститься на затвердженому паперовому носії.
15. Термін зберігання форми № 008/о — 50 років.«.
6. У Стандарті інфекційного контролю для закладів охорони здоров’я, що надають допомогу хворим на туберкульоз, затвердженому наказом Міністерства охорони здоров’я України від 01 лютого 2019 року № 287, зареєстрованому в Міністерстві юстиції України 17 квітня 2019 року за № 408/33379:
1) у розділі II:
у пункті 2:
абзац другий викласти в такій редакції:
«створення відділу з інфекційного контролю (далі — ВІК);»;
абзац дев’ятий викласти в такій редакції:
«Організація ІК ТБ у закладах, що надають допомогу хворим на туберкульоз, покладається на керівника ВІК. ВІК створюється відповідно до Положення про відділ з інфекційного контролю закладу охорони здоров’я та установи / закладу надання соціальних послуг / соціального захисту населення, затвердженого наказом Міністерства охорони здоров’я України від 03 серпня 2021 року № 1614. Посадові інструкції працівників затверджуються керівником закладу.»;
абзаци десятий — шістнадцятий виключити. У зв’язку з цим абзаци сімнадцятий — дев’яностий вважати відповідно абзацами десятим — вісімдесят третім;
речення третє абзацу двадцять шостого виключити;
речення друге абзацу двадцять дев’ятого викласти в такій редакції:
«Дозволяється застосовувати когортну ізоляцію не більше двох пацієнтів в одній палаті за умови підтвердження ідентичного профілю резистентності до протитуберкульозних препаратів першого та другого ряду за допомогою молекулярно-генетичних методів діагностики туберкульозу.»;
у абзаці тридцять третьому слова «таких процедур» замінити словами «проведення аерозольгенеруючих процедур, таких як»;
у абзаці сороковому слово «підвищеним» замінити словом «високим»;
у абзаці сорок першому слова «місці з посиленою вентиляцією» замінити словами «окремому приміщенні (рекомендовано в приміщенні з негативним тиском)»;
абзац сорок другий доповнити новим реченням такого змісту:
«Медичні працівники повинні використовувати респіратори.»;
у абзаці сорок четвертому слова «та інших пристроїв знезаражування повітря», «сертифікованих» виключити;
у абзаці сорок п’ятому слова «бактеріальних фільтрів» замінити словами «фільтрів, спеціальних режимів дезінфекції після проведення процедур»;
абзац сорок восьмий після слів «його треба виписати» доповнити словами «для продовження лікування»;
абзац сорок восьмий доповнити новим реченням такого змісту:
«З цією метою на рівні регіону розробляється та затверджується маршрут пацієнта із захворюванням на туберкульоз.»;
абзац п’ятдесят третій після слів «перебування у приміщенні» доповнити словами «поза межами палати»;
у пункті 4:
абзац перший викласти в такій редакції:
«4. З огляду на поширення туберкульозної інфекції через інфекційний аерозоль, індивідуальний захист органів дихання має мінімізувати проникнення до дихальних шляхів часточок, що можуть містити інфекційний агент. Це забезпечується використанням респіраторів класу захисту FFP2 і FFP3.»;
у абзаці четвертому після слів «контагіозним хворим» доповнити словами «або хворим з підозрою на туберкульоз»;
у абзаці п’ятому слово «КІК» замінити словом «ВІК»;
абзац сьомий викласти в такій редакції:
«Для правильного вибору розміру індивідуального респіратора і правильного його надягання перед першим застосуванням необхідно провести якісний або кількісний тест на щільність прилягання респіратора до обличчя („фіт-тест“). Надалі „фіт-тести“ проводяться не рідше одного разу на рік, а також у разі переходу на інший вид респіратора та зміни анатомії обличчя (шрами, косметична хірургія, зміна маси тіла тощо). Під час підбору і користування респіратором не допускається носіння працівником бороди. Методику проведення якісного „фіт-тесту“ наведено в додатку 4 до цього Стандарту.»;
в абзаці восьмому слова «(медична сестра)» замінити словами «(наприклад, сестра медична стаціонару)»;
2) пункт 1 розділу V викласти в такій редакції:
«1. Моніторинг заходів ІК ТБ в ЗОЗ проводиться ВІК постійно, фахівцями територіальних закладів громадського здоров’я відповідно до адміністративно-територіальної належності не рідше одного разу на рік і фахівцями державної установи „Центр громадського здоров’я Міністерства охорони здоров’я України“ не рідше одного разу на два роки (обласні та Київський міський протитуберкульозні заклади охорони здоров’я).»;
3) у додатках до Стандарту:
додатки 2, 3 виключити, у зв’язку з цим додатки 4–6 вважати відповідно додатками 2–4;
додаток 2 викласти в такій редакції:
«Додаток 2
до Стандарту інфекційного контролю для закладів охорони здоров’я,
що надають допомогу хворим на туберкульоз
(пункт 2 розділу II)
Заходи інфекційного контролю під час збору мокротиння
1. Необхідність у зборі мокротиння постійно виникає у закладах, що надають первинну медичну допомогу, стаціонарних відділеннях пульмонологічного профілю і протитуберкульозних закладах. У кожному такому закладі з урахуванням місцевої специфіки має бути розроблено положення (наказ, протокол) про умови і правила збору мокротиння, в якому призначаються відповідальні особи, визначається місце й інженерні вимоги до устаткування, що використовується, регламентується забезпечення витратними матеріалами, визначаються обов’язки персоналу та хворих, детально описується методика якісного та безпечного здійснення збору мокротиння і визначається процедура контролю виконання.
2. Стандартна операційна процедура збору мокротиння:
1) призначається відповідальна особа за збір мокротиння в закладі;
2) збір мокротиння всередині закладу здійснюється у спеціальному приміщенні (пункт збору мокротиння). Приміщення необхідно розділити скляною перегородкою (або облаштувати вікно в перегородці) на дві частини: для збирання мокротиння та для медичного персоналу, який контролює цей процес. Оптимально збирати мокротиння у спеціальних кабінах, обладнаних механічною вентиляцією, що забезпечує кратність повітрообміну по витяжці не менше 20. Викид повітря, що видаляється, організовується таким чином, щоб уникнути потрапляння інфекційного аерозолю назад в приміщення. У пункті збору мокротиння обов’язково встановлюється екранований та відкритий УФ-опромінювачі;
3) за неможливості облаштувати приміщення для збору мокротиння відповідно до зазначених вимог альтернативою є збір мокротиння на відкритому повітрі. Такий варіант є також найбільш доцільним, якщо збір мокротиння не є рутинною діагностичною процедурою в закладі (наприклад, спеціалізовані амбулаторні та стаціонарні заклади іншого, ніж пульмонологічний, профілю);
4) всі процедури, пов’язані з індукуванням кашлю, слід проводити у спеціальних кабінах або відведених для цього приміщеннях із негативним тиском. Пацієнти повинні залишатися в кабінах або приміщеннях до припинення виділення мокротиння і кашлю. Входити до кабіни або приміщення персоналу та іншим хворим дозволяється лише після завершення знезараження контамінованого повітря шляхом бактерицидного УФ-опромінення при роботі відкритого УФ опромінювача;
5) якщо пацієнт збирає мокротиння вдома, відповідальна особа має пояснити всі ризики цієї процедури та рекомендувати, щоб збір мокротиння проходив на відкритому повітрі або в окремому приміщенні перед відкритим вікном, без присутності інших людей;
6) у разі якщо мокротиння необхідно зібрати у пацієнта, який перебуває у тяжкому стані, треба попросити людей, не задіяних у процесі, вийти з приміщення. Збір мокротиння проводити за ввімкненого УФ-випромінювача екранованого типу при закритих дверях. Після збору мокротиння необхідно провітрити приміщення. Медичний працівник під час збору мокротиння повинен надягати респіратор класу захисту FFP3, халат захисний (за необхідності) та медичні рукавички;
7) якщо збір мокротиння проводиться в кімнаті збору мокротиння, медичному працівникові слід вийти з кабінету, де пацієнт відкашлює мокроту, і спостерігати за пацієнтом через скляну частину дверей.
Стандартна операційна процедура «Збір мокротиння»
від __ / ________ / 20__ року
Посада |
П. І. Б. |
Підпис |
|
Розробив |
|||
Погодив |
Керівник ВІК |
||
Підписав |
Керівник ЗОЗ |
||
Дата наступного перегляду: ___ / ________ / 20__ року" |
|||
Мета |
Зниження ризику поширення інфекційного аерозолю в приміщеннях закладу та попередження інфікування медичного персоналу. |
Виконавці |
Відповідальна особа (сестра медична). |
Місце проведення |
Спеціально обладнана кімната або відкритий майданчик збору мокротиння. |
Необхідне обладнання для спеціальної кімнати |
УФ-опромінювач (відкритого та екранованого типу) |
Послідовність дій |
1. Медичний працівник одягає респіратор та медичні рукавички. |
У разі якщо мокротиння необхідно зібрати у пацієнта, який знаходиться у тяжкому стані, слід попросити вийти із кімнати/палати людей, які не задіяні в процесі. Збір мокротиння проводиться за ввімкненого УФ-опромінювача екранованого типу. Після закінчення процедури необхідно провітрити приміщення. |
|
Якщо пацієнт збирає мокротиння вдома, відповідальна особа має пояснити всі ризики даної процедури та рекомендувати, аби збір мокротиння проходив на відкритому повітрі або в окремому приміщенні перед відчиненим вікном, без присутності інших людей. |
|
Заборонено проводити процедуру індукції мокротиння у приміщеннях, не обладнаних механічною вентиляцією. За таких умов рекомендовано проводити процедуру на відкритому повітрі (спеціально відведеному майданчику). |
|
* час роботи відкритого УФ опромінювача визначається за формулою: t (с) = 10000/р, де Отриманий результат округлюється в більшу сторону до кількості хвилин. Використання більшої кількості бактерицидних УФ-ламп дає змогу зменшити час дезінфекції приміщення. |
|
»;
відмітку додатка 3 викласти в такій редакції:
«Додаток 3
до Стандарту інфекційного контролю для закладів охорони здоров’я,
що надають допомогу хворим на туберкульоз
(пункт 2 розділу II)»;
додаток 4 викласти в такій редакції:
«Додаток 4
до Стандарту інфекційного контролю для закладів охорони здоров’я,
що надають допомогу хворим на туберкульоз
(пункт 4 розділу II)
Методика проведення якісного «фіт-тесту»
«Фіт тест» (тест на щільність прилягання респіратора) є ключовим етапом програми респіраторного захисту, оскільки це єдиний визнаний інструмент для оцінки відповідності певної моделі та розміру респіратора до обличчя користувача. Працівникам дозволяється використовувати тільки марку, модель і розмір респіратора або респіраторів, у яких вони успішно пройшли «фіт-тест». «Фіт-тест» є обов’язковим для всіх користувачів респіраторів. Цей тест гарантує, що у разі правильного надівання обрана модель і розмір респіратора підходить для адекватного захисту користувача. Цей тест слід повторювати щороку і кожного разу, коли у працівника спостерігаються зміни у фізичному стані організму, такі як збільшення ваги або її втрата, рубці на обличчі, стоматологічні протези тощо. «Фіт-тест» буває двох типів — якісний та кількісний. Принцип якісного «фіт-тесту» полягає в тому, що під спеціальний ковпак розпиляється речовина, яка під час потрапляння на рецептори язика викликає відчуття смаку (наприклад, солодкого чи гіркого). Наявність відчуття смаку є свідченням того, що тест вважається не пройденим. Принцип кількісного «фіт-тесту» полягає в тому, що за допомогою спеціального обладнання (лічильника часточок) вимірюється концентрація часточок у повітрі приміщення і в просторі між обличчям та респіратором. Під час порівняння цих концентрацій оцінюється ступінь протиаерозольного захисту. Особа, яка проводить «фіт-тест» працівникам, має бути компетентною, проте для цього не потрібна спеціальна сертифікація або ліцензування. Визначені особи, які проводять тест, повинні вміти готувати тестові розчини, регулювати обладнання, правильно проводити перевірку, виявляти негативний результат і забезпечувати правильну роботу обладнання, навчати персонал правилам надівання і знімання респіраторів.
Процедура тестування полягає в розпиленні тестового агента (бітрекс — гіркий, сахарин — солодкий) під ковпак при надітому респіраторі. Якщо досліджуваний не відчуває смаку, це означає, що респіратор досить щільно прилягає до обличчя. До набору для проведення тесту входять: небулайзер, ковпак, комір, розчини для визначення чутливості та тестування.
Методика проведення тесту
1. Тест на чутливість (проводиться без надівання респіратора) проводиться з метою визначення, чи може досліджуваний відчувати смак тестового агента.
Методика проведення тесту на чутливість:
досліджуваний не повинен їсти, пити (окрім води), курити та жувати гумку за 15 хвилин до проведення тесту;
під час проведення оцінки чутливості досліджуваний дихає через відкритий рот зі злегка висунутим язиком;
досліджуваного просять повідомити, коли він (вона) відчує смак:
10 натискань (якщо відчуває смак, перейти до «фіт-тесту»);
ще 10 натискань (якщо відчуває смак, перейти до «фіт-тесту»);
ще 10 натискань (якщо відчуває смак, перейти до «фіт-тесту»). Якщо не відчуває, тестовий агент не може використовуватися для проведення «фіт-тесту» досліджуваному.
Кількість натискань в тесті на чутливість впливає на кількість натискань в наступному етапі.
2. «Фіт-тест»:
1) процедура проведення:
досліджуваний не повинен їсти, пити (окрім води), курити та жувати гумку за 15 хвилин до проведення тесту;
досліджуваний надіває ковпак при одягненому респіраторі;
респіратор має бути правильно надітим, підігнаним;
2) методика проведення:
так само як і під час тесту на чутливість, досліджуваний дихає через відкритий рот із незначно висунутим язиком;
досліджуваного просять повідомити, коли він (вона) відчує смак;
сопло небулайзера вставляють у отвір ковпака і початкова концентрація тестового розчину вводиться під ковпак такою самою кількістю натискань на небулайзер, що і в тесті на чутливість (10, 20 чи 30);
досліджуваного просять виконувати вправи протягом однієї хвилини (таблиця).
Методика проведення «фіт-тесту»
Таблиця
Використаний час |
Кількість розпилювань |
Вправа |
00:00 |
10/20/30 |
Звичайне дихання |
00:30 |
5/10/15 |
|
01:00 |
5/10/15 |
Глибоке дихання |
01:30 |
5/10/15 |
|
02:00 |
5/10/15 |
Повороти головою з боку в бік |
02:30 |
5/10/15 |
|
03:00 |
5/10/15 |
Рухи вверх-вниз головою |
03:30 |
5/10/15 |
|
04:00 |
5/10/15 |
Безперервна розмова |
04:30 |
5/10/15 |
|
05:00 |
5/10/15 |
Біг/ходьба на місці (або наклони тулуба) |
05:30 |
5/10/15 |
|
6:00 |
5/10/15 |
Звичайне дихання |
06:30 |
5/10/15 |
|
07:00 |
Стоп |
Завершення облікових записів |
3. Результат «фіт-тесту»:
досліджуваний має повідомити, чи він (вона) відчуває смак тестового агента;
якщо досліджуваний не відчуває смаку під час тесту, «фіт-тест» вважається позитивним (пройденим);
якщо досліджуваний повідомляє про появу смаку, «фіт-тест» вважається негативним і його потрібно провести повторно з іншим респіратором.
Після проходження «фіт-тесту» оформлюється протокол, який має зберігатися у закладі упродовж року до наступного «фіт-тесту». Конкретної форми такого протоколу в Україні не затверджено. Рекомендовано, щоб він містив таку інформацію: прізвище, ім’я, по батькові (за наявності) працівника, посада; тип «фіт-тесту»; специфічна марка, модель і розмір респіратора, в якому працівника тестують; дата проведення випробування; результат якісного тесту або роздруківка результату кількісного тесту, а також був складений за наведеним зразком.
Зразок
ПРОТОКОЛ
проходження «фіт-тесту»
заклад _____________________________________________________________________ підрозділ _____________________________________________________________________ |
|||||||||
Дата проходження тесту |
|||||||||
П. І. Б. працівника та підпис |
|||||||||
Посада |
|||||||||
Респіратор |
Не багаторазового використання
|
Багаторазового використання
|
|||||||
Марка / модель респіратора |
|||||||||
Розмір респіратора |
|
||||||||
Тип «фіт-тесту» |
|
||||||||
Поріг чутливості |
|
||||||||
Результат тесту |
|
||||||||
Особа, що проводила тест |
|||||||||
________ |
7. У Заходах та Засобах щодо попередження інфікування при проведенні догляду за пацієнтами, затверджених наказом Міністерства охорони здоров’я України від 03 серпня 2020 року № 1777, зареєстрованих в Міністерстві юстиції України 10 листопада 2020 року за № 1110/35393:
1) у розділі I:
у пункті 4:
абзац третій викласти в такій редакції:
«аерозольгенеруючі процедури — процедури, при проведенні яких може утворюватися велика кількість дрібних часточок, які містять патогени, що збільшує ймовірність інфікування через контакт цих дрібних часточок із слизовими оболонками або шляхом їх вдиханням. До аерозольгенеруючих процедур відносяться такі процедури/маніпуляції, але не обмежуються ними: інтубація та екстубація трахеї, трахеотомія, трахеостомія та догляд за трахеостомою, аспіраційна санація трахео-бронхіального дерева, забір мокротиння, індукція мокротиння з використанням небулайзера та сольового розчину, бронхоскопія, мануальна штучна вентиляція легень з використанням самороздувного дихального мішка типу АМБУ, неінвазивна вентиляція легень з використанням режимів BiPAP, CPAP, високочастотна осциляторна вентиляція (HFOV), високопоточна назальна оксигенація (HFNO), інгаляційне введення ліків, дослідження функцій дихання, аутопсія та інші клінічні, хірургічні і лабораторні процедури, які можуть призводити до утворення дрібнодисперсного аерозолю (наприклад, використання операційної кісткової пилки, центрифуги, гастроскопу, аспіраційного обладнання);»
абзац четвертий викласти в такій редакції:
«алогенна трансплантація (алотрансплантація) — вид трансплантації, при якому пересаджують орган чи тканину від однієї особи (донор) до іншої генетично відмінної особи (реципієнт) того самого виду;»;
після абзацу четвертого доповнити абзацом п’ятим в такій редакції:
«антимікробна хіміопрофілактика (далі — хіміопрофілактика) — це практика використання антимікробних препаратів (антибактеріальні, противірусні, антипротозойні та протигрибкові препарати) з метою попередження розвитку інфекційного захворювання після контакту із інфекційним агентом, серед певних категорій населення протягом визначеного періоду часу, у випадку асимптоматичної чи повільної латентної інфекції, у разі подорожі до/з країн, в яких є високий ризик інфікування, перед проведенням оперативного втручання для запобігання розвитку інфекції області хірургічного втручання;».
У зв’язку з цим абзаци п’ятий-тридцять дев’ятий вважати відповідно абзацами шостим-сороковим;
абзац сьомий викласти в такій редакції:
«віспа мавп — рідкісне вірусне зоонозне природно-осередкове захворювання, що поширене у Центральній та Західній Африці та спричинюється вірусами родини поксвірусів, і за своїми клінічними проявами має подібність до натуральної віспи;»;
у абзаці одинадцятому слово «епілептичні» замінити словом «судомні»;
абзац п’ятнадцятий викласти в такій редакції:
«колонізація інфекційними агентами (мікроорганізмами) — наявність мікроорганізмів на частинах тіла або всередині організму (шкіра, ротова та носова порожнина, шлунково-кишковий тракт, дихальні шляхи) людини без клінічних проявів захворювання;»;
абзац двадцять третій викласти в такій редакції:
«респіраторна терапія — комплекс заходів, які спрямовані на підтримку та відновлення вентиляції і газообміну в легенях;»;
абзац двадцять сьомий викласти в такій редакції:
«хвороба Крейтцфельда-Якоба (далі — ХКЯ), також відома як підгостра спонгіоформна енцефалопатія — фатальне прогресуюче нейродегенеративне захворювання, що викликане специфічним інфекційним білковим агентом (пріоном);
абзац двадцять дев’ятий виключити. У зв’язку з цим абзаци тридцятий — сороковий вважати відповідно абзацами двадцять дев’ятим — тридцять дев’ятим;
абзац тридцять перший викласти в такій редакції:
«ВІК — відділ з інфекційного контролю;»;
абзац тридцять сьомий викласти в такій редакції:
«СОП — стандартна операційна процедура;»;
2) у розділі II:
пункт 4 викласти в такій редакції:
«4. Інфекційна хвороба — найвищий ступінь вираженості інфекційного процесу, що виник, як результат складної взаємодії між макроорганізмом, інфекційним агентом (мікроорганізмом), навколишнім середовищем та проявляється переважанням патологічних реакцій над пристосувальними з поєднаним порушенням гомеостазу. Характеристики інфекційного агента, які впливають на розвиток інфекційного захворювання: патогенність, вірулентність та антигенність, а також інфікуюча доза, шляхи інфікування. Спектр можливих результатів після взаємодії потенційного хазяїна та інфекційного агенту варіює від безсимптомного захворювання до тяжкої хвороби із летальним наслідком. Деякі особи схильні до тимчасової або хронічної колонізації (носійства), але не хворіють, інші ж можуть захворіти після багатьох років колонізації інфекційним агентом. Чинниками, які підвищують сприйнятливість організму до інфекцій, є: літній вік, відмова від вакцинації, деякі захворювання (ВІЛ/СНІД, онкологічні хвороби, цукровий діабет, вроджені імунодефіцити), стан після трансплантації стовбурових гемопоетичних клітин, вживання певних груп лікарських засобів (антимікробні препарати, кортикостероїди, протипухлинні та імуномодулюючі препарати, засоби, що знижують кислотність шлунку), опромінення. Такі медичні пристрої як сечові катетери, ендотрахеальні та трахеостомічні трубки, імплантовані кардіовертери-дефібрилятори, ендопротези, металоконструкції, периферійні та центральні венозні і артеріальні катетери полегшують виникнення ІПНМД та можуть бути джерелом утворення біоплівок, які сприяють колонізації і здатні захищати мікроорганізми від проникнення антимікробних засобів.»;
друге речення пункту 8 викласти в такій редакції:
«ЗІЗ, навіть при правильному використанні, можуть відігравати роль в процесі інфікування пацієнтів (опосередковане інфікування).»;
пункт 9 викласти в такій редакції:
«9. Інфікування крапельним шляхом, фізично, є формою контактного інфікування і деякі інфекційні агенти, які передаються крапельним шляхом, також можуть передаватися шляхом прямого або опосередкованого контакту. Однак, на відміну від контактного інфікування, контаміновані інфекційним агентом краплі з дихальних шляхів інфікують потенційного хазяїна лише у випадку потрапляння на сприйнятливі слизові оболонки. При цьому відстань між особами має бути незначною, а убезпечитися можна шляхом захисту обличчя. Хворий генерує респіраторні краплі під час кашлю, чхання та розмови або під час таких процедур як ендотрахеальна інтубація, відсмоктування слизу, індукція кашлю за допомогою фізіотерапевтичних методів та під час серцево-легеневої реанімації. Дослідження показали, що слизові оболонки носа і кон’юнктива (рідше слизова ротової порожнини) — основні вхідні ворота для вірусів респіраторної групи. Максимальна відстань між людьми, яка достатня для передавання інфекційного агента через краплі не визначена. Вона залежить від швидкості і механізму виходу крапель, їхньої щільності, наявності перешкод, чинників навколишнього середовища, таких як температура, вологість, напрям та сила руху повітря, інсоляція, здатність патогену підтримувати свою вірулентність на відстані. В приміщеннях рекомендовано надягати ЗІЗ обличчя до входу в палату пацієнта, особливо коли існує ймовірність інфікування високовірулентним інфекційним агентом.»;
3) у розділі III:
перше речення абзацу другого пункту 3 викласти в такій редакції:
«Профілактика інфікування має засновуватися на використанні контактних заходів захисту при контактах з пацієнтами з діареєю, точній ідентифікації хворих, контактних осіб, та носіїв інфекційних агентів, заходах з охорони внутрішнього середовища ЗОЗ або ЗСЗ (наприклад, ретельне прибирання кімнат/палат) і постійній гігієні рук.»;
пункт 4 викласти в такій редакції:
«4. Незважаючи на те, що назва деяких МРМО говорить про резистентність лише до одного препарату (наприклад, МРЗС або ВРЕ), такі мікроорганізми зазвичай стійкі практично до всіх доступних АМП (ця особливість і визначає важливість таких мікроорганізмів для госпітальної епідеміології). До групи МРМО, які мають особливе значення для госпітальної епідеміології, відносяться:
1) інфекційні агенти надзвичайного рівня загрози: карбапенем-резистентний Acinetobacter, Candida auris, Clostridioides difficile, карбапенем-резистентні Enterobacteriaceae, антибіотикорезистентна Neisseria gonorrhoeae;
2) інфекційні агенти високого рівня загрози: антибіотикорезистентний Campylobacter, резистентна до протигрибкових лікарських засобів Candida, Enterobacteriaceae продуценти бета-лактамаз розширеного спектру (далі — ПБЛРС), ванкоміцин-резистентні Enterococci, мультирезистентна Pseudomonas aeruginosa, мультирезистентна нетифоїдна Salmonella, антибіотикорезистентна Salmonella серотип Typhi, антибіотикорезистентна Shigella, метицилін-резистентний (MRSA), помірно чутливий до ванкоміцину (ПЧВЗС) та ванкоміцин-резистентний (ВРЗС) Staphylococcus aureus, мультирезистентний Streptococcus pneumoniae (МРСП), антибіотикорезистентна M. tuberculosis;
3) інфекційні агенти, що розглядаються, як можливі загрози: еритроміцин-резистентний Streptococcus групи A, кліндаміцин-резистентний Streptococcus групи B;
4) інфекційні агенти, ризик яких для госпітальної епідеміології досліджується: азол-резистентний Aspergillus fumigatus, антибіотикорезистентна Mycoplasma genitalium, антибіотикорезистентна Bordetella pertussis.»;
пункт 11 викласти в такій редакції:
«11. Пріонні захворювання у тварин включають скрепі у овець і кіз, губчасту енцефалопатію великої рогатої худоби („коров’ячий сказ“, далі — КГЕ) і хронічну хворобу виснаження у оленів і лосів. Перший випадок КГЕ серед великої рогатої худоби у Великій Британії був пов’язаний зі споживанням інфікованого корму у вигляді м’ясо-кісткового борошна, який був виготовлений з туш інфікованих тварин.»;
пункт 22 викласти в такій редакції:
«22. До вірусних геморагічних гарячок (далі — ВГГ), що становлять найбільшу епідемічну небезпеку належать:
1) гарячки, що викликані вірусами Ебола та Марбург (Filoviridae);
2) гарячка Ласса (Arenaviridae);
3) гарячка долини Ріфт та Крим-Конго (Bunyaviridae);
4) гарячка денге та жовта гарячка (Flaviviridae).»;
номер пункту 20, який слідує за пунктом 22, замінити на 23, у зв’язку з цим пункти 23–24 вважати відповідно пунктами 24–25;
4) у розділі IV:
третє, четверте речення пункту 10 викласти в такій редакції:
«Крім того, серед госпіталізованих немовлят та дітей молодшого віку відзначається висока частота розвитку інфекційних хвороб, не характерних для загальної популяції, що пояснюється відсутністю набутого імунітету до цих інфекцій (внаслідок природньо перенесеної хвороби чи після вакцинації). Це призводить до розповсюдження інфекційних хвороб з крапельним шляхом інфікування серед пацієнтів педіатричних стаціонарів, особливо в період сезонних епідемій (наприклад, кашлюк, респіраторні вірусні інфекції, в тому числі викликані РСВ, вірусами грипу, парагрипу, метапневмовірусом, аденовірусом, вірусом кору, вірусом вітряної віспи, ротавірусом).»;
пункт 22 викласти в такій редакції:
«22. Інфекційні хвороби, щодо яких мають бути впроваджені заходи ПІІК в ЗСЗ, включають:
1) туберкульоз;
2) короста;
3) респіраторні вірусні інфекції;
4) грип;
5) менінгококова інфекція;
4) захворювання, що передаються через кров (наприклад, ВІЛ-інфекція, гепатити B і C, сифіліс);
5) кишкові інфекції (наприклад, гепатит А, норовірусна і ротавірусні інфекції).
Крім того, слід проводити скринінг (анкетування) щодо туберкульозу серед пацієнтів ЗСЗ та заохочувати їх до проведення вакцинації.»;
пункт 28 викласти в такій редакції:
«28. Потенційна небезпека передавання інфекційних агентів через біологічні препарати (кров, органи і тканини) є можливою, незважаючи на скринінг донорів.
Основні інфекції, стосовно яких має бути настороженість:
1) ВІЛ;
2) вірусні гепатити B і C;
3) цитомегаловірусна інфекція та Ебштейна-Барр-вірусна інфекція;
4) сифіліс;
5) туберкульоз (особливо при трансплантації легень);
6) токсоплазмоз (особливо при трансплантації серця);
7) лихоманка Західного Нілу;
8) стронгілоїдоз;
9) кокциоїдомікоз;
10) пріонові інфекційні хвороби (ХКЯ);
11) інфекційні хвороби, викликані бактеріями роду Clostridium;
12) малярія;
13) бабезіоз;
14) хвороба Шагаса (Trypanosma cruzi);
15) лімфоцитарний хоріоменінгіт;
16) сказ.
Крім того, при розробці заходів з ПІІК слід приділити увагу оцінці пацієнтів, як потенційних джерел інфекції (активація ендогенної мікрофлори).»;
5) пункт 5 розділу VI викласти в такій редакції:
«5. В підрозділах ЗОЗ/ЗСЗ, де співробітники не мають достатнього досвіду проведення серцево-легеневої реанімації або не можуть ефективно та безпечно проводити штучне дихання варто проводити лише компресії грудної клітини да дефібриляцію. Вентиляція методом рот-в-рот та використання кишенькової плівки-клапана не відповідає вимогам інфекційної безпеки.
В підрозділах ЗОЗ/ЗСЗ, де співробітники мають достатній досвід проведення серцево-легеневої реанімації варто проводити вентиляцію легень з допомогою лицевої маски з клапаном та дихального мішка типу АМБУ дворучним способом якомога коротший термін часу з наступною якнайшвидшою інтубацією трахеї.»;
6) пункт 9 розділу X викласти в такій редакції:
«9. Противірусні лікарські засоби не рекомендовано використовувати рутинно з метою хіміопрофілактики поза межами локальних спалахів захворюваності на грип. Хіміопрофілактика грипу з використанням озельтамівіру (перорально) та занамівіру (інгаляційно) показана для таких груп:
1) дорослі та діти, віком три і більше місяців на тривалість періоду підвищеної захворюваності на грип у випадку наявності захворювань, при яких існує високий ризик виникнення ускладнень і тяжкого перебігу грипу, відповідно до пункту 4 розділу II Календаря профілактичних щеплень в Україні, затвердженого наказом Міністерства охорони здоров’я України від 16 вересня 2011 року № 595, зареєстрованого в Міністерстві юстиції Україні 10 жовтня 2011 року за № 1159/19897 (зі змінами) (далі — високий ризик розвитку ускладнень), та у разі, якщо вакцинація є протипоказаною, недоступною для цих осіб або передбачається її низька ефективність;
2) дорослі та діти віком три і більше місяців на тривалість періоду підвищеної захворюваності на грип у випадку наявності високого ризику розвитку ускладнень та у разі, якщо вакцинація є показаною для цих осіб або передбачається її висока ефективність, але вона не була вчасно проведена (короткотривала хіміопрофілактика у поєднанні з належним введенням інактивованої вакцини від грипу);
3) невакциновані дорослі, в тому числі медичні працівники, та діти віком три і більше місяців на тривалість періоду підвищеної захворюваності на грип, в разі наявності у них постійного тісного контакту з особами, які мають високий ризик розвитку ускладнень та мають протипоказання до вакцинації або вона недоступна і ці особи не можуть приймати противірусні препарати з метою хіміопрофілактики (короткотривала хіміопрофілактика);
4) дорослі та діти віком три і більше місяців на тривалість періоду підвищеної захворюваності на грип у випадку наявності високого ризику розвитку ускладнень та у разі, якщо вакцинація є протипоказаною, недоступною для цих осіб або передбачається її низька ефективність (передконтактна хіміопрофілактика);
5) дорослі та діти віком три і більше місяців, які мають високий ризик розвитку ускладнень і не мають симптомів захворювання після контакту з хворим на грип в родині, та у разі, якщо вакцинація є протипоказаною, недоступною для цих осіб або передбачається її низька ефективність (постконтактна хіміопрофілактика);
6) дорослі та діти віком три і більше місяців, після контакту з хворими на грип, які не були вакциновані, та мають постійний тісний контакт в родині з особами, які мають високий ризик розвитку ускладнень (постконтактна хіміопрофілактика у поєднанні з належним введенням інактивованої вакцини від грипу).
Необхідно невідкладно провести лабораторне підтвердження грипу у пацієнтів, які отримували засоби для передконтактної/постконтактної профілактики та мають симптоми, для підтвердження діагнозу. Якщо діагноз підтверджено, слід призначити противірусні препарати з різним профілем ризику розвитку стійкості у терапевтичних дозах, якщо це не протипоказано.
Постконтактну профілактику необхідно почати не пізніше ніж через 48 годин після контакту з хворим на грип. Повна терапевтична доза противірусного лікарського засобу має бути надана пацієнтові за умови появи симптомів і показів до етіотропного лікування.
У випадках якщо пацієнт, визначений підпунктами 1–6 цього пункту, перебуває поза межами території, на якій триває спалах грипу, постконтактну хіміопрофілактику слід проводити протягом семи днів після останнього тісного контакту з хворим.
У пацієнтів, які перебувають постійно у ЗСЗ, хіміопрофілактику грипу необхідно проводити мінімум протягом 14 днів та закінчувати не раніше ніж через сім днів після початку симптомів у пацієнта, який захворів останнім.
Противірусна хіміопрофілактика має проводитись якнайшвидше всім пацієнтам, які мали контакт з хворим на грип під час перебування в ЗОЗ/ЗСЗ, навіть за відсутності клінічних ознак чи лабораторно підтвердженого грипу, незалежно від наявності/відсутності вакцинації від грипу, якщо немає протипоказань до її проведення.
Працівникам ЗОЗ/ЗСЗ, які отримали вакцинацію від грипу в період спалаху грипу, проводиться противірусна хіміопрофілактика протягом 14 днів після вакцинації.»;
7) у розділі XI:
пункт 6 викласти в такій редакції:
«6. До стандартних заходів захисту відносяться:
1) гігієна рук;
2) використання рукавичок в залежності від методів проведення догляду;
3) використання ХЗІА в залежності від методів проведення догляду;
4) респіраторна гігієна і етикет кашлю, використання масок в залежності від методів проведення догляду;
5) використання захисних окулярів або щитків в залежності від методів проведення догляду;
6) безпека при виконанні ін’єкцій;
7) використання чистого і безпечного обладнання та інструментарію для проведення догляду;
8) безпечне поводження з медичними відходами;
9) очищення та дезінфекція приміщень;
10) використання чистої і безпечної білизни.»;
пункт 15 викласти в такій редакції:
«15. Для безпечного проведення ін’єкцій слід дотримуватися таких правил:
1) для виконання кожної окремої ін’єкції варто підготувати всі необхідні лікарські засоби та витратні матеріали у чистій зоні використовуючи асептичну техніку;
2) перед проколюванням необхідно протерти корок флакону серветкою, змоченою спиртовмісним антисептиком;
3) для виконання кожної окремої ін’єкції слід використовувати окрему одноразову стерильну голку та шприц (одна голка та один шприц для одного пацієнта), в тому числі ручки-ін’єктори з інсуліном чи адреналіном;
4) до та під час виконання ін’єкції уникати забруднення голки, шприца та лікарського засобу, а в разі забруднення негайно припинити процедуру;
5) за можливості, використовувати індивідуальну ємність (флакон, ампулу) з лікарським засобом для кожного окремого пацієнта;
6) отримання лікарського засобу з первинної упаковки (флакон, ампула) для одноразового чи багаторазового застосування має здійснюватися за допомогою нової голки та шприца, навіть за необхідності отримання додаткових доз препарату для одного пацієнта;
7) заборонено набирати дозу лікарського засобу з залишків кількох первинних упаковок (флакон, ампула), які залишились від попереднього пацієнта;
8) дотримуватися правил асептики протягом всієї процедури.»;
в підпункті 6 пункту 26 число «V» замінити числом «VIII»;
8) пункт 6 розділу XII викласти в такій редакції:
«6. Ксенотрансплантація потребує використання суворої ізоляції у ПЗІП у випадку появи у реципієнта тяжкого інфекційного захворювання або виявлення у нього нового рекомбінантного мікроорганізму.
Інші види трансплантації не потребують рутинного використання ПЗІП.»;
9) по тексту Заходів:
слово «в-лактамаз» замінити словом «бета-лактамаз»;
10) по тексту Заходів та у додатках 1, 3, 4, 7, 8 до них слово «КІК» замінити словом «ВІК»;
11) у додатках до цих Заходів:
у позиції двісті дев’ять графи «Інфекційна хвороба/стан» таблиці «Вид і тривалість заходів захисту, що слід використовувати при окремих інфекційних хворобах та станах» додатку 1 слово «Rotavirus» замінити словом «Гастроентерити»;
додаток 5 викласти у такій редакції:
«Додаток 5
до Заходів та Засобів щодо попередження інфікування
при проведенні догляду за пацієнтами
(пункт 1 розділу V)
Підходи одягання і зняття ЗІЗ
Послідовність та правила одягання ЗІЗ
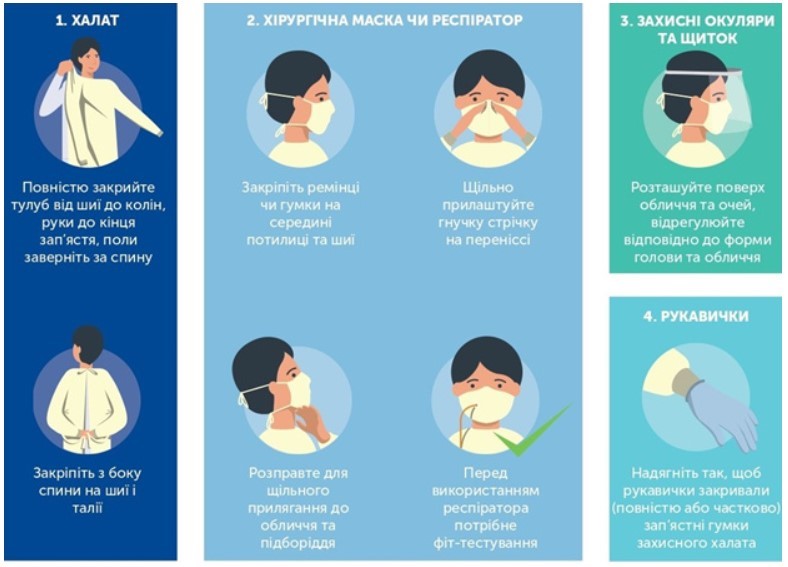
Послідовність та правила зняття ЗІЗ (варіант 1)
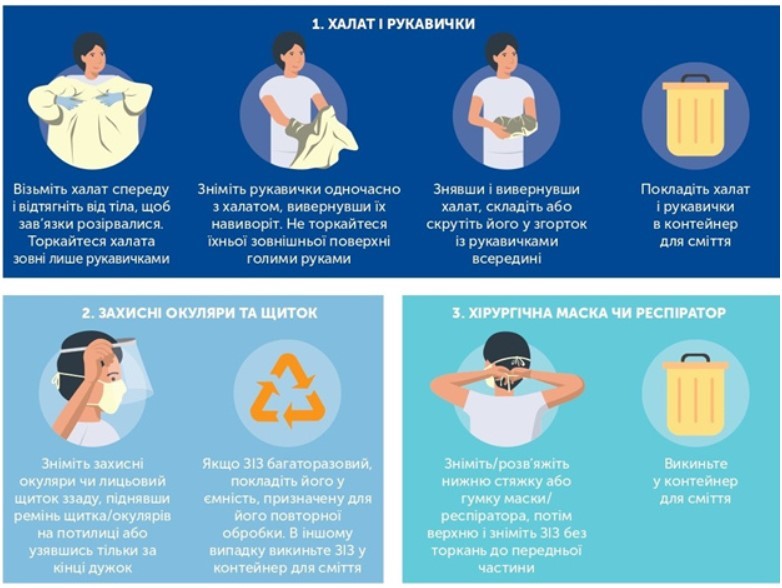
Послідовність та правила зняття ЗІЗ (варіант 2)
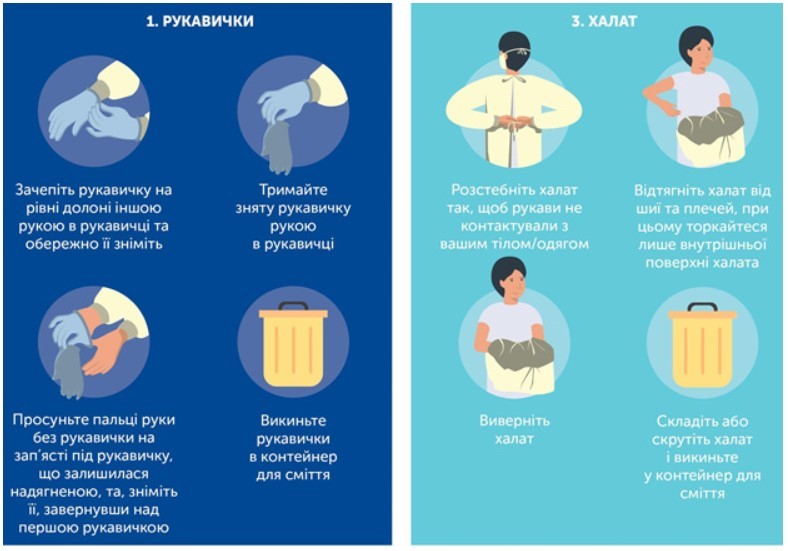

».
8. У розділі VII Порядку проведення епідеміологічного нагляду за кором, краснухою та синдромом вродженої краснухи, затвердженого наказом Міністерства охорони здоров’я України від 23 квітня 2019 року № 954, зареєстрованого в Міністерстві юстиції України 20 травня 2019 року за № 519/33490:
1) пункт 17 виключити. У зв’язку з цим пункти 18–23 вважати відповідно пунктами 17–22;
2) пункт 18 виключити. У зв’язку з цим пункти 19–22 вважати відповідно пунктами 18–21.
9. У пункті 14 Переліку необхідних обстежень лікарів-спеціалістів, видів клінічних, лабораторних та інших досліджень, що необхідні для проведення обов’язкових медичних оглядів, та періодичність їх проведення, затвердженого наказом Міністерства охорони здоров’я України від 23 липня 2002 року № 280, зареєстрованого в Міністерстві юстиції України 08 серпня 2002 року за № 640/6928:
1) в позиції «Адміністрація» графу 12 «мазок з горла та носа на наявність патогенного стафілококу» викласти в такій редакції:
«При проведенні попереднього медогляду»;
2) в позиції «Медичні працівники (лікарі, середній та молодший медичний персонал)» графу 12 «мазок з горла та носа на наявність патогенного стафілококу» викласти в такій редакції:
«При проведенні попереднього медогляду»;
3) в позиції «Технічний персонал, у тому числі прибиральники приміщень» графу 12 «мазок з горла та носа на наявність патогенного стафілококу» викласти в такій редакції:
«При проведенні попереднього медогляду».
Генеральний директор Директорату громадського здоров’я
та профілактики захворюваності
І. Руденко
